Clear Sky Science · it
Inibizione gerarchica delle MYST acetiltransferasi da parte di piccole molecole
Perché i piccoli interruttori sul DNA contano per il trattamento del cancro
All'interno di ogni cellula, interruttori chimici sul nostro DNA aiutano a decidere quali geni si accendono o si spengono. Un gruppo di enzimi chiamati acetiltransferasi MYST regola finemente questi interruttori ed è stato associato a tumori come il cancro al seno e la leucemia. Questo studio esplora come nuove molecole farmacologiche possano modulare questi enzimi in modo controllato e graduale, offrendo indizi per progettare terapie oncologiche più precise e per interpretare gli studi clinici in corso.
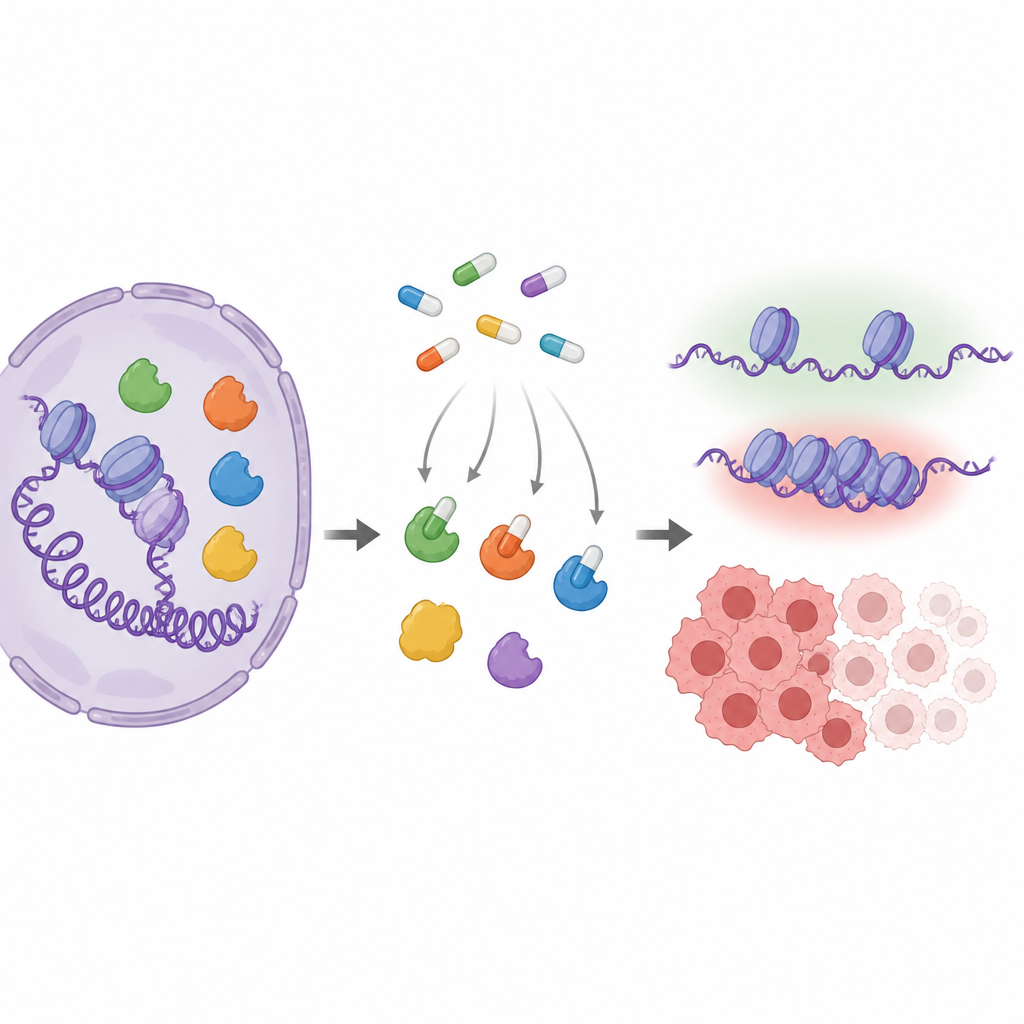
Attori chiave che modulano l'attività genica
Le proteine MYST modificano sottilmente il confezionamento del DNA aggiungendo piccoli gruppi chimici alle proteine dette istoni. Questo confezionamento contribuisce a decidere se i geni coinvolti nella crescita, nella riparazione o nella risposta ormonale sono attivi. Diversi membri di questa famiglia, in particolare KAT6A e KAT6B, risultano alterati o sovraespressi nei tumori, rendendoli bersagli farmacologici interessanti. Le aziende farmaceutiche hanno sviluppato composti simili a pillole che si inseriscono nel sito attivo di questi enzimi, ma poiché i diversi enzimi MYST hanno un aspetto molto simile in quel sito, è difficile sapere esattamente quali vengano colpiti da ciascun farmaco nelle cellule reali.
Misurare quali enzimi colpisce realmente ogni farmaco
Gli autori hanno costruito una strategia di test a più livelli per mappare come un farmaco di punta, PF-9363, e composti correlati interagiscono con le MYST. Per prima cosa hanno usato una molecola “esca” attaccata a perline magnetiche che cattura gli enzimi usando la stessa tasca dove consumano il loro combustibile naturale. Se un farmaco blocca quella tasca, l'enzima non si lega più all'esca. Aggiungendo dosi crescenti di farmaco a estratti nucleari di cellule e poi misurando, con spettrometria di massa, quali proteine restavano legate all'esca, hanno trovato una gerarchia chiara: PF-9363 prima spiazza KAT6A e KAT6B, poi KAT7, poi KAT8 e solo ai livelli più alti KAT5. Lo stesso schema si osserva per il farmaco clinico PF-8144, ora in sperimentazioni per il carcinoma mammario positivo per il recettore degli estrogeni.
Scoprire partner nascosti e letture cellulari chiare
Poiché il blocco della tasca enzimatica indebolisce anche l'aderenza di interi complessi proteici che si legano all'esca, il gruppo ha potuto vedere quali altre proteine viaggiano insieme a ciascuna MYST. Raggruppando le proteine che venivano perse dall'esca con lo stesso profilo di dose dei membri di complessi noti, e combinando questo con predizioni di struttura 3D ed esperimenti cellulari, hanno segnalato il fattore di trascrizione FOXK2 come partner prima non riconosciuto, in particolare legato al complesso NSL contenente KAT8. Successivamente sono passati a cellule tumorali vive ed hanno esaminato centinaia di modifiche chimiche sugli istoni mentre aumentavano la dose di PF-9363. Hanno individuato un piccolo insieme di marchi di acetilazione che riportano in modo affidabile quale enzima MYST è stato bloccato: una modifica su istone H3 (H3K23Ac) per KAT6A/B, un'altra su H3 (H3K14Ac) per KAT7, una su H4 (H4K16Ac) per KAT8 e marcatori sulla variante istonica H2A.Z per KAT5. Questi marcatori possono essere misurati sia mediante spettrometria di massa avanzata sia con blot standard basati su anticorpi, rendendoli pratici per molti laboratori.
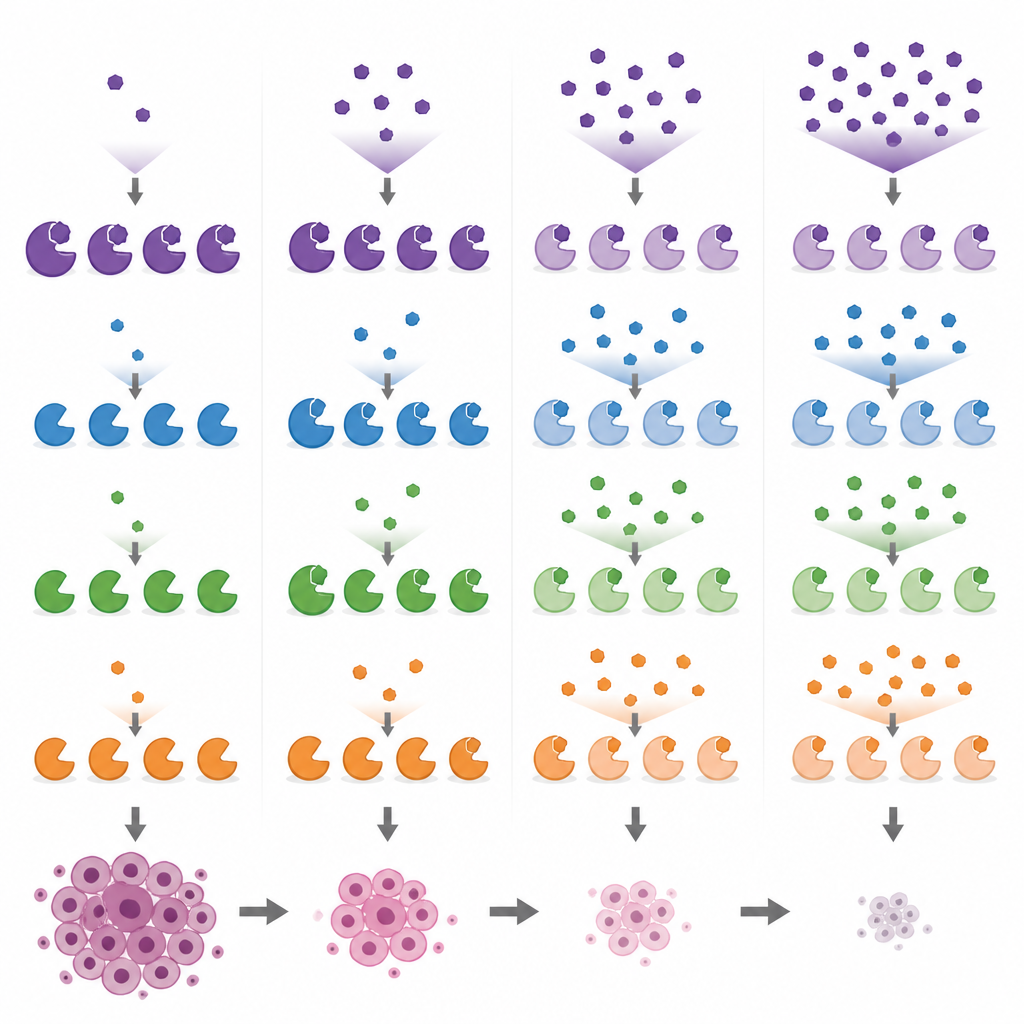
Confrontare farmaci da ricerca popolari e i loro bersagli secondari
Armati di questi indicatori biologici, i ricercatori hanno confrontato diversi composti largamente usati per mirare le MYST in cellule di carcinoma mammario su una gamma di dosi. Hanno mostrato che PF-9363 e il suo cugino clinico PF-8144 seguono entrambi lo stesso schema graduale, arrivando infine a interessare KAT8 a dosi più alte. Al contrario, WM-1119 si è rivelato altamente selettivo per KAT6A/B anche a concentrazioni elevate, mentre WM-8014 e WM-3835 inibiscono prima KAT6A/B e solo successivamente KAT7. Un composto, MOZ-IN-3, che appare potente negli essay in provetta, ha mostrato scarso effetto nelle cellule, probabilmente perché non vi penetra bene. Questi confronti rivelano che alcuni strumenti commercializzati come specifici per un enzima in realtà colpiscono più bersagli, il che può complicare l'interpretazione di esperimenti passati e futuri.
Collegare dose, coinvolgimento enzimatica e crescita delle cellule tumorali
Il gruppo si è poi chiesto se questo schema di inibizione a strati influenzi la risposta delle cellule tumorali. Screening di PF-9363 sulla panel NCI-60 di linee cellulari tumorali ha mostrato che esposizioni brevi a dosi che bloccano solo KAT6A/B e KAT7 hanno effetti modesti sulla crescita. Rallentamenti rapidi e marcati della crescita tipicamente comparivano solo a dosi più alte in cui veniva coinvolto anche KAT8, un enzima essenziale per la maggior parte delle cellule. In una linea di carcinoma mammario triplo-negativo che dipende in modo particolare da KAT8, la dose che riduceva il numero di cellule corrispondeva alla dose che sopprimeva completamente il marcatore istonico legato a KAT8 pur bloccando anche KAT6A/B e KAT7. Ciò suggerisce che per alcuni tumori dosi più elevate di questi farmaci possano agire tramite un'inibizione più ampia delle MYST piuttosto che solo attraverso KAT6A/B.
Cosa significa per i futuri farmaci antitumorali
Nel complesso, lo studio mostra che i bloccanti molecolari delle MYST si comportano in modo simile a molti farmaci per chinasi: a basse dosi colpiscono principalmente i bersagli preferiti, ma all'aumentare della dose si estendono agli enzimi strettamente correlati in un ordine prevedibile. Fornendo letture semplici basate sugli istoni per ciascun membro MYST e rivelando dove i composti popolari sono veramente selettivi, il lavoro offre a ricercatori e clinici un kit di strumenti per abbinare la dose alla copertura enzimatica desiderata. Questo dovrebbe aiutare a progettare studi di laboratorio più chiari, interpretare i risultati degli studi clinici e, in ultima analisi, guidare lo sviluppo di terapie più precise che rimodellano il controllo genico nelle cellule tumorali limitando gli effetti collaterali indesiderati.
Citazione: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Parole chiave: enzimi epigenetici, acetilazione degli istoni, targeting farmacologico del cancro, chemoproteomica, inibitori delle acetiltransferasi della lisina