Clear Sky Science · nl
Hiërarchische remming van MYST-acetyltransferasen door kleine moleculen
Waarom kleine schakelaars op DNA van belang zijn voor kankerbehandeling
In elke cel helpen chemische schakelaars op ons DNA bepalen welke genen aan- of uitgezet worden. Een groep enzymen die MYST-acetyltransferasen heet, stelt deze schakelaars fijn af en is gekoppeld aan kankers zoals borstkanker en leukemie. Deze studie onderzoekt hoe nieuwe geneesmiddelmoleculen deze enzymen gecontroleerd en stapsgewijs kunnen dempen, wat aanwijzingen biedt voor het ontwerpen van preciezere kankerbehandelingen en voor de interpretatie van lopende klinische onderzoeken.
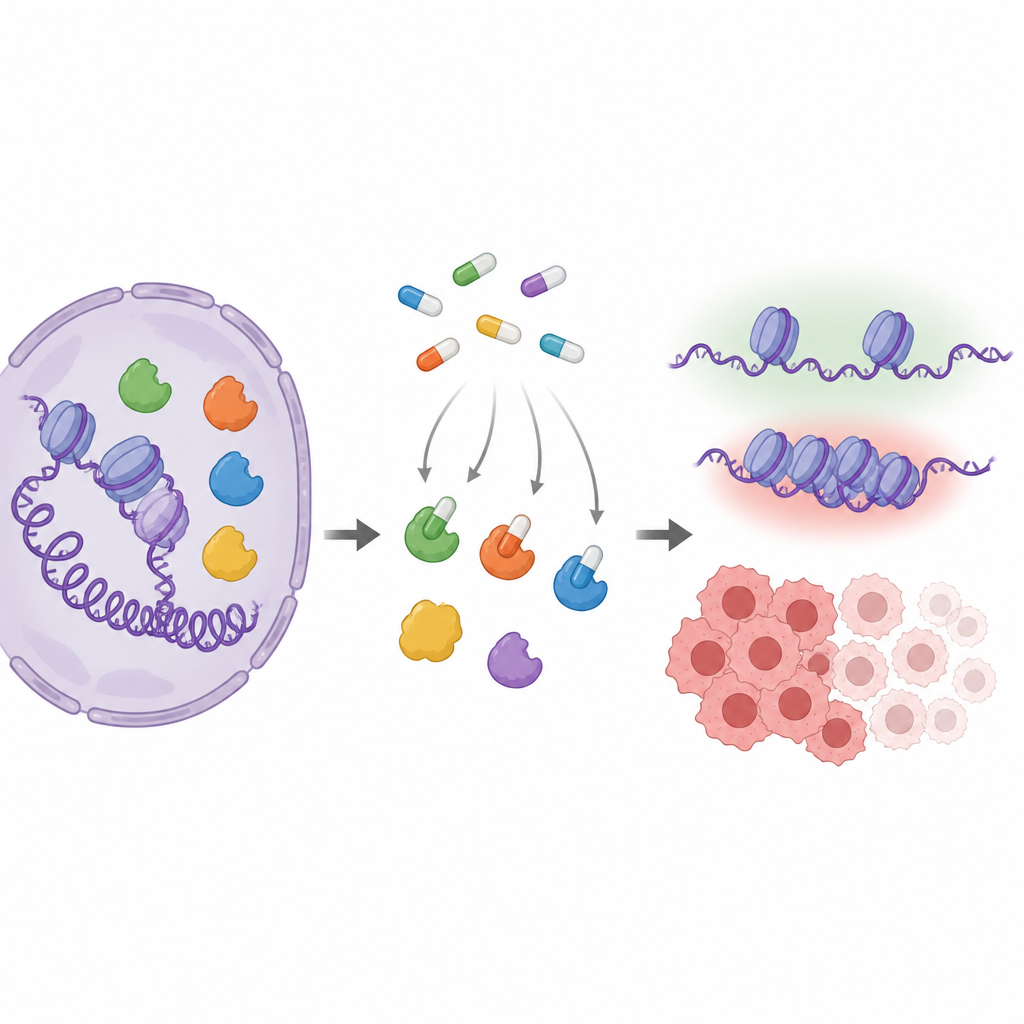
Belangrijke spelers die genactiviteit bijstellen
MYST-enzymen veranderen subtiel hoe DNA is verpakt door kleine chemische labels aan eiwitten genaamd histonen toe te voegen. Die verpakking helpt bepalen of genen die betrokken zijn bij groei, herstel of hormoonrespons actief zijn. Verschillende leden van deze familie, vooral KAT6A en KAT6B, zijn gewijzigd of overgeëxprimeerd in tumoren, wat ze tot aantrekkelijke medicatiedoelen maakt. Farmaceutische bedrijven hebben pilachtige verbindingen ontwikkeld die in de actieve plaats van deze enzymen passen, maar omdat de verschillende MYST-enzymen er in die plek zeer vergelijkbaar uitzien, is het moeilijk precies te weten welke enzymen elk middel in echte cellen treft.
Meten welke enzymen een middel echt raakt
De auteurs bouwden een gelaagde teststrategie om in kaart te brengen hoe een leidend middel, PF-9363, en verwante verbindingen met MYST-enzymen interageren. Eerst gebruikten ze een "aas"-molecuul gekoppeld aan magnetische kralen dat enzymen grijpt via dezelfde pocket waar ze hun natuurlijke brandstof gebruiken. Als een middel die pocket blokkeert, hecht het enzym niet langer aan het aas. Door oplopende medicatiedoses toe te voegen aan nucleaire extracten uit cellen en vervolgens met massaspectrometrie te meten welke eiwitten nog steeds aan het aas gebonden waren, vonden ze een duidelijke hiërarchie: PF-9363 verdrijft eerst KAT6A en KAT6B, daarna KAT7, vervolgens KAT8, en pas bij de hoogste concentraties KAT5. Ditzelfde patroon verschijnt voor het klinische middel PF-8144, dat nu in proeven is voor oestrogeenreceptor-positieve borstkanker.
Verborgen partners en duidelijke cellulaire meetpunten vinden
Aangezien het blokkeren van de enzym-pocket ook de bevestiging van volledige eiwitcomplexen die aan het aas zitten verzwakt, kon het team zien welke andere eiwitten met elk MYST-enzym meereizen. Door eiwitten te clusteren die in hetzelfde dosispatroon van het aas verdwenen als bekende complexleden, en dit te combineren met 3D-structuurvoorspelling en cel-experimenten, identificeerden ze de transcriptiefactor FOXK2 als een eerder onbekende partner, vooral gekoppeld aan het KAT8-bevattende NSL-complex. Vervolgens onderzochten ze levende kankercellen en analyseerden honderden chemische markeringen op histonen terwijl ze de PF-9363-dosis verhoogden. Ze pinpointten een kleine set acetylatiemarkers die betrouwbaar aangeven welk MYST-enzym is geblokkeerd: een merk op histon H3 (H3K23Ac) voor KAT6A/B, een andere op H3 (H3K14Ac) voor KAT7, één op H4 (H4K16Ac) voor KAT8, en markers op het variant-histon H2A.Z voor KAT5. Deze markers zijn meetbaar met geavanceerde massaspectrometrie of met standaard antilichaamgebaseerde blots, wat ze praktisch maakt voor veel laboratoria.
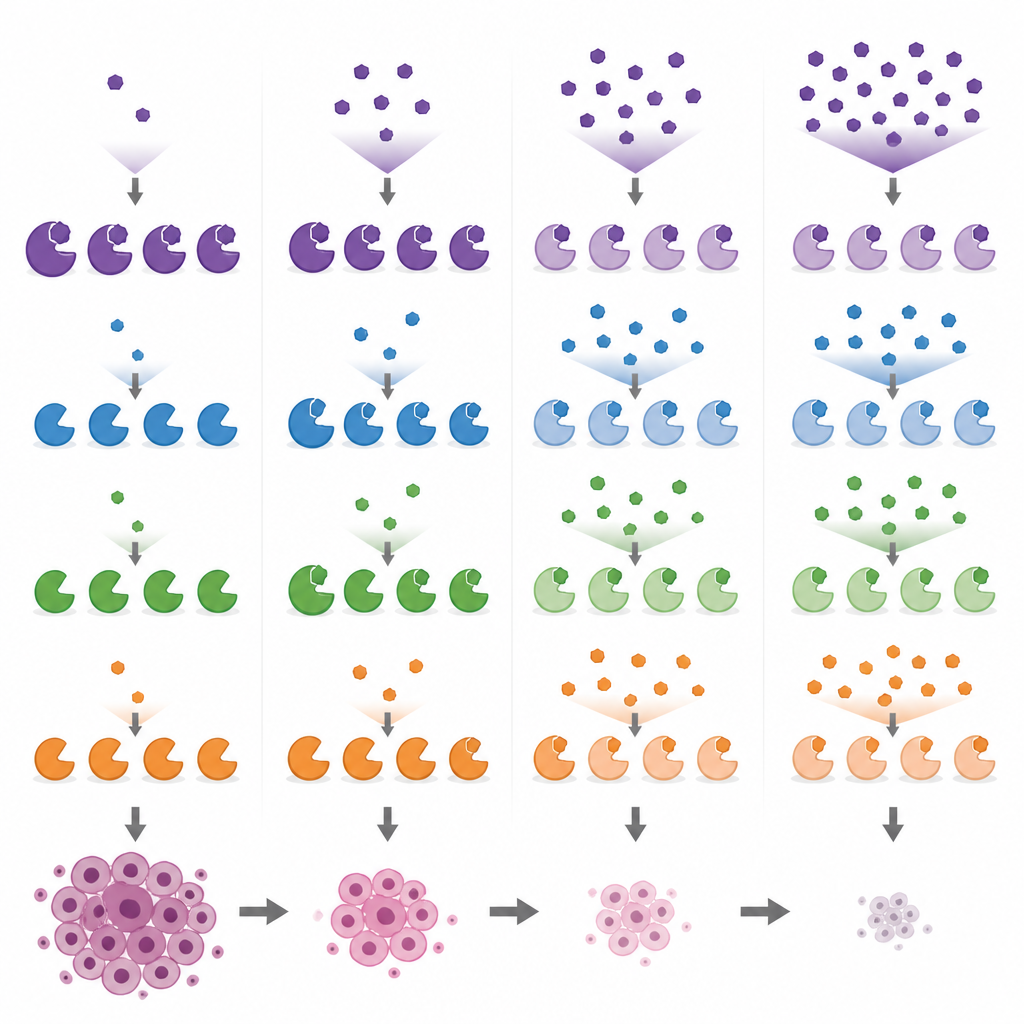
Vergelijking van veelgebruikte onderzoeksmedicijnen en hun neventargets
Met deze biomarker-readouts vergeleken de onderzoekers verschillende veelgebruikte MYST-richtende verbindingen in borstkankercellen over een reeks dosisconcentraties. Ze toonden aan dat PF-9363 en het klinische familielid PF-8144 hetzelfde stapsgewijze patroon volgen en uiteindelijk KAT8 bij hogere doses beïnvloeden. WM-1119 bleek daarentegen zeer selectief voor KAT6A/B, zelfs bij hoge concentraties, terwijl WM-8014 en WM-3835 eerst KAT6A/B remmen en pas daarna KAT7. Een verbinding, MOZ-IN-3, die in buisjesanalyses krachtig lijkt, toonde weinig effect in cellen, waarschijnlijk omdat ze de cellen slecht binnendringt. Deze vergelijkingen laten zien dat sommige hulpmiddelen die als specifiek voor één enzym op de markt worden gebracht, in werkelijkheid meerdere enzymen raken, wat de interpretatie van eerdere en toekomstige experimenten kan bemoeilijken.
Dosering, enzymbetrokkenheid en kankercelgroei koppelen
Het team vroeg zich vervolgens af of dit gelaagde remmingspatroon de reactie van kankercellen bepaalt. Het screenen van PF-9363 over het NCI-60-paneel van kankercellijnen liet zien dat korte blootstellingen aan doses die alleen KAT6A/B en KAT7 blokkeren een bescheiden effect op groei hebben. Sterke, snelle groeivertragingen traden meestal pas op bij hogere doses waarbij ook KAT8, een enzym essentieel voor de meeste cellen, werd betrokken. In een triple-negatieve borstkankelijn die sterk afhankelijk is van KAT8, kwam de dosis die het aantal cellen deed krimpen overeen met de dosis die het KAT8-gekoppelde histonmerk volledig onderdrukte, terwijl ook KAT6A/B en KAT7 werden geblokkeerd. Dit suggereert dat bij sommige tumoren hogere doses van deze middelen kunnen werken via bredere MYST-remming in plaats van alleen via KAT6A/B.
Wat dit betekent voor toekomstige kankergeneesmiddelen
Samengevat toont de studie aan dat kleine-molecuulblokkers van MYST-enzymen zich gedragen zoals veel kinaseremmers: bij lage doses raken ze vooral hun voorkeursdoelen, maar naarmate de dosis stijgt verspreken ze zich naar nauw verwante enzymen in een voorspelbare volgorde. Door eenvoudige histon-gebaseerde meetpunten voor elk MYST-lid aan te reiken en te onthullen waar populaire verbindingen echt selectief zijn, biedt het werk onderzoekers en clinici een hulpmiddelenkist om dosis af te stemmen op gewenste enzymdekking. Dit zal helpen bij het ontwerpen van duidelijkere laboratoriumstudies, het interpreteren van klinische proeven en uiteindelijk bij het ontwikkelen van preciezere therapieën die genregulatie in kankercellen hervormen terwijl ongewenste bijwerkingen worden beperkt.
Bronvermelding: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Trefwoorden: epigenetische enzymen, histonacetylatie, targeting van kankergeneesmiddelen, chemoproteomics, lysine-acetyltransferaseremmers