Clear Sky Science · es
Inhibición jerárquica por pequeñas moléculas de las acetiltransferasas MYST
Por qué importan los interruptores diminutos en el ADN para el tratamiento del cáncer
Dentro de cada célula, interruptores químicos sobre nuestro ADN ayudan a decidir qué genes se activan o se silencian. Un grupo de enzimas llamadas acetiltransferasas MYST ajusta finamente esos interruptores y se ha relacionado con cánceres como el de mama y la leucemia. Este estudio explora cómo nuevas moléculas farmacológicas pueden modular estas enzimas de forma controlada y escalonada, ofreciendo pistas para diseñar tratamientos contra el cáncer más precisos y para interpretar ensayos clínicos en curso.
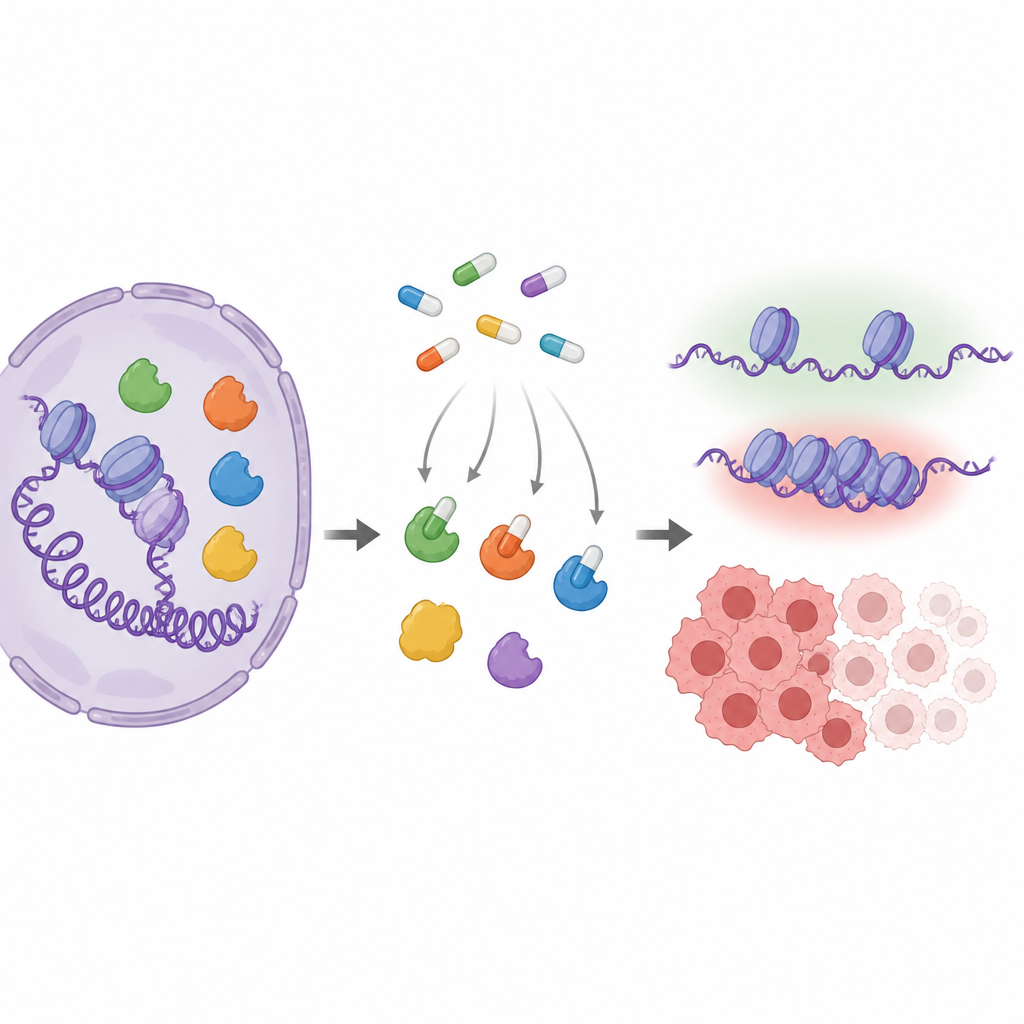
Actores clave que regulan la actividad génica
Las enzimas MYST alteran sutilmente cómo se empaqueta el ADN añadiendo pequeñas etiquetas químicas a las proteínas llamadas histonas. Ese empaquetamiento ayuda a decidir si los genes implicados en crecimiento, reparación o respuesta hormonal están activos. Varios miembros de esta familia, especialmente KAT6A y KAT6B, están alterados o sobreexpresados en cánceres, lo que los convierte en objetivos terapéuticos atractivos. Las compañías farmacéuticas han desarrollado compuestos tipo pastilla que encajan en el sitio activo de estas enzimas, pero como las distintas MYST son muy parecidas en ese sitio, resulta difícil saber exactamente cuáles ataca cada fármaco dentro de células reales.
Medir qué enzimas afecta realmente cada fármaco
Los autores diseñaron una estrategia de ensayos por capas para mapear cómo un fármaco líder, PF-9363, y compuestos relacionados interactúan con las enzimas MYST. Primero usaron una molécula “cebo” acoplada a perlas magnéticas que captura enzimas mediante el mismo hueco donde usan su combustible natural. Si un fármaco bloquea ese hueco, la enzima deja de unirse al cebo. Al añadir dosis crecientes del fármaco a extractos nucleares de células y luego medir por espectrometría de masas qué proteínas seguían unidas al cebo, hallaron una jerarquía clara: PF-9363 desplaza primero a KAT6A y KAT6B, luego a KAT7, después a KAT8 y solo a niveles más altos a KAT5. El mismo patrón aparece para el fármaco clínico PF-8144, ahora en ensayos contra cáncer de mama receptor de estrógeno positivo.
Encontrar socios ocultos y lecturas celulares claras
Puesto que bloquear el hueco enzimático también debilita la unión de ensamblajes proteicos enteros que se sientan sobre el cebo, el equipo pudo ver qué otras proteínas viajan junto con cada enzima MYST. Al agrupar las proteínas que se perdían del cebo con el mismo patrón de dosis que miembros conocidos de complejos, y combinar esto con predicción de estructura 3D y experimentos en células, identificaron al factor de transcripción FOXK2 como un socio previamente no reconocido, vinculado sobre todo al complejo NSL que contiene KAT8. A continuación pasaron a células cancerosas vivas y examinaron cientos de marcas químicas en histonas mientras aumentaban la dosis de PF-9363. Identificaron un pequeño conjunto de marcas de acetilación que informan de forma fiable qué enzima MYST ha sido bloqueada: una marca en la histona H3 (H3K23Ac) para KAT6A/B, otra en H3 (H3K14Ac) para KAT7, una en H4 (H4K16Ac) para KAT8 y marcas en la histona variante H2A.Z para KAT5. Estas marcas se pueden medir por espectrometría de masas avanzada o por técnicas estándar basadas en anticuerpos, lo que las hace prácticas para muchos laboratorios.
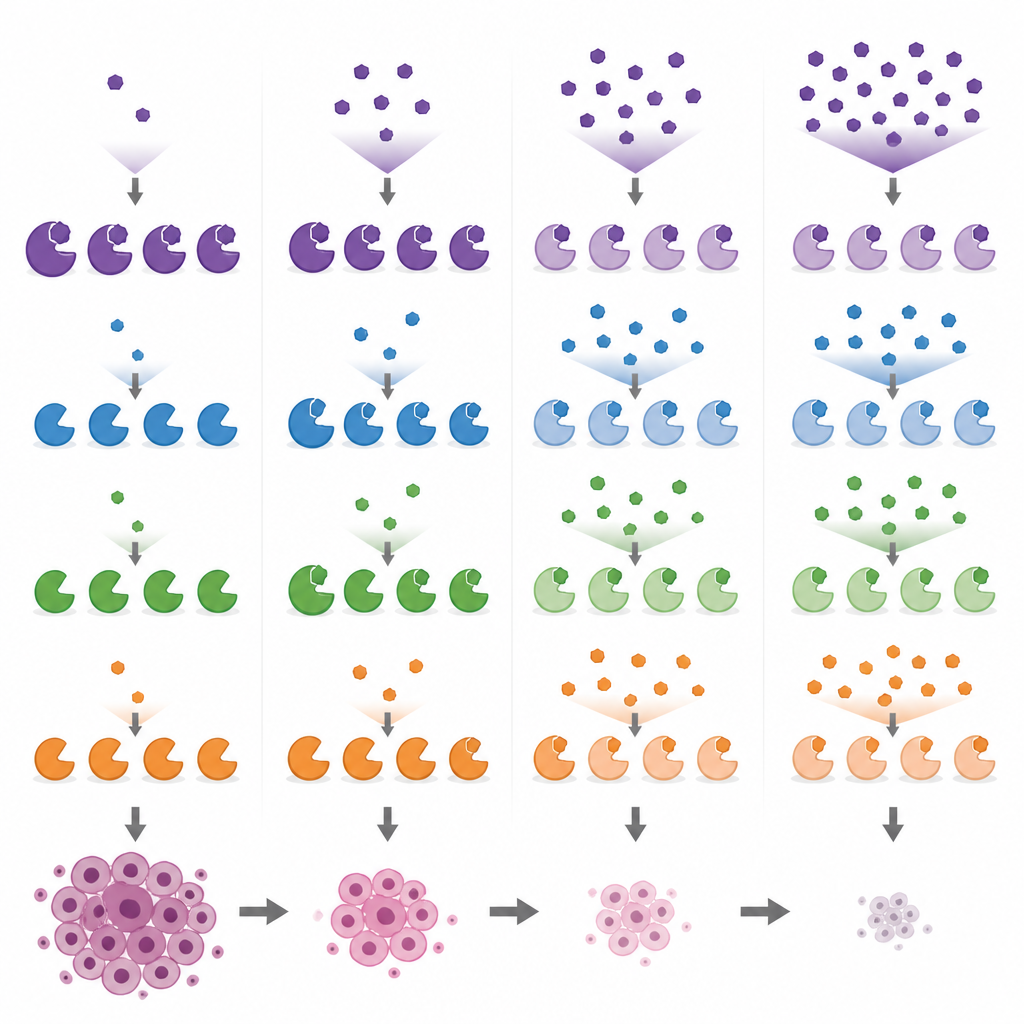
Comparando fármacos de uso habitual en la investigación y sus objetivos secundarios
Con estos marcadores, los investigadores compararon varios compuestos ampliamente usados que se dirigen a MYST en células de cáncer de mama a lo largo de un rango de dosis. Mostraron que PF-9363 y su pariente clínico PF-8144 siguen el mismo patrón escalonado, afectando finalmente a KAT8 a dosis más altas. En contraste, WM-1119 resultó ser muy selectivo para KAT6A/B incluso a concentraciones elevadas, mientras que WM-8014 y WM-3835 inhiben primero KAT6A/B y solo después KAT7. Un compuesto, MOZ-IN-3, que parece potente en ensayos in vitro mostró poco efecto en células, probablemente porque no entra bien en ellas. Estas comparaciones revelan que algunas herramientas comercializadas como específicas de una enzima en realidad atacan varias, lo que puede complicar la interpretación de experimentos pasados y futuros.
Vinculando dosis, compromiso enzimático y crecimiento de células cancerosas
El equipo preguntó entonces si este patrón de inhibición por capas moldea la respuesta de las células cancerosas. El cribado de PF-9363 en el panel NCI-60 de líneas celulares mostró que exposiciones breves a dosis que bloquean solo KAT6A/B y KAT7 tienen efectos modestos sobre el crecimiento. Las ralentizaciones fuertes y rápidas del crecimiento aparecieron típicamente solo a dosis más altas donde también se comprometía KAT8, una enzima esencial para la mayoría de las células. En una línea de cáncer de mama triple negativo que depende especialmente de KAT8, la dosis que redujo el número de células coincidió con la dosis que suprimió completamente la marca histona vinculada a KAT8 mientras bloqueaba también KAT6A/B y KAT7. Esto sugiere que, para algunos tumores, dosis más altas de estos fármacos pueden actuar mediante una inhibición más amplia de MYST en lugar de por KAT6A/B solamente.
Qué significa esto para futuros fármacos contra el cáncer
En conjunto, el estudio muestra que los bloqueadores de pequeñas moléculas de las enzimas MYST se comportan de forma parecida a muchos fármacos dirigidos a quinasas: a dosis bajas atacan principalmente sus objetivos preferidos, pero al aumentar la dosis se extienden a enzimas estrechamente relacionadas en un orden predecible. Al proporcionar lecturas simples basadas en histonas para cada miembro de MYST y revelar dónde son realmente selectivos los compuestos populares, el trabajo ofrece a investigadores y clínicos un conjunto de herramientas para ajustar la dosis al alcance enzimático deseado. Esto debería ayudar a diseñar estudios de laboratorio más claros, a interpretar resultados de ensayos clínicos y, en última instancia, a guiar el desarrollo de terapias más precisas que reconfiguren el control génico en células tumorales limitando los efectos secundarios no deseados.
Cita: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Palabras clave: enzimas epigenéticas, acetilación de histonas, dirección de fármacos contra el cáncer, quimoproteómica, inhibidores de acetiltransferasas de lisina