Clear Sky Science · pl
Hierarchiczne hamowanie małocząsteczkowe acetylotransferaz MYST
Dlaczego drobne przełączniki na DNA mają znaczenie w leczeniu raka
W każdej komórce chemiczne przełączniki na naszym DNA pomagają decydować, które geny są włączane lub wyłączane. Grupa enzymów zwanych acetylotransferazami MYST precyzyjnie reguluje te przełączniki i powiązana jest z nowotworami, takimi jak rak piersi i białaczka. W badaniu tym analizuje się, jak nowe molekuły leków mogą kontrolowanie wyciszać lub zmniejszać aktywność tych enzymów w sposób stopniowy, co daje wskazówki do projektowania bardziej precyzyjnych terapii przeciwnowotworowych oraz do interpretacji trwających badań klinicznych.
Główni aktorzy regulujący aktywność genów
Enzymy MYST subtelnie zmieniają sposób pakowania DNA poprzez dodawanie małych grup chemicznych do białek zwanych histonami. To pakowanie wpływa na to, czy geny związane z wzrostem, naprawą czy odpowiedzią hormonalną są aktywne. Kilku członków tej rodziny, zwłaszcza KAT6A i KAT6B, jest zmienionych lub nadmiernie produkowanych w nowotworach, co czyni je atrakcyjnymi celami terapeutycznymi. Firmy farmaceutyczne opracowały związki w formie cząsteczek, które wpasowują się w czynne miejsce tych enzymów, ale ponieważ różne enzymy MYST mają bardzo podobne miejsce aktywne, trudno jest ustalić, które z nich dany lek uderza w rzeczywistych komórkach.
Pomiary, które enzymy rzeczywiście trafia dany lek
Autorzy opracowali wielowarstwową strategię testową, aby odwzorować, jak wiodący lek PF-9363 i powiązane związki wchodzą w interakcje z enzymami MYST. Najpierw użyli „przynęty” — cząsteczki przymocowanej do magnetycznych kulek, która wychwytuje enzymy przez to samo miejsce, w którym korzystają z naturalnego substratu. Jeśli lek blokuje to miejsce, enzym nie przylega już do przynęty. Dodając rosnące dawki leku do ekstraktów jądrowych z komórek i mierząc następnie metodą spektrometrii mas, które białka nadal wiązały przynętę, odkryli wyraźną hierarchię: PF-9363 najpierw wypiera KAT6A i KAT6B, potem KAT7, potem KAT8, a dopiero przy najwyższych stężeniach — KAT5. Ten sam wzorzec obserwowano dla leku klinicznego PF-8144, obecnie w badaniach nad rakiem piersi z dodatnim receptorem estrogenowym.
Odnajdywanie ukrytych partnerów i jasnych odczytów komórkowych
Ponieważ blokowanie kieszeni enzymatycznej osłabia także przyczepność całych zespołów białkowych, które siedzą na przynęcie, zespół mógł zobaczyć, które inne białka współwędrują z każdym enzymem MYST. Grupując białka, które znikały z przynęty przy tym samym wzorcu dawki co znani członkowie kompleksu, a następnie łącząc to z predykcją struktury 3D i eksperymentami w komórkach, wskazali czynnik transkrypcyjny FOXK2 jako wcześniej nierozpoznanego partnera, szczególnie powiązanego z kompleksem NSL zawierającym KAT8. Następnie przeszli do żywych komórek nowotworowych i zbadali setki modyfikacji chemicznych na histonach przy stopniowo rosnącej dawce PF-9363. Wyodrębnili niewielki zestaw znaków acetylacji, które wiarygodnie informują, który enzym MYST został zablokowany: jeden znak na histonie H3 (H3K23Ac) dla KAT6A/B, inny na H3 (H3K14Ac) dla KAT7, jeden na H4 (H4K16Ac) dla KAT8 oraz modyfikacje na wariancie histonu H2A.Z dla KAT5. Te markery można mierzyć zarówno za pomocą zaawansowanej spektrometrii mas, jak i standardowych testów z przeciwciałami, co czyni je praktycznymi dla wielu laboratoriów.
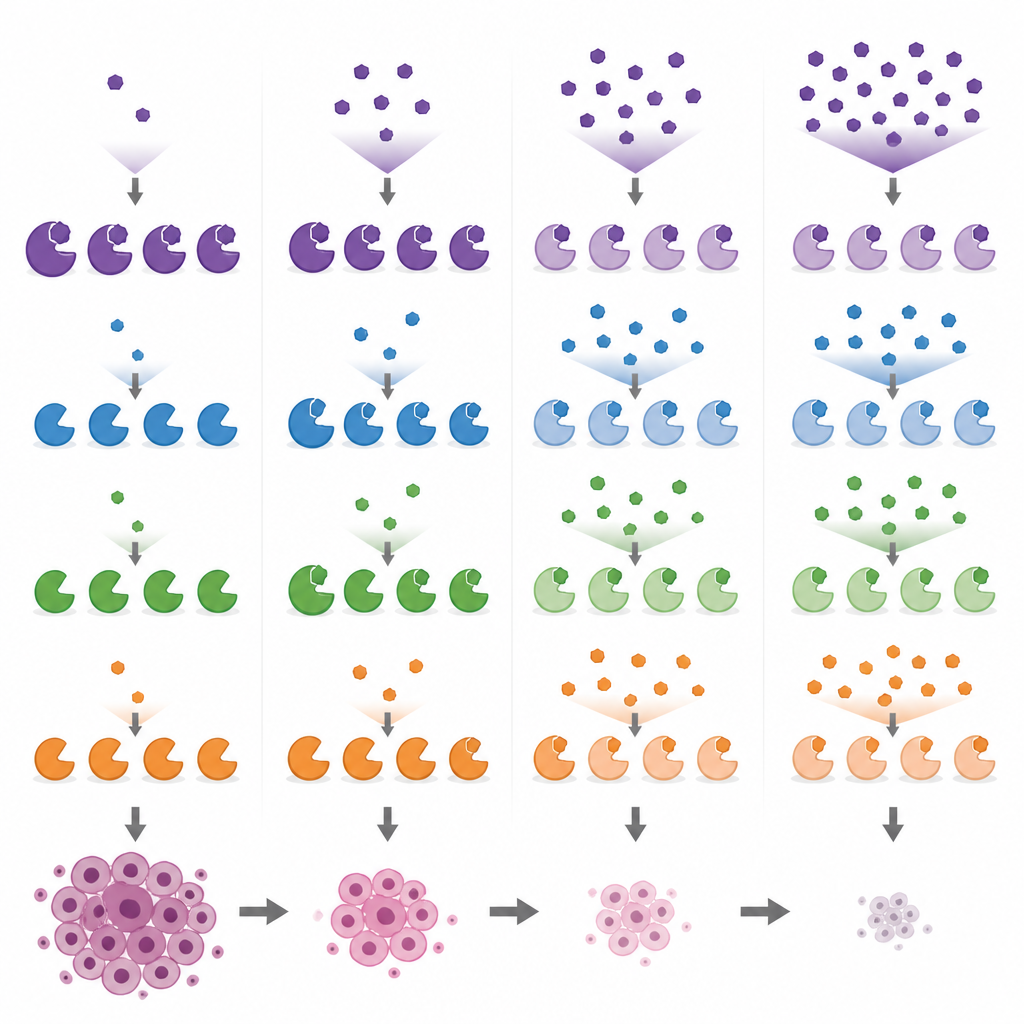
Porównanie popularnych narzędzi badawczych i ich celów ubocznych
Wykorzystując te odczyty biomarkerów, badacze porównali kilka powszechnie stosowanych związków skierowanych przeciw MYST w komórkach raka piersi przy różnych dawkach. Pokazali, że PF-9363 i jego kliniczny odpowiednik PF-8144 wykazują ten sam krokowy wzorzec, ostatecznie wpływając na KAT8 przy wyższych dawkach. Dla odmiany WM-1119 okazał się wysoce selektywny wobec KAT6A/B nawet przy wysokich stężeniach, podczas gdy WM-8014 i WM-3835 najpierw hamują KAT6A/B, a dopiero potem KAT7. Jeden z związków, MOZ-IN-3, który wydaje się silny w testach probówkowych, wykazywał niewielki efekt w komórkach, prawdopodobnie dlatego, że słabo do nich wchodzi. Te porównania pokazują, że niektóre narzędzia reklamowane jako specyficzne dla jednego enzymu w rzeczywistości oddziałują na kilka, co może komplikować interpretację wcześniejszych i przyszłych eksperymentów.
Łączenie dawki, zaangażowania enzymu i wzrostu komórek nowotworowych
Zespół zapytał następnie, czy ten wielowarstwowy wzorzec hamowania kształtuje reakcję komórek nowotworowych. Przesiew PF-9363 w panelu linii komórkowych NCI-60 wykazał, że krótkie ekspozycje na dawki blokujące tylko KAT6A/B i KAT7 mają umiarkowany wpływ na wzrost. Silne, szybkie spowolnienie wzrostu pojawiało się przeważnie dopiero przy wyższych dawkach, gdy zaangażowany był również KAT8 — enzym niezbędny dla większości komórek. W linii raka piersi potrójnie negatywnej, która szczególnie zależy od KAT8, dawka zmniejszająca liczbę komórek odpowiadała dawce całkowicie tłumiącej powiązany z KAT8 znacznik histonowy przy jednoczesnym zablokowaniu KAT6A/B i KAT7. Sugeruje to, że w niektórych guzach wyższe dawki tych leków mogą działać poprzez szersze zahamowanie MYST, a nie wyłącznie przez KAT6A/B.
Co to oznacza dla przyszłych leków przeciwnowotworowych
Podsumowując, badanie pokazuje, że małocząsteczkowe inhibitory enzymów MYST zachowują się podobnie do wielu leków kinazowych: przy niskich dawkach trafiają głównie swoje preferowane cele, ale wraz ze wzrostem dawki rozszerzają zakres działania na blisko spokrewnione enzymy w przewidywalnym porządku. Dostarczając proste histonowe odczyty dla każdego członka rodziny MYST i ujawniając, gdzie popularne związki naprawdę są selektywne, praca daje badaczom i klinicystom zestaw narzędzi do dopasowania dawki do pożądanego zakresu blokady enzymów. Powinno to pomóc w projektowaniu bardziej klarownych badań laboratoryjnych, interpretacji wyników badań klinicznych i ostatecznie prowadzić do rozwoju dokładniejszych terapii, które przekształcają kontrolę genów w komórkach nowotworowych, ograniczając jednocześnie niepożądane skutki uboczne.
Cytowanie: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Słowa kluczowe: enzymy epigenetyczne, acetylacja histonów, celowanie leków przeciwnowotworowych, chemoproteomika, inhibitory acetylotransferaz lizynowych