Clear Sky Science · ru
Иерархическое маломолекулярное ингибирование ацетилтрансфераз MYST
Почему крошечные переключатели на ДНК важны для лечения рака
Внутри каждой клетки химические переключатели на нашей ДНК помогают решать, какие гены включаются или выключаются. Группа ферментов, называемых ацетилтрансферазами MYST, тонко регулирует эти переключатели и связана с такими онкологическими заболеваниями, как рак молочной железы и лейкемия. В этом исследовании изучают, как новые лекарственные молекулы могут управляемо, пошагово снижать активность этих ферментов, что дает подсказки для разработки более точных противораковых терапий и для интерпретации текущих клинических испытаний.
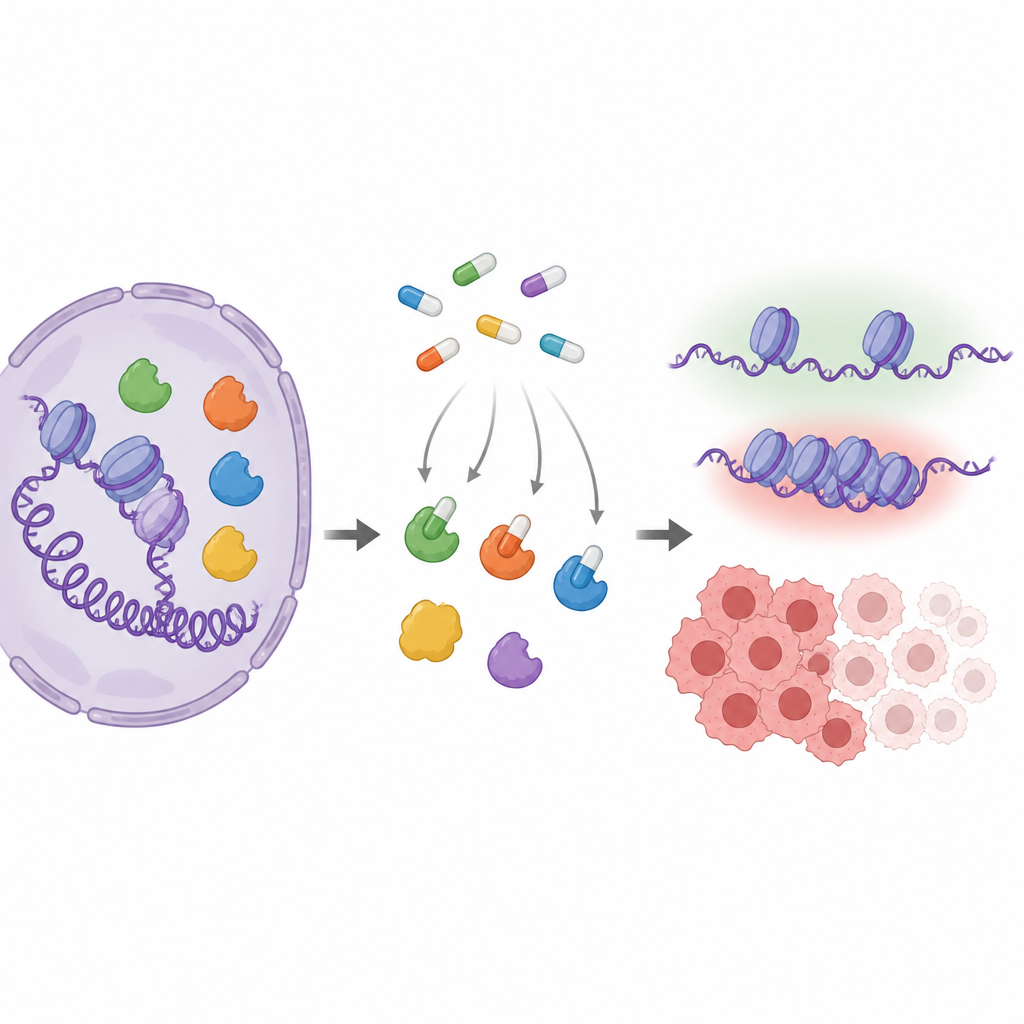
Ключевые участники, регулирующие активность генов
Ферменты MYST тонко изменяют упаковку ДНК, добавляя небольшие химические метки к белкам, называемым гистонами. Такая упаковка помогает определять, активны ли гены, связанные с ростом, восстановлением или гормональным ответом. Несколько членов этого семейства, особенно KAT6A и KAT6B, изменены или перепроизводятся при раке, что делает их привлекательными мишенями для лекарств. Фармацевтические компании создали таблеткоподобные соединения, которые подходят в рабочее «карманное» место этих ферментов, но поскольку разные ферменты MYST имеют очень похожую структуру в этой области, внутри реальных клеток трудно точно определить, какие именно ферменты каждый препарат поражает.
Измерение того, какие ферменты действительно поражает каждое лекарство
Авторы разработали многослойную стратегию тестирования, чтобы отобразить, как ведущий препарат PF-9363 и родственные соединения взаимодействуют с ферментами MYST. Сначала они использовали «наживку» — молекулу, прикрепленную к магнитным бусинам, которая захватывает ферменты, используя тот же карман, что и их природный субстрат. Если препарат блокирует этот карман, фермент больше не прилипает к наживке. Добавляя нарастающие дозы препарата к ядерным экстрактам клеток и затем измеряя масс-спектрометрией, какие белки всё ещё связаны с наживкой, они обнаружили очевидную иерархию: PF-9363 сначала вытесняет KAT6A и KAT6B, затем KAT7, затем KAT8, и только при самых высоких уровнях — KAT5. Та же последовательность наблюдается и для клинического препарата PF-8144, который сейчас проходит испытания при раке молочной железы с положительной экспрессией рецептора эстрогена.
Поиск скрытых партнёров и явных клеточных показателей
Поскольку блокировка ферментного кармана также ослабляет связность целых белковых комплексов, сидящих на наживке, команда смогла увидеть, какие другие белки перемещаются вместе с каждым ферментом MYST. Кластеризуя белки, исчезающие с наживки с той же дозовой динамикой, что и известные члены комплексов, а затем сочетая это с предсказанием 3D-структур и клеточными экспериментами, они выделили транскрипционный фактор FOXK2 как ранее нераспознанного партнёра, особенно связанного с комплексом NSL, содержащим KAT8. Далее они перешли к живым раковым клеткам и исследовали сотни химических меток на гистонах при повышении дозы PF-9363. Они выделили небольшой набор ацетилирований, которые надежно указывают, какой MYST-фермент был заблокирован: метка на гистоне H3 (H3K23Ac) для KAT6A/B, другая на H3 (H3K14Ac) для KAT7, метка на H4 (H4K16Ac) для KAT8 и метки на вариантном гистоне H2A.Z для KAT5. Эти метки можно измерять либо с помощью продвинутой масс‑спектрометрии, либо стандартными антительно-обусловленными вестерн‑блотами, что делает их практичными для многих лабораторий.
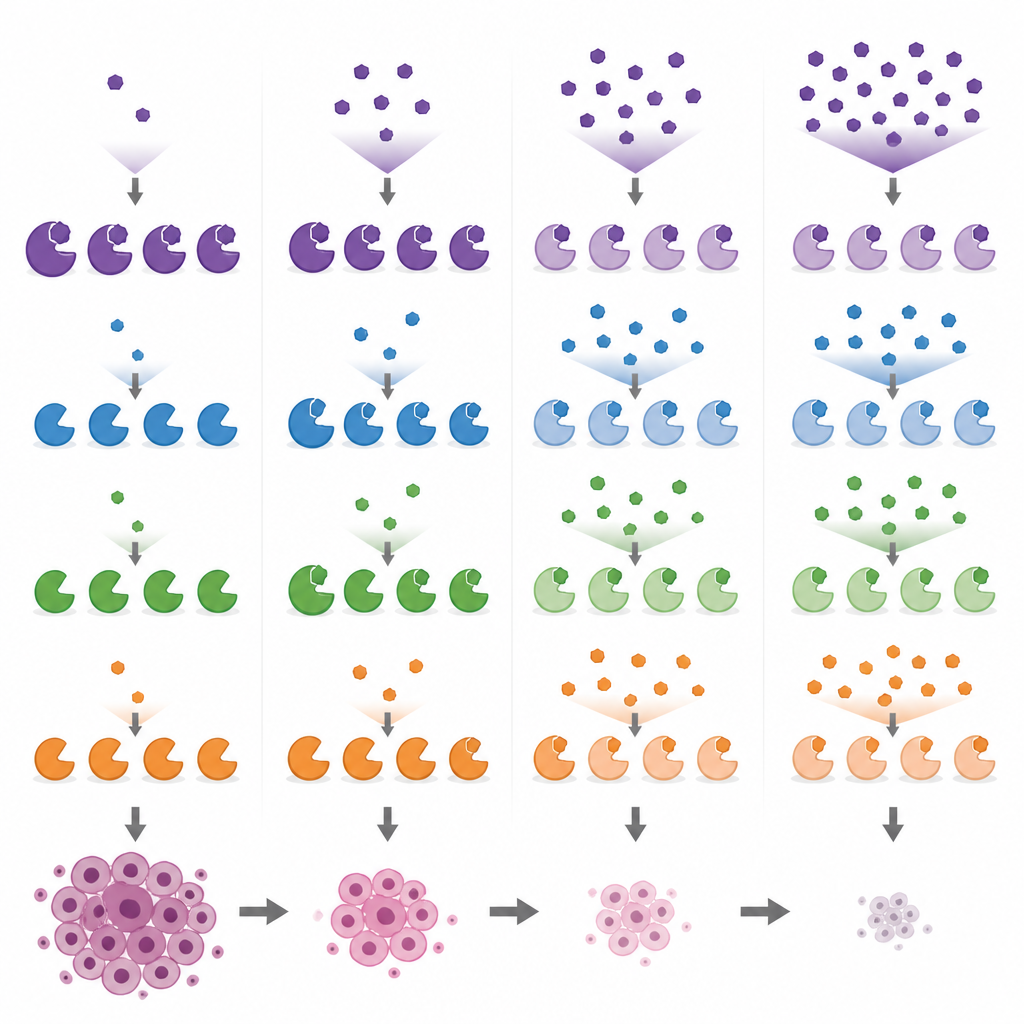
Сравнение популярных исследовательских препаратов и их побочных мишеней
Вооружившись этими биомаркерными индикаторами, исследователи сравнили несколько широко используемых соединений, нацеленных на MYST, в клетках рака молочной железы при разных дозах. Они показали, что PF-9363 и его клинический родственник PF-8144 следуют той же пошаговой схеме, в конечном счёте затрагивая KAT8 при более высоких дозах. Напротив, WM-1119 оказался высокоселективным для KAT6A/B даже при больших концентрациях, тогда как WM-8014 и WM-3835 сначала ингибируют KAT6A/B и лишь затем KAT7. Одно соединение, MOZ-IN-3, которое выглядит мощным в пробирочных тестах, почти не проявило эффекта в клетках, вероятно, потому что плохо проникает в них. Эти сравнения показывают, что некоторые инструменты, рекламируемые как специфичные для одного фермента, на самом деле поражают несколько, что может осложнять интерпретацию прошлых и будущих экспериментов.
Связь дозы, вовлечения фермента и роста раковых клеток
Затем команда спросила, формирует ли эта многоступенчатая схема ингибирования ответ раковых клеток. Скрининг PF-9363 на панели клеточных линий NCI-60 показал, что короткие экспозиции доз, блокирующих только KAT6A/B и KAT7, оказывают умеренное влияние на рост. Сильные и быстрые замедления роста обычно появлялись только при более высоких дозах, когда также вовлекался KAT8 — фермент, жизненно важный для большинства клеток. В линии тройного негативного рака молочной железы, которая особенно зависит от KAT8, доза, уменьшавшая число клеток, соответствовала дозе, полностью подавлявшей гистоновую метку, связанную с KAT8, одновременно блокируя KAT6A/B и KAT7. Это указывает на то, что для некоторых опухолей более высокие дозы этих препаратов могут действовать через более широкое ингибирование MYST, а не только через KAT6A/B.
Что это значит для будущих противораковых препаратов
В целом, исследование показывает, что маломолекулярные блокаторы ферментов MYST ведут себя схоже со многими ингибиторами киназ: при низких дозах они в основном поражают предпочтительные мишени, но по мере роста дозы распространяются на близкородственные ферменты в предсказуемом порядке. Предоставив простые гистоновые индикаторы для каждого члена MYST и показав, где популярные соединения действительно селективны, работа предлагает исследователям и клиницистам инструменты для подбора дозы в соответствии с желаемым покрытием ферментов. Это должно помочь проектировать более прозрачные лабораторные исследования, интерпретировать результаты клинических испытаний и в конечном счёте направлять разработку более точных методов лечения, которые перестраивают генетический контроль в раковых клетках, ограничивая побочные эффекты.
Цитирование: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Ключевые слова: эпигенетические ферменты, ацетилирование гистонов, таргетирование противораковых препаратов, хемопротеомика, ингибиторы лизиновых ацетилтрансфераз