Clear Sky Science · ar
تثبيط هرمي لجزيئات صغيرة لأنزيمات MYST ناقلة الأسيتيل
لماذا تهم مفاتيح صغيرة على الحمض النووي لعلاج السرطان
داخل كل خلية، تساعد مفاتيح كيميائية على حمضنا النووي في تقرير أي الجينات تُشغل أو تُطفأ. مجموعة من الإنزيمات تسمى ناقلات الأسيتيل MYST تضبط هذه المفاتيح بدقة وقد ارتبطت ببعض أنواع السرطان مثل سرطان الثدي واللوكيميا. تستكشف هذه الدراسة كيف يمكن لجزيئات دوائية جديدة أن ترفع أو تُخفت نشاط هذه الإنزيمات بطريقة مُتحكَّم بها وبخطوات، مما يوفر دلائل لتصميم علاجات سرطانية أكثر دقة ولتفسير التجارب السريرية الجارية.
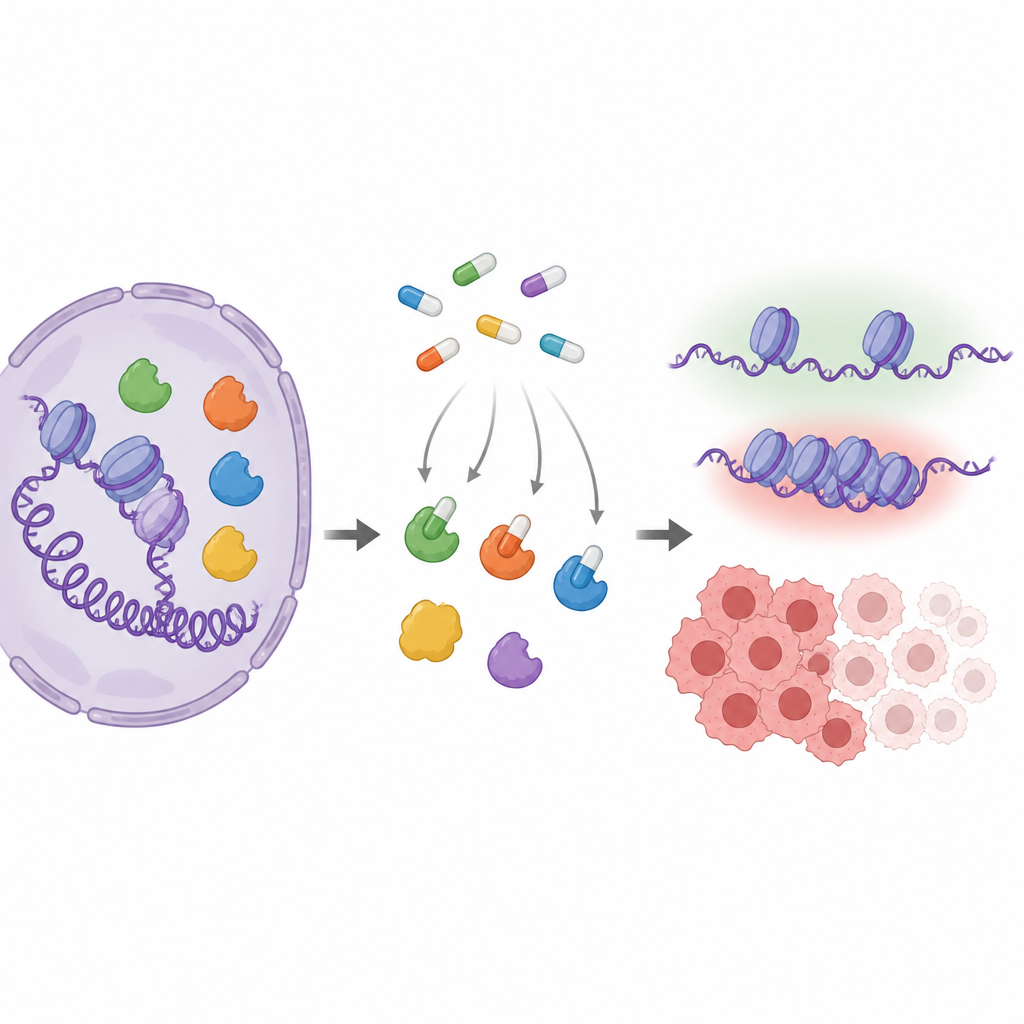
الفاعلون الرئيسيون في ضبط نشاط الجينات
تغيّر إنزيمات MYST بشكل دقيق كيفية تغليف الحمض النووي عبر إضافة علامات كيميائية صغيرة على بروتينات تُدعى الهيستونات. يساعد هذا التغليف في تقرير ما إذا كانت الجينات المشاركة في النمو أو الإصلاح أو الاستجابة الهرمونية نشطة. كثير من أعضاء هذه العائلة، وخاصة KAT6A وKAT6B، تتغير أو تُنتَج بكثرة في السرطان، مما يجعلها أهدافاً دوائية جذابة. طورت شركات الدواء مركبات شبيهة بالأقراص تتناسب مع موقع العمل في هذه الإنزيمات، لكن لأن مواقع العمل لدى إنزيمات MYST المختلفة تبدو متشابهة جداً، فصعب معرفة أيها يتأثر فعلياً داخل الخلايا الحية.
قياس أي إنزيمات تُصيبها كل دواء فعلاً
بنى المؤلفون استراتيجية اختبار طبقية لرسم خريطة كيفية تفاعل دواء رائد، PF-9363، ومركبات ذات صلة مع إنزيمات MYST. أولاً، استخدموا جزيئاً «طُعمياً» مربوطاً بحبات مغناطيسية يلتقط الإنزيمات عبر نفس الجيب الذي يستخدمونه لوقودهم الطبيعي. إذا سدَّ دواء ذلك الجيب، لا يعود الإنزيم متمسكاً بالطُعم. عبر إضافة جرعات متزايدة من الدواء إلى مستخلصات نووية من خلايا ثم قياس أي البروتينات ظلت مرتبطة بالطُعم بواسطة مطيافية الكتلة، وجدوا ترتيباً واضحاً: PF-9363 يزيح أولاً KAT6A وKAT6B، ثم KAT7، ثم KAT8، وفقط عند أعلى المستويات يؤثر على KAT5. يظهر نفس النمط في الدواء السريري PF-8144، الموجود حالياً في تجارب لسرطان الثدي الإيجابي لمستقبلات الإستروجين.
اكتشاف شركاء مخفيين ومؤشرات خلوية واضحة
لأن سدّ جيب الإنزيم يضعف أيضاً تماسك مجاميع البروتين الكاملة التي تجلس على الطُعم، تمكن الفريق من رؤية أي البروتينات تسافر مع كل إنزيم MYST. عبر تجميع البروتينات التي اختفت من الطُعم بنفس نمط الجرعة كأعضاء المجمع المعروفة، ثم دمج ذلك بتنبؤات البنية ثلاثية الأبعاد وتجارب خلوية، أشاروا إلى عامل النسخ FOXK2 كشريك لم يكن معروفاً سابقاً، مرتبطاً خصوصاً بمجمع NSL المحتوي على KAT8. بعد ذلك، انتقلوا إلى خلايا سرطانية حية وفحصوا المئات من العلامات الكيميائية على الهيستونات بينما زادوا جرعة PF-9363. حددوا مجموعة صغيرة من علامات الأسيتلة التي تبلغ بثبات عن أي إنزيم MYST قد تم قفله: علامة على الهيستون H3 (H3K23Ac) لـ KAT6A/B، وأخرى على H3 (H3K14Ac) لـ KAT7، وواحدة على H4 (H4K16Ac) لـ KAT8، وعلامات على الهيستون المتغير H2A.Z لـ KAT5. يمكن قياس هذه العلامات إما بمطيافية الكتلة المتقدمة أو بواسطة اللطخات التقليدية المعتمدة على الأجسام المضادة، مما يجعلها عملية للعديد من المختبرات.
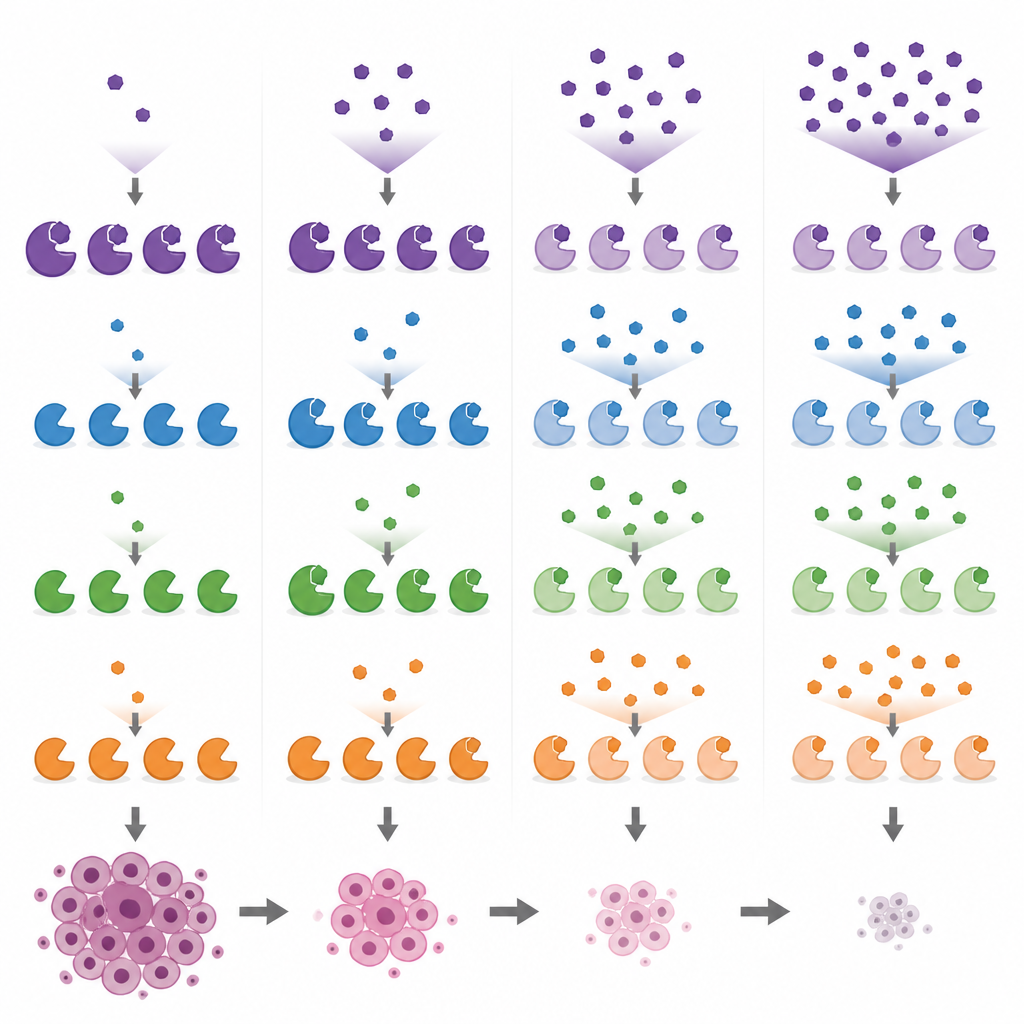
مقارنة أدوية البحث الشائعة وأهدافها الجانبية
مسلحين بهذه مؤشرات العلامات الحيوية، قارن الباحثون عدة مركبات مستخدمة على نطاق واسع والمستهدفة لـ MYST في خلايا سرطان الثدي عبر نطاق من الجرعات. أظهروا أن PF-9363 وابن عمّه السريري PF-8144 يتبعان كلاهما نفس النمط المرحلي، ويؤثران في النهاية على KAT8 عند الجرعات الأعلى. بالمقابل، تبين أن WM-1119 انتقائي للغاية لـ KAT6A/B حتى عند تركيزات عالية، بينما يثبط WM-8014 وWM-3835 KAT6A/B أولاً ثم KAT7 فقط بعد ذلك. أحد المركبات، MOZ-IN-3، الذي يبدو قوياً في تجارب الأنبوب، أظهر تأثيراً ضئيلاً في الخلايا، على الأرجح لأنه لا يدخلها جيداً. تكشف هذه المقارنات أن بعض الأدوات المسوقة على أنها محددة لانزيم واحد تضرب فعلياً عدة إنزيمات، وهو ما قد يعقّد تفسير التجارب الماضية والمستقبلية.
ربط الجرعة وتفاعل الإنزيم ونمو الخلايا السرطانية
ثم تساءل الفريق عما إذا كان هذا النمط الطبقي من التثبيط يشكل استجابة الخلايا السرطانية. أظهر اختبار PF-9363 عبر لوحة NCI-60 من خطوط الخلايا السرطانية أن التعرضات القصيرة للجرعات التي تسد KAT6A/B وKAT7 فقط لها آثار متواضعة على النمو. عادةً ظهرت تباطؤات قوية وسريعة في النمو فقط عند الجرعات الأعلى التي تُشرك أيضاً KAT8، إنزيم ضروري لمعظم الخلايا. في خط سرطان الثدي الثلاثي السلبي الذي يعتمد بشكل خاص على KAT8، طابقت الجرعة التي قلّصت أعداد الخلايا الجرعة التي قمعَت بالكامل علامة الهيستون المرتبطة بـ KAT8 بينما كانت قد عطّلت أيضاً KAT6A/B وKAT7. هذا يشير إلى أنه لبعض الأورام، قد تعمل جرعات أعلى من هذه الأدوية عبر تثبيط أوسع لعائلة MYST بدلاً من العمل عبر KAT6A/B فقط.
ما معنى هذا لأدوية السرطان المستقبلية
بصفة عامة، تُظهر الدراسة أن مانعات الجزيئات الصغيرة لإنزيمات MYST تتصرف مثل العديد من أدوية الكيناز: عند الجرعات المنخفضة تضرب أهدافها المفضلة بشكل رئيسي، لكن مع ارتفاع الجرعة تمتد لتشمل إنزيمات قريبة مرتبطَة بترتيب قابل للتنبؤ. من خلال توفير قراءات بسيطة مستندة إلى الهيستون لكل عضو من MYST وكشف أين تكون المركبات الشائعة منتقاة فعلاً، يقدم العمل لمختبرات البحث والأطباء السريريين مجموعة أدوات لمطابقة الجرعة بتغطية الإنزيم المطلوبة. ينبغي أن يساعد ذلك في تصميم دراسات مخبرية أوضح، وتفسير نتائج التجارب السريرية، وبالنهاية توجيه تطوير علاجات أكثر دقة تعيد تشكيل ضبط الجينات في الخلايا السرطانية مع الحد من الآثار الجانبية غير المرغوبة.
الاستشهاد: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
الكلمات المفتاحية: إنزيمات فوق جينية, أسيتلة الهيستون, استهداف أدوية السرطان, كيموبروتيوميكيات, مثبطات ناقلات أسيتيل الليزين