Clear Sky Science · tr
Canlı hücre etiketlemesiyle mümkün kılınan tek hücre tioyl profillemesi, ferroptoziste metabolik heterojenliği ortaya koyuyor
Neden küçük hücresel kimyasallar önemli?
Vücudumuzdaki her hücre, kimyasının düzgün işlemesi için tiyoller adı verilen küçük kükürt içeren molekül ailesine bağımlıdır. Bu moleküller enerji kullanımını kontrol etmeye, reaktif oksijenin neden olduğu hasardan korumaya ve bir hücrenin yaşayıp yaşamayacağına karar vermeye yardım eder. Ancak tiyoller hassas ve çok az miktarda bulunduğu için araştırmacılar aynı anda birçok farklı tiyolü tek hücre düzeyinde ölçmekte zorlandı. Bu çalışma, bireysel canlı hücrelerin içindeki tiyolleri 'dondurup' okunabilir hale getiren bir yöntem tanıtıyor ve bununla bazı kanser hücrelerinin ferroptozis adı verilen bir hücre ölümü türüne neden yenildiğini bazılarının ise direnç gösterdiğini ortaya koyuyor.
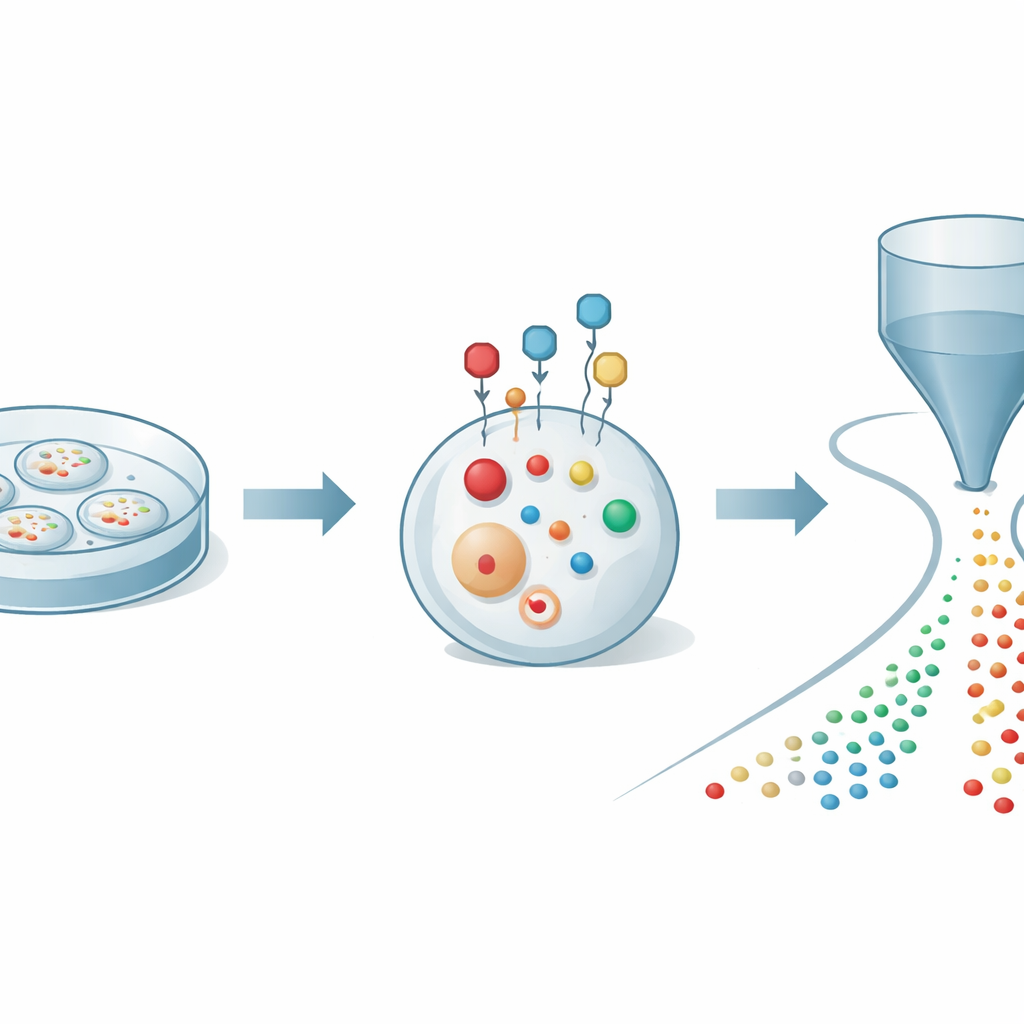
Kırılgan hücresel yardımcıları yerinde kilitlemek
Yazarlar önce temel bir sorunu ele aldı: tiyoller hücreler parçalandığında hızla okside olur ve değişir; bu da içeride gerçekten olup bitenin çarpıtılmış bir görünümünü verebilir. Hücre zarından geçebilen ve canlı hücrelerde tiyollerle hızlı ve seçici olarak reaksiyona giren küçük bir kimyasal problar tasarladılar. Prob bağlandığında hem koruyucu bir kafes hem de bir yükseltici gibi davranır: tiyolleri oksidasyona karşı stabilize eder ve onlar için bir elektriksel yük ekleyerek kütle spektrometrisi ile tespit edilmelerini çok daha kolay hale getirir. Probun yapısını dikkatle ayarlayarak ekip, hücreleri sağlıklı tutarken tiyolleri dakikalar içinde etiketleyen koşulları buldu ve böylece tiyol kimyasının gerçek zamanlı güvenilir bir anlık görüntüsünü yakalayabildi.
Tek hücreden yüzlerce molekül okumak
Bu etiketlemeyi kullanmak için araştırmacılar onu organik kütle sitometrisi olarak bilinen gelişmiş bir tespit platformuna bağladılar. Bu düzenekte binlerce etiketlenmiş hücre nazikçe tek tek ince bir kapilardan bir iyonizasyon kaynağına ve yüksek çözünürlüklü bir kütle spektrometresine doğru itilir. Her hücre geçerken küçük molekülleri çıkarılır ve iyonlara dönüştürülür, bu da o hücreye özgü kısa bir sinyal darbesi oluşturur. Hesaplamalı araçlar daha sonra hangi darbenin hangi hücreye ait olduğunu belirler ve her olaya yüzlerce moleküler pik atar. Bu entegre stratejiyle yazarlar, tek bir kanser hücresinde 27 farklı etiketlenmiş tiyolü ve 300’den fazla diğer metaboliti nicelendirerek tek hücre çözünürlüğünde zengin bir kükürt ve enerji metabolizması haritası ortaya koyabildiler.
Stresin kükürt ağları boyunca nasıl yayıldığını izlemek
Grup daha sonra bu yaklaşımın tiyol yolları kasıtlı olarak bozulduğunda hücrelerin nasıl yanıt verdiğini izleyip izleyemeyeceğini sordu. Hücreleri oksidatif hasardan koruyan ana tiyollerden biri olan glutatyon (GSH) sentezinin farklı adımlarını seçici olarak engelleyen ilaçlar kullandılar. Tek hücrelerde, kesin ve yol‑tutarlı değişimler gözlemlediler: sistin girişinin engellenmesi sistein ve birçok aşağı akış kükürt metabolitini tüketti; bireysel glutatyon yapım enzimlerinin engellenmesi ise üst akış bileşenlerinin birikmesine ve GSH düzeylerinin düşmesine neden oldu. Tiyollerin ötesinde, yüzlerce diğer metabolit de enerji ve redoks dengesindeki daha geniş değişimleri yansıtan karakteristik desenlerde değişti. Bu deneyler, yöntemin hücrenin birbirine bağlı kükürt ağı boyunca yayılan ince, lokal değişiklikleri takip edebildiğini gösterdi.
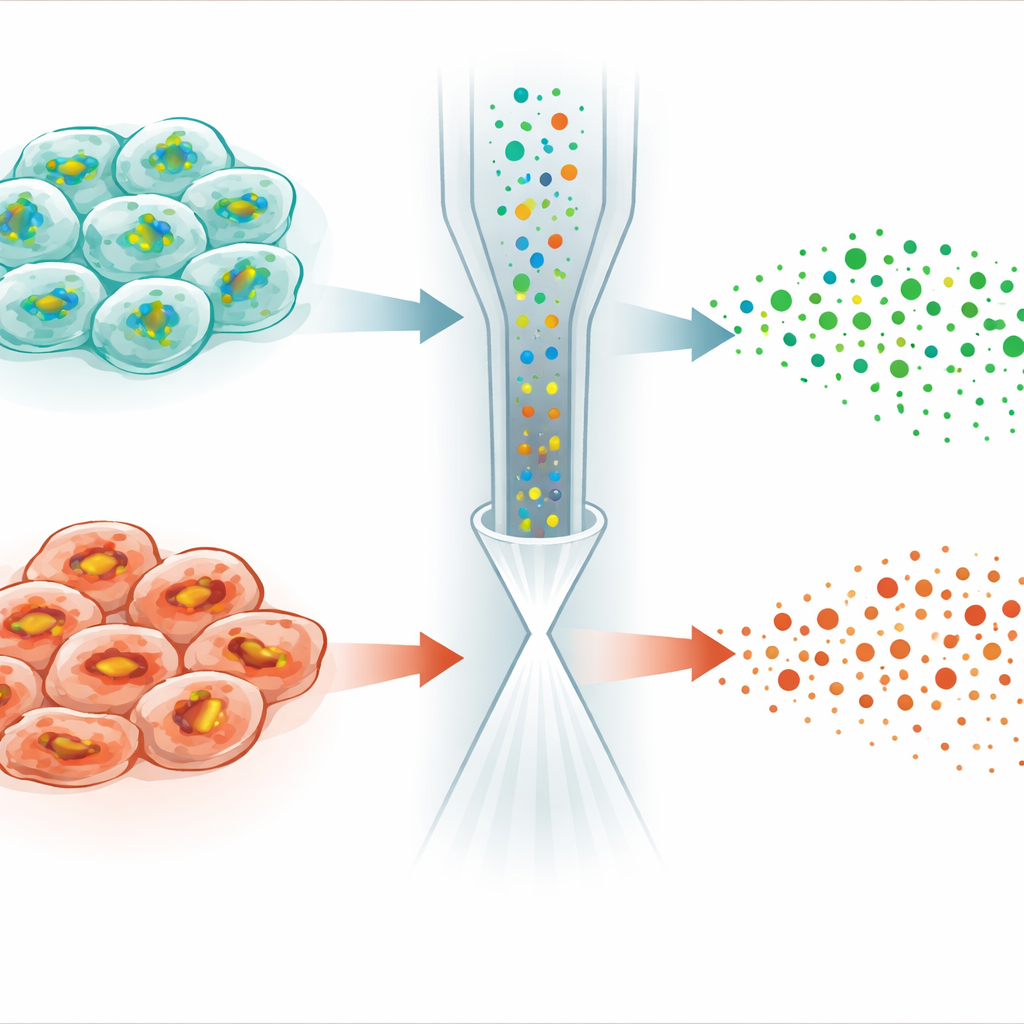
Hücre ölümü hassasiyetinde gizli farkları ortaya çıkarmak
En çarpıcı uygulama ferroptozisi incelemekten geldi; ferroptozis, demire bağımlı membran hasarı tarafından tetiklenen düzenlenmiş bir hücre ölümü biçimidir. RSL3 adlı küçük bir molekül, normalde GSH kullanarak lipit peroksitlerini detoksifiye eden bir enzimi devre dışı bırakarak kanser hücrelerini öldürür. İlginç bir şekilde, yazarlar HeLa kanser hücrelerini RSL3 ile muamele ettiğinde GSH düzeyleri, tüketimi bloke edildiğinde beklenebileceği gibi sadece sabitlenmedi ya da artmadı; birçok hücrede düştü. Tek hücre analizi, popülasyonun iki alt tipe ayrıldığını ortaya koydu: biri neredeyse normal GSH ve lipid profillerini korurken, diğeri belirgin şekilde azalmış GSH, zayıflamış GSH üretimi ve peroksidasyona yatkın lipid moleküllerinde belirgin değişiklikler gösterdi. Ek deneyler bu farkları, sistin girişini ve GSH sentezini ve geri dönüşümünü kontrol eden genlerin ifadesini yöneten bir stres‑yanıt düzenleyicisi olan NRF2’nin farklı düzeyleriyle ilişkilendirdi.
Gelecek terapiler için bunun anlamı
Bir arada ele alındığında çalışma, canlı hücre tiyol etiketlemesini organik kütle sitometrisiyle birleştirmenin çok sayıda kırılgan tiyolü ve daha geniş metabolizmayı bireysel hücrelerde stabilize edip ölçebileceğini gösteriyor. Bu güçlü ölçüm, RSL3’ün sadece GSH kullanımını engellemekle kalmayıp aynı zamanda NRF2–glutatyon ekseni aracılığıyla GSH üretimini de baskıladığını ortaya koydu; bu da aynı tümör hattı içinde ferroptozise dirençli ve ferroptozise duyarlı ayrı alt popülasyonlar yaratıyor. Bilim dışı okuyucu için ana mesaj şudur: mikroskop altında aynı görünen hücreler, glutatyon gibi koruyucu kimyasalları nasıl yönettikleri konusunda derin farklılıklar gösterebilir ve bu farklar bir kanser tedavisinin işe yarayıp yaramayacağını belirleyebilir. Bu yeni yöntem, bu gizli metabolik varyasyonları hücre hücre görebilmeyi mümkün kılarak, hassas hücreleri ölüme itecek, sağlıklı veya dirençli hücreleri koruyacak daha hassas stratejiler tasarlamaya yardımcı olabilir.
Atıf: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Anahtar kelimeler: tek hücre metabolomisi, glutatyon, ferroptozis, redoks metabolizması, kanser hücresi heterojenliği