Clear Sky Science · de
Einzelzell‑Thiolprofilierung mittels Lebendzell‑Markierung zeigt metabolische Heterogenität bei Ferroptose
Warum winzige Zellchemikalien wichtig sind
Jede Zelle in unserem Körper ist auf eine Familie kleiner schwefelhaltiger Moleküle, sogenannte Thiole, angewiesen, damit ihre Chemie reibungslos funktioniert. Diese Moleküle steuern den Energiehaushalt, schützen vor Schäden durch reaktive Sauerstoffspezies und entscheiden darüber, ob eine Zelle überlebt oder abstirbt. Da Thiole jedoch labil sind und nur in winzigen Mengen vorkommen, fiel es Forschern lange schwer, viele verschiedene Thiole gleichzeitig in Einzelzellen zu messen. Diese Studie stellt eine Methode vor, um Thiole in lebenden Einzelzellen zu fixieren und auszulesen, und verwendet sie, um zu erklären, warum einige Krebszellen einer Form des Zelltods namens Ferroptose erliegen, während andere resistent bleiben.
Fragile Zellhelfer an Ort und Stelle fixieren
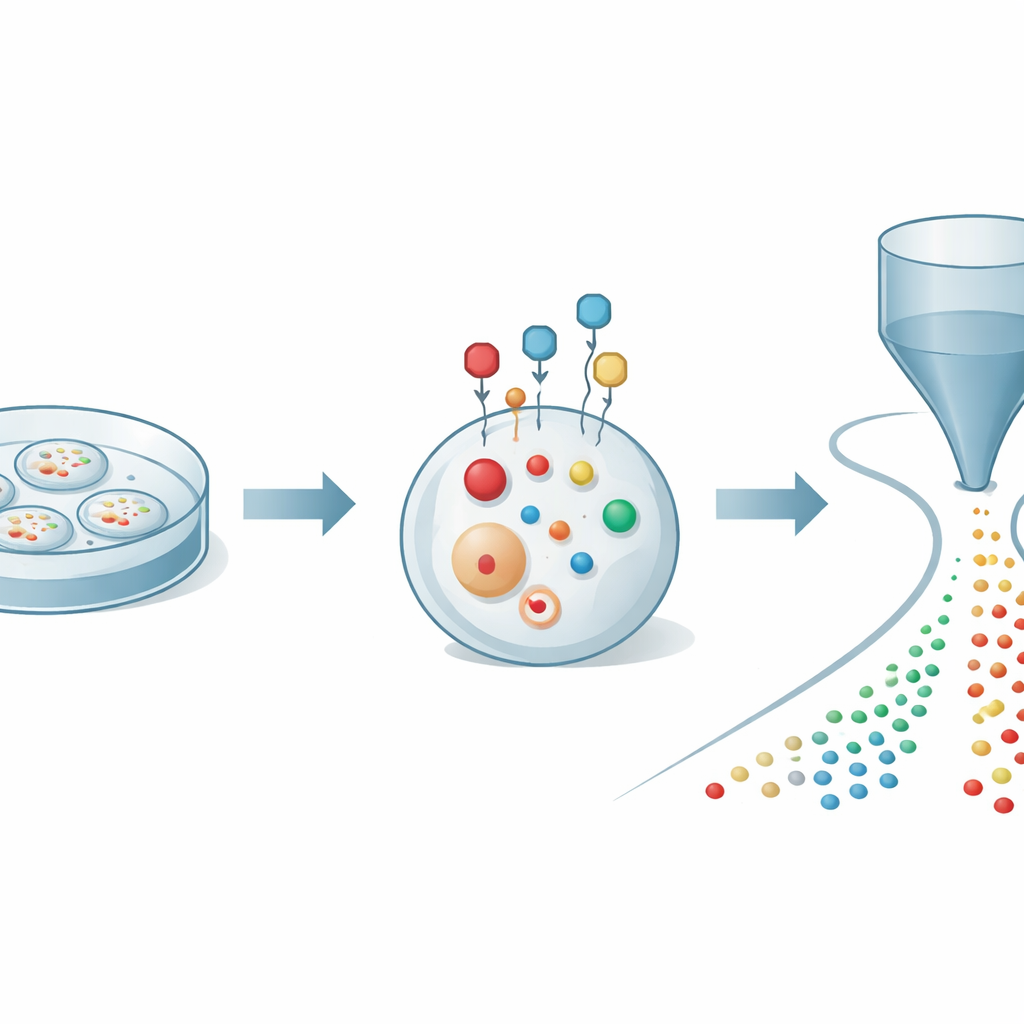
Die Autoren begannen mit einem grundlegenden Problem: Thiole oxidieren schnell und verändern sich, wenn Zellen zur Analyse geöffnet werden, was ein verzerrtes Bild dessen liefern kann, was tatsächlich in der Zelle vor sich geht. Sie entwickelten eine kleine chemische Sonde, die durch die Zellmembran diffundiert und in lebenden Zellen schnell und selektiv mit Thiolen reagiert. Einmal gebunden wirkt die Sonde wie ein Schutzkäfig und zugleich wie ein Verstärker: Sie stabilisiert die Thiole gegenüber Oxidation und verleiht ihnen eine elektrische Ladung, die ihre Erfassung per Massenspektrometrie erheblich erleichtert. Durch sorgfältige Anpassung der Sondenstruktur fanden die Forschenden Bedingungen, unter denen Thiole innerhalb weniger Minuten markiert werden können, ohne die Zellen zu schädigen, sodass sich ein zuverlässiger Schnappschuss der Thiolchemie in Echtzeit einfangen lässt.
Hunderte Moleküle aus Einzelzellen auslesen
Um diese Markierung nutzbar zu machen, kombinierten die Forschenden sie mit einer fortschrittlichen Detektionsplattform, der organischen Massenzytometrie. In diesem Aufbau werden Tausende markierter Zellen einzeln und schonend durch eine dünne Kapillare in eine Ionisationsquelle eines hochauflösenden Massenspektrometers geleitet. Während jede Zelle vorbeipasst, werden ihre kleinen Moleküle extrahiert und in Ionen umgewandelt, wodurch ein kurzer Signalschub entsteht, der für diese Zelle charakteristisch ist. Rechnerische Werkzeuge ordnen diese Pulse den einzelnen Zellen zu und weisen jedem Ereignis Hunderte molekularer Peaks zu. Mit dieser integrierten Strategie konnten die Autoren 27 verschiedene markierte Thiole sowie mehr als 300 weitere Metaboliten in einzelnen Krebszellen quantifizieren und so eine detaillierte Karte des Schwefel‑ und Energiestoffwechsels auf Einzelzellniveau erstellen.
Beobachtung, wie Stress durch Schwefelnetzwerke wandert
Als Nächstes untersuchte das Team, ob sich mit diesem Ansatz verfolgen lässt, wie Zellen reagieren, wenn Thiolpfade gezielt gestört werden. Sie setzten Wirkstoffe ein, die selektiv verschiedene Schritte der Glutathionsynthese (GSH) blockieren — ein zentrales Thiol, das Zellen vor oxidativen Schäden schützt. In Einzelzellen beobachteten sie präzise und wegekonforme Verschiebungen: Blockiert man den Cystinimport, kam es zu einem Mangel an Cystein und vielen nachgeschalteten Schwefelmetaboliten; blockiert man einzelne glutat ionsaufbauende Enzyme, häuften sich vorgeschaltete Komponenten, während die GSH‑Spiegel sanken. Neben den Thiolen veränderten sich Hunderte anderer Metaboliten in charakteristischen Mustern, was breitere Verschiebungen in Energie‑ und Redoxgleichgewicht widerspiegelt. Diese Experimente zeigten, dass die Methode subtile, lokal begrenzte Änderungen verfolgen kann, während sie sich durch das vernetzte Schwefelnetz der Zelle ausbreiten.
Verborgene Unterschiede in der Empfindlichkeit gegenüber Zelltod aufdecken
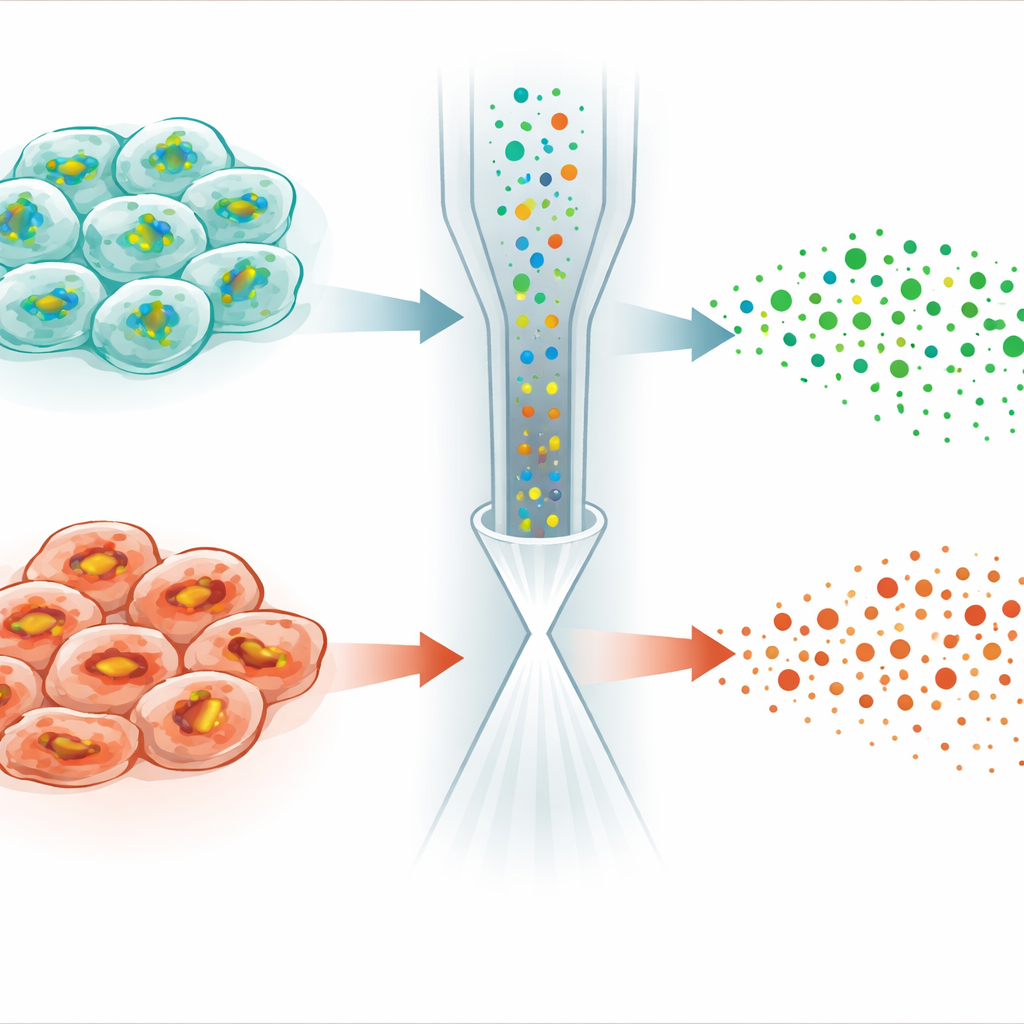
Die eindrücklichste Anwendung ergab sich aus der Untersuchung der Ferroptose, einer regulierten Form des Zelltods, die durch eisenabhängige Schäden an Zellmembranen ausgelöst wird. Ein kleines Molekül namens RSL3 tötet Krebszellen, indem es ein Enzym ausschaltet, das normalerweise GSH nutzt, um Lipidperoxide zu entgiften. Überraschenderweise fielen bei Behandlung von HeLa‑Krebszellen mit RSL3 die GSH‑Werte in vielen Zellen nicht einfach stabil oder erhöht aus — wie man erwarten könnte, wenn der Verbrauch blockiert ist — sondern sanken. Die Einzelzellanalyse zeigte, dass sich die Population in zwei Subtypen aufspaltet: Der eine behielt annähernd normale GSH‑ und Lipidprofile bei, während der andere stark vermindertes GSH, geschwächte GSH‑Produktion und ausgeprägte Veränderungen an lipophilen Molekülen zeigte, die anfällig für Peroxidation sind. Weitere Experimente verbanden diese Unterschiede mit variierenden Spiegeln eines Stressantwortregulators namens NRF2, der die Expression von Genen steuert, die Cystin importieren sowie GSH synthetisieren und recyceln.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Studie, dass die Kombination aus Lebendzell‑Thiolmarkierung und organischer Massenzytometrie viele labile Thiole zusammen mit dem weiteren Metabolismus in Einzelzellen stabilisieren und messen kann. Dieser leistungsfähige Nachweis legte offen, dass RSL3 mehr bewirkt als nur die Nutzung von GSH zu blockieren: Es unterdrückt zusätzlich die GSH‑Produktion über die NRF2–Glutathion‑Achse und schafft so innerhalb derselben Tumorzelllinie unterschiedliche Subpopulationen von Ferroptose‑resistenten und ferroptose‑sensiblen Zellen. Für eine allgemeine Leserschaft ist die Kernbotschaft, dass Zellen, die unter dem Mikroskop identisch aussehen, sich grundlegend darin unterscheiden können, wie sie schützende Stoffe wie Glutathion handhaben — und dass diese Unterschiede darüber entscheiden können, ob eine Krebstherapie wirkt. Indem die neue Methode solche verborgenen metabolischen Variationen eine Zelle nach der anderen sichtbar macht, kann sie helfen, präzisere Strategien zu entwickeln, um verwundbare Zellen gezielt zum Tod zu bringen und gleichzeitig gesunde oder resistente Zellen zu schonen.
Zitation: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Schlüsselwörter: Einzelzell‑Metabolomik, Glutathion, Ferroptose, Redoxstoffwechsel, Heterogenität von Krebszellen