Clear Sky Science · ar
تتبع الثيول على مستوى خلية مفردة باستخدام وسم الخلايا الحية يكشف تغايرية استقلابية في الفيروبتوز
لماذا تهم الجزيئات الصغيرة داخل الخلايا
تعتمد كل خلية في أجسامنا على عائلة من الجزيئات الصغيرة المحتوية على الكبريت، المسماة الثيولات، للحفاظ على سير كيميائها بشكل سليم. تساعد هذه الجزيئات في تنظيم استخدام الطاقة، والحماية من الضرر الناتج عن الأكسجين التفاعلي، وتقرير ما إذا كانت الخلية ستبقى حية أم تموت. ومع ذلك، ولأن الثيولات هشة وتوجد بكميات ضئيلة، فقد واجه الباحثون صعوبة في قياس العديد من الثيولات المختلفة في خلية مفردة دفعة واحدة. تقدم هذه الدراسة طريقة لتجميد وقراءة الثيولات داخل خلايا حية مفردة، وتستخدمها لكشف سبب استسلام بعض خلايا السرطان لشكل من أشكال الموت الخلوي يُدعى الفيروبتوز بينما تقاومها خلايا أخرى.
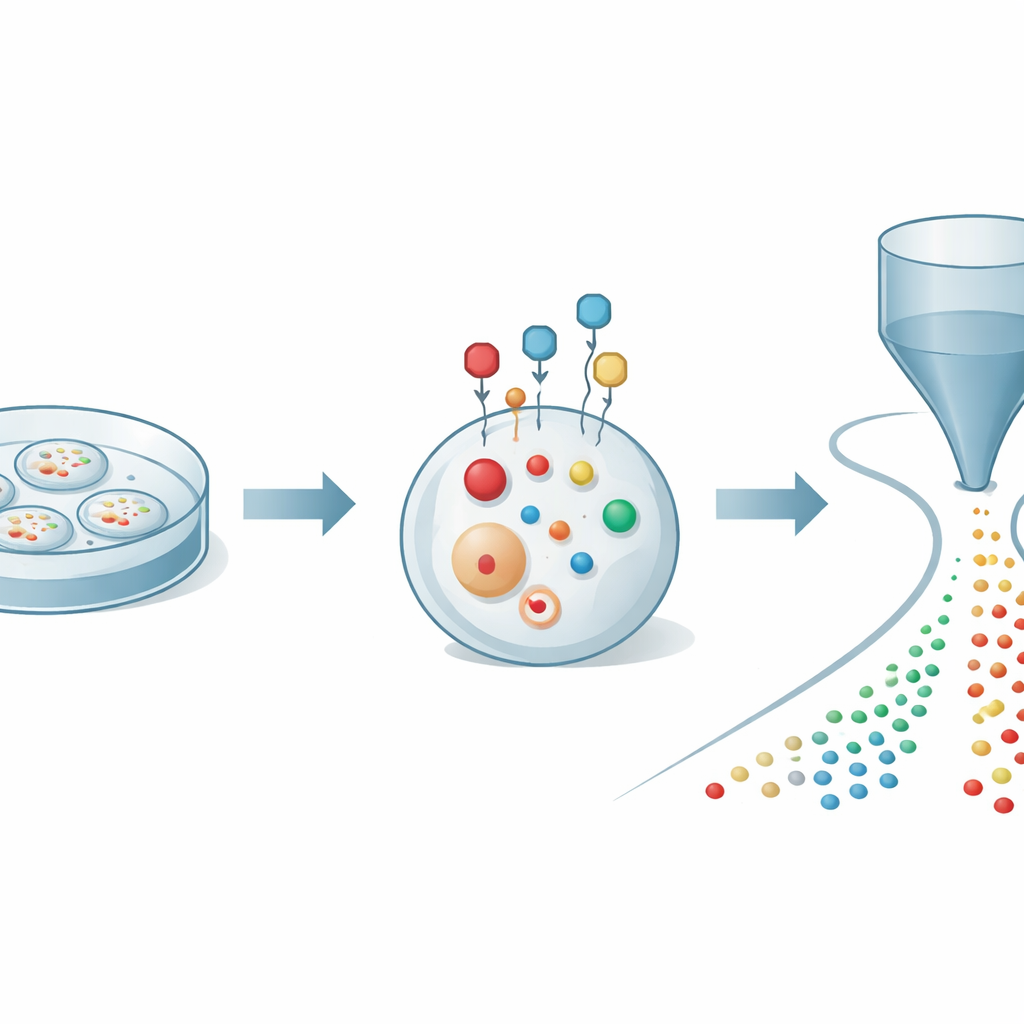
تثبيت المساعدين الخلويين الهشين في مكانهم
بدأ المؤلفون بحل مشكلة أساسية: الثيولات تتأكسد وتتغير بسرعة عندما تُفتح الخلايا للتحليل، ما قد يعطي صورة مشوهة عما يحدث بالفعل بداخلها. صمموا مسبارًا كيميائيًا صغيرًا قادرًا على عبور غشاء الخلية والتفاعل بسرعة وبانتقائية مع الثيولات داخل الخلايا الحية. بعد ارتباطه، يعمل المسبار كقفص وقائي ومضخّم: يثبّت الثيولات ضد الأكسدة ويضيف شحنة كهربائية تجعل اكتشافها بواسطة مطيافية الكتلة أسهل بكثير. من خلال ضبط هيكل المسبار بعناية، وجد الفريق ظروفًا تؤدي إلى وسم الثيولات خلال دقائق مع الحفاظ على صحة الخلايا، مما سمح لهم بالتقاط لقطة موثوقة لكيمياء الثيول في الزمن الحقيقي.
قراءة مئات الجزيئات من خلية مفردة
لاستغلال هذا الوسم، ربط الباحثون الطريقة بمنصة كشف متقدمة تُعرف باسم مطيافية الكتلة العضوية (organic mass cytometry). في هذا الإعداد، تُدفع آلاف الخلايا الموصّمة بلطف واحدة تلو الأخرى عبر شعيرة رفيعة إلى مصدر تأيين متصل بمطياف كتلة عالي الدقة. أثناء مرور كل خلية، تُستخرج جزيئاتها الصغيرة وتُحوَّل إلى أيونات، مكونة نبضة قصيرة من الإشارات الفريدة لتلك الخلية. تحدد الأدوات الحاسوبية أي نبضة تنتمي إلى أي خلية وتخصص مئات القمم الجزيئية لكل حدث. بهذه الاستراتيجية المتكاملة، استطاع المؤلفون قياس 27 ثيولاً موسومًا مميزًا إلى جانب أكثر من 300 مستقلب آخر في خلايا سرطان مفردة، كاشفين خريطة غنية لاستقلاب الكبريت والطاقة على دقة خلية مفردة.
مراقبة كيف ينتشر الإجهاد عبر شبكات الكبريت
سأل الفريق بعد ذلك ما إذا كانت هذه المقاربة تستطيع تتبع استجابة الخلايا عند تعطيل مسارات الثيول عمدًا. استخدموا أدوية تحجب خطوات مختلفة من تركيب الجلوتاثيون (GSH)، وهو ثيول رئيسي يحمي الخلايا من الضرر التأكسدي. في خلايا مفردة، رصدوا تحولات دقيقة ومتسقة مع المسارات: حجب دخول السيستين أدى إلى استنفاد السيستئين والعديد من المستقلبات الكبريتية اللاحقة؛ وإيقاف إنزيمات بناء الجلوتاثيون الفردية تسبب بتراكم المكونات المتقدمة بينما انخفضت مستويات GSH. إلى جانب الثيولات، تغيرت أيضًا مئات المستقلبات الأخرى بأنماط مميزة، معبرة عن تحولات أوسع في توازن الطاقة والأكسدة-الاختزال. أظهرت هذه التجارب أن الطريقة قادرة على متابعة تغيّرات دقيقة ومحلية أثناء انتشارها عبر شبكة الكبريت المترابطة داخل الخلية.
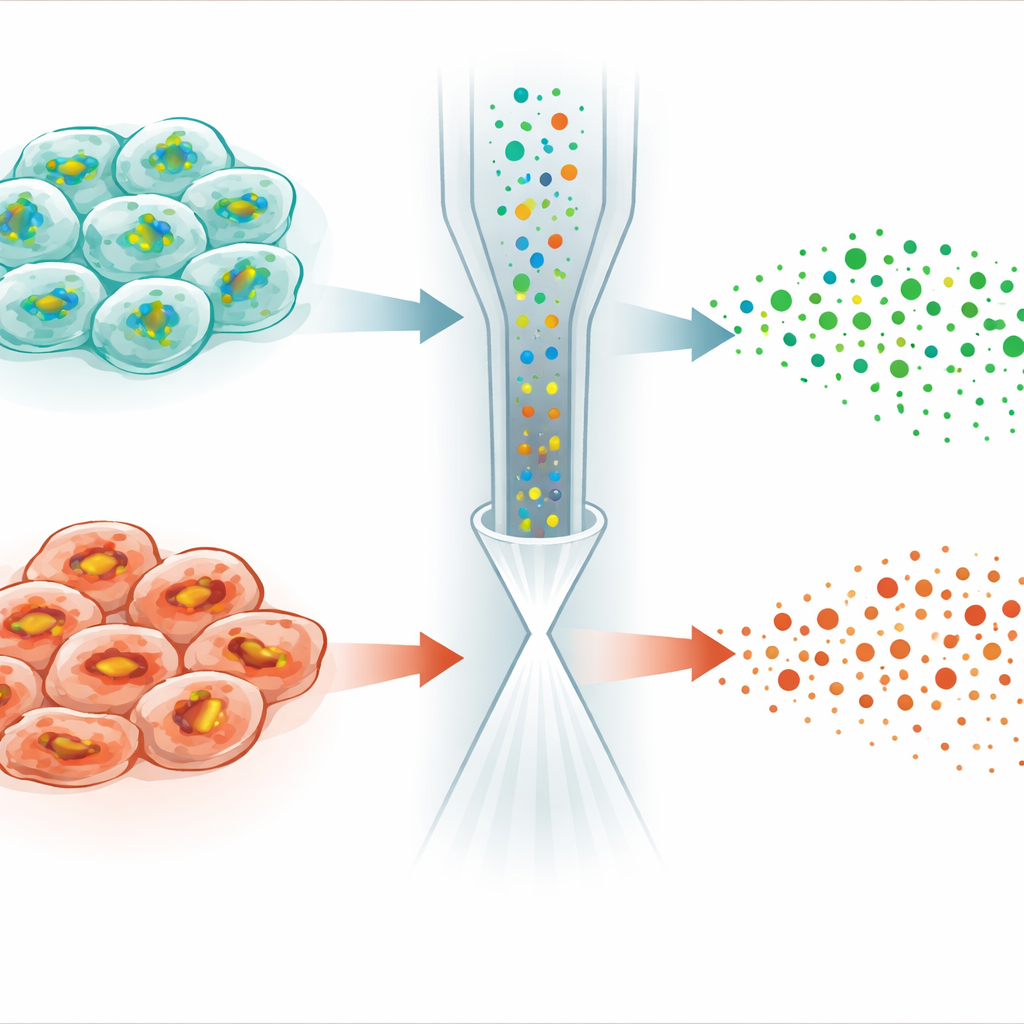
كشف اختلافات خفية في حساسية الموت الخلوي
أتى التطبيق الأكثر لفتًا للانتباه من دراسة الفيروبتوز، وهو شكل من الموت الخلوي المنظم الناتج عن ضرر معتمد على الحديد لأغشية الخلايا. جزيء صغير يُدعى RSL3 يقتل خلايا السرطان عن طريق تعطيل إنزيم يستخدم GSH عادة لإزالة سمية البيروكسيدات الدهنية. من المفاجئ، عندما عالج المؤلفون خلايا هِيلا السرطانية بـRSL3، لم تستقر مستويات GSH أو ترتفع ببساطة — كما قد يُتوقع عند حجب استهلاكها — بل انخفضت في العديد من الخلايا. كشف تحليل خلية مفردة أن المجتمع انقسم إلى نوعين فرعيين: أحدهما حافظ على مستويات GSH وملفّات دهنية قريبة من الطبيعي، بينما أظهر الآخر انخفاضًا حادًا في GSH، وضعفًا في إنتاج GSH، وتغيرات بارزة في الجزيئات الدهنية المعرضة للتأكسد. ربطت تجارب إضافية هذه الاختلافات بمستويات متفاوتة من منظم الاستجابة للإجهاد المسمى NRF2، الذي يتحكم في التعبير عن جينات تستورد السيستين وتُكوّن وتُدوّر GSH.
ما معنى هذا للعلاجات المستقبلية
مجتمعة، تُظهر الدراسة أن الجمع بين وسم الثيول في الخلايا الحية ومطيافية الكتلة العضوية يمكنه تثبيت وقياس العديد من الثيولات الهشة إلى جانب استقلاب أوسع في خلايا مفردة. كشف هذا القياس القوي أن RSL3 لا يكتفي بمنع استخدام GSH فحسب: بل يقمع أيضًا إنتاج GSH عبر محور NRF2–الجلوتاثيون، مكوّنًا خلايا فرعية متميزة مقاومة للفيروبتوز وأخرى حساسة له داخل نفس سلالة الورم. للقراء غير المتخصصين، الرسالة الأساسية هي أن الخلايا التي تبدو متماثلة تحت المجهر قد تختلف اختلافًا جذريًا في كيفية إدارتها لمواد واقية مثل الجلوتاثيون، وهذه الاختلافات قد تُقرّر ما إذا نجحت معالجة السرطان أم لا. من خلال تمكين رؤية هذه التباينات الاستقلابية الخفية خليةً خلية، قد تساعد الطريقة الجديدة في تصميم استراتيجيات أدق لدفع الخلايا الضعيفة نحو الموت مع الحفاظ على الخلايا الصحية أو المقاومة.
الاستشهاد: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
الكلمات المفتاحية: ميتوبولوميات خلية مفردة, جلوتاثيون, فيروبتوز, استقلاب الأكسدة والاختزال, تغايرية خلايا سرطان