Clear Sky Science · es
Perfilado de tioles a nivel unicelular habilitado por marcado en células vivas revela heterogeneidad metabólica en ferroptosis
Por qué importan los pequeños compuestos celulares
Cada célula de nuestro cuerpo depende de una familia de pequeñas moléculas que contienen azufre, llamadas tioles, para mantener su química funcionando correctamente. Estas moléculas ayudan a controlar el uso de energía, protegen frente al daño por especies reactivas del oxígeno y deciden si una célula sobrevive o muere. Sin embargo, porque los tioles son frágiles y están presentes en cantidades diminutas, los investigadores han tenido dificultades para medir muchos tioles distintos en células individuales a la vez. Este estudio presenta una forma de congelar y leer los tioles dentro de células vivas individuales, y la usa para descubrir por qué algunas células cancerosas sucumben a un tipo de muerte celular llamado ferroptosis mientras otras resisten.
Fijar a los auxiliares celulares frágiles en su lugar
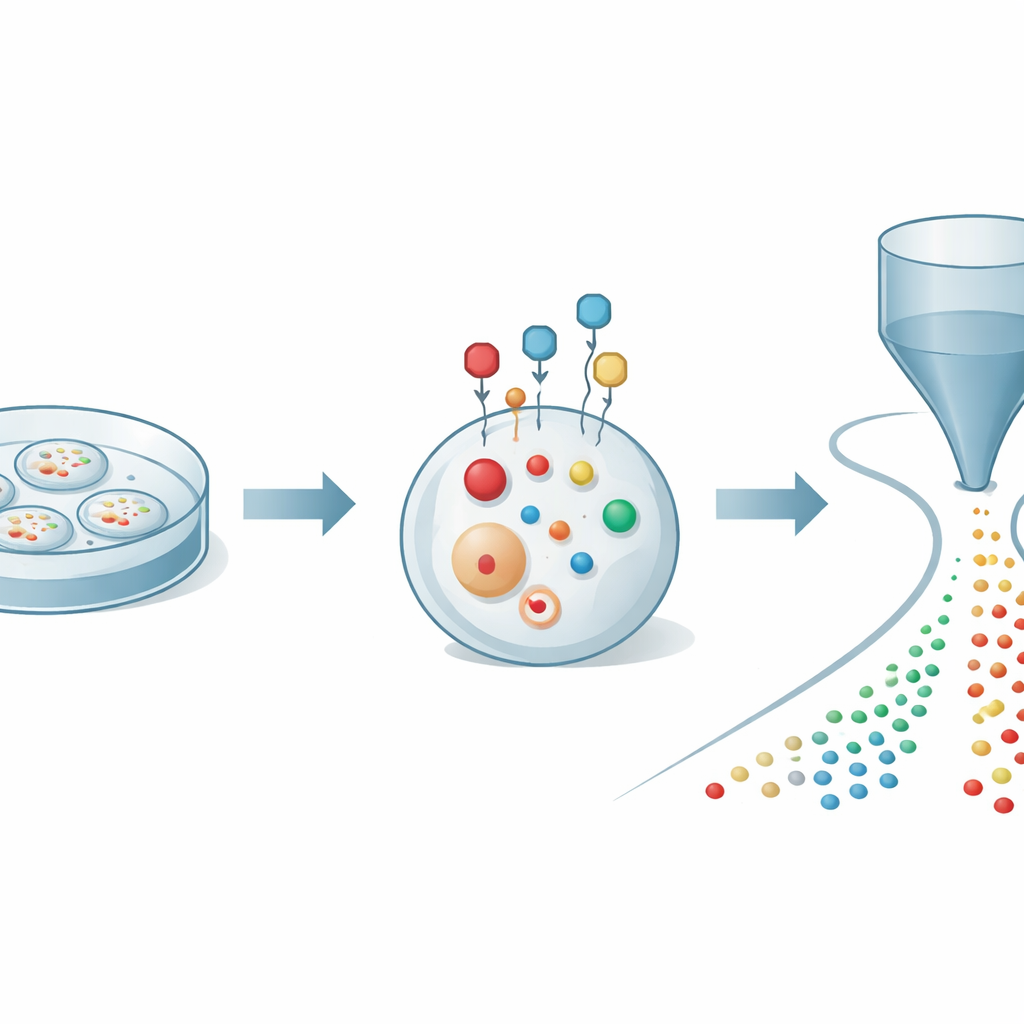
Los autores empezaron abordando un problema básico: los tioles se oxidan y cambian rápidamente cuando las células se rompen para su análisis, lo que puede dar una visión distorsionada de lo que realmente ocurre dentro. Diseñaron una pequeña sonda química que puede atravesar la membrana celular y reaccionar de forma rápida y selectiva con los tioles en células vivas. Una vez unida, la sonda actúa como una jaula protectora y un amplificador: estabiliza los tioles frente a la oxidación y añade una carga eléctrica que los hace mucho más fáciles de detectar por espectrometría de masas. Al ajustar cuidadosamente la estructura de la sonda, el equipo encontró condiciones que marcan los tioles en cuestión de minutos manteniendo la salud celular, lo que les permite capturar una instantánea fiable de la química de los tioles en tiempo real.
Leer cientos de moléculas de células individuales
Para aprovechar este marcado, los investigadores lo acoplaron a una plataforma avanzada de detección conocida como citometría orgánica de masas. En esta configuración, miles de células marcadas son impulsadas suavemente una por una a través de un capilar fino hacia una fuente de ionización conectada a un espectrómetro de masas de alta resolución. A medida que cada célula pasa, sus pequeñas moléculas se extraen y convierten en iones, creando un pulso breve de señales único para esa célula. Herramientas computacionales luego identifican a qué célula pertenece cada pulso y asignan cientos de picos moleculares a cada evento. Con esta estrategia integrada, los autores pudieron cuantificar 27 tioles distintos marcados junto con más de 300 otros metabolitos en células cancerosas individuales, revelando un mapa rico del metabolismo del azufre y de la energía a resolución unicelular.
Observar cómo el estrés se propaga por las redes de azufre
El equipo preguntó a continuación si este enfoque podría seguir cómo responden las células cuando se interrumpen deliberadamente las vías de los tioles. Usaron fármacos que bloquean selectivamente distintos pasos de la síntesis de glutatión (GSH), un tiol principal que protege a las células del daño oxidativo. En células individuales observaron desplazamientos precisos y consistentes con las vías: bloquear la importación de cistina agotó la cisteína y muchos metabolitos de azufre aguas abajo; bloquear enzimas concretas que construyen glutatión hizo que los componentes aguas arriba se acumularan mientras los niveles de GSH caían. Más allá de los tioles, cientos de otros metabolitos también cambiaron en patrones característicos, reflejando cambios más amplios en el equilibrio energético y redox. Estos experimentos mostraron que el método puede seguir cambios sutiles y localizados mientras se propagan por la red interconectada de azufre de la célula.
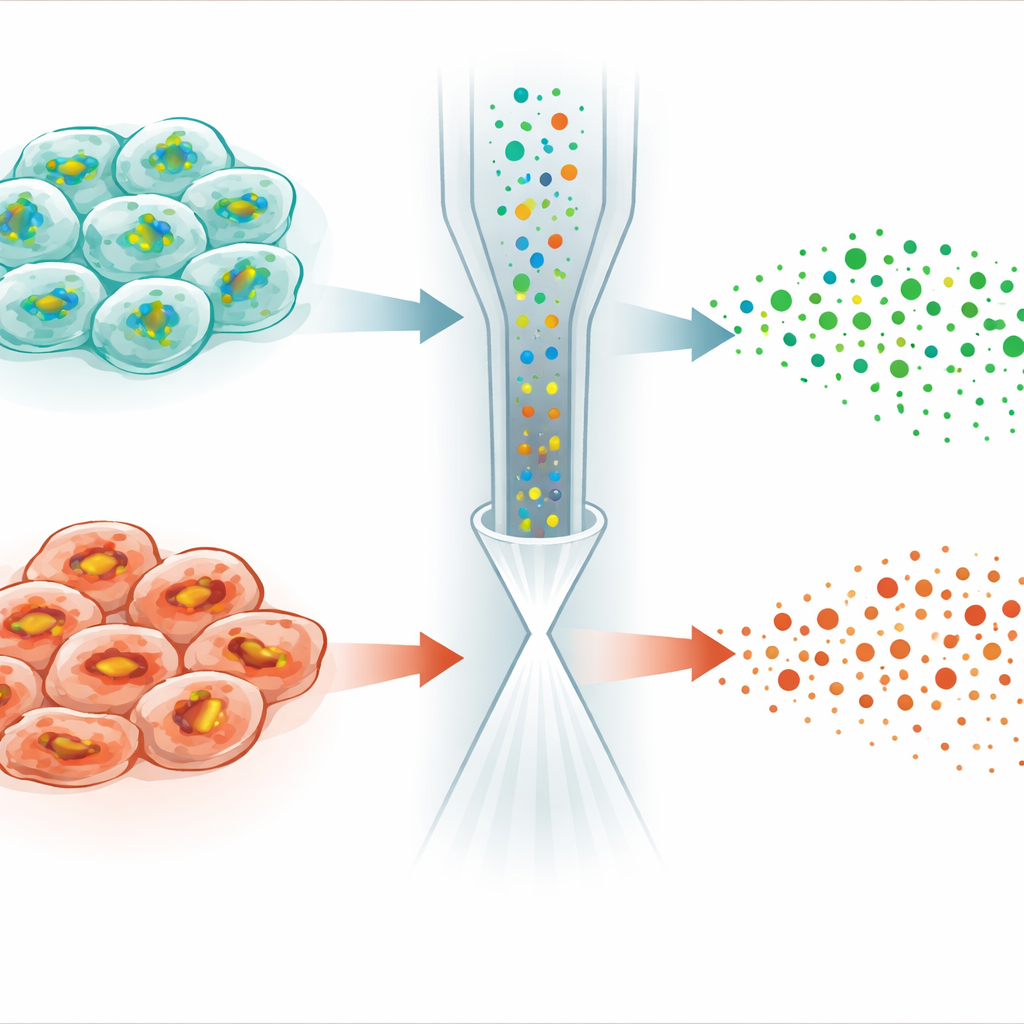
Descubrir diferencias ocultas en la sensibilidad a la muerte celular
La aplicación más llamativa provino del estudio de la ferroptosis, una forma de muerte celular regulada impulsada por daño dependiente de hierro a las membranas celulares. Una pequeña molécula llamada RSL3 mata células cancerosas al inhabilitar una enzima que normalmente usa GSH para desintoxicar peróxidos lipídicos. Sorprendentemente, cuando los autores trataron células HeLa con RSL3, los niveles de GSH no se estabilizaron ni aumentaron —como cabría esperar si se bloquea su consumo— sino que cayeron en muchas células. El análisis unicelular reveló que la población se dividió en dos subtipos: uno mantuvo perfiles de GSH y lípidos casi normales, mientras que el otro mostró una marcada reducción de GSH, debilitamiento de la producción de GSH y cambios importantes en las moléculas lipídicas propensas a la peroxidación. Experimentos adicionales vincularon estas diferencias a niveles variables de un regulador de la respuesta al estrés llamado NRF2, que controla la expresión de genes que importan cistina y sintetizan y reciclan GSH.
Qué significa esto para terapias futuras
En conjunto, el estudio muestra que combinar el marcado de tioles en células vivas con citometría orgánica de masas puede estabilizar y medir muchos tioles frágiles junto con el metabolismo más amplio en células individuales. Esta potente lectura descubrió que RSL3 hace más que bloquear el uso de GSH: también suprime la producción de GSH a través del eje NRF2–glutatión, creando subpoblaciones distintas de células resistentes y sensibles a la ferroptosis dentro de la misma línea tumoral. Para un lector general, el mensaje clave es que células que parecen idénticas al microscopio pueden diferir profundamente en cómo gestionan compuestos protectores como el glutatión, y esas diferencias pueden determinar si una terapia contra el cáncer funciona. Al hacer posible ver estas variaciones metabólicas ocultas una célula a la vez, el nuevo método puede ayudar a diseñar estrategias más precisas para empujar a las células vulnerables hacia la muerte mientras se preservan las sanas o resistentes.
Cita: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Palabras clave: metabolómica unicelular, glutatión, ferroptosis, metabolismo redox, heterogeneidad de células cancerosas