Clear Sky Science · pl
Profilowanie tiooli w pojedynczych komórkach umożliwione przez znakowanie na żywych komórkach ujawnia heterogeniczność metaboliczną w ferroptozie
Dlaczego drobne cząsteczki w komórkach mają znaczenie
Każda komórka w naszym ciele polega na rodzinie małych, zawierających siarkę cząsteczek zwanych tioolami, aby utrzymać sprawne funkcje chemiczne. Te cząsteczki pomagają kontrolować wykorzystanie energii, chronią przed uszkodzeniami wywołanymi przez reaktywne formy tlenu i decydują o przeżyciu lub śmierci komórki. Ponieważ jednak tioole są kruche i występują w bardzo małych ilościach, naukowcy mieli trudności z równoczesnym zmierzeniem wielu różnych tiooli w pojedynczych komórkach. W tym badaniu opisano sposób „zamrożenia” i odczytu tiooli wewnątrz pojedynczych żywych komórek, który pozwolił wyjaśnić, dlaczego niektóre komórki nowotworowe ulegają rodzajowi śmierci komórkowej zwanej ferroptozą, podczas gdy inne wykazują oporność.
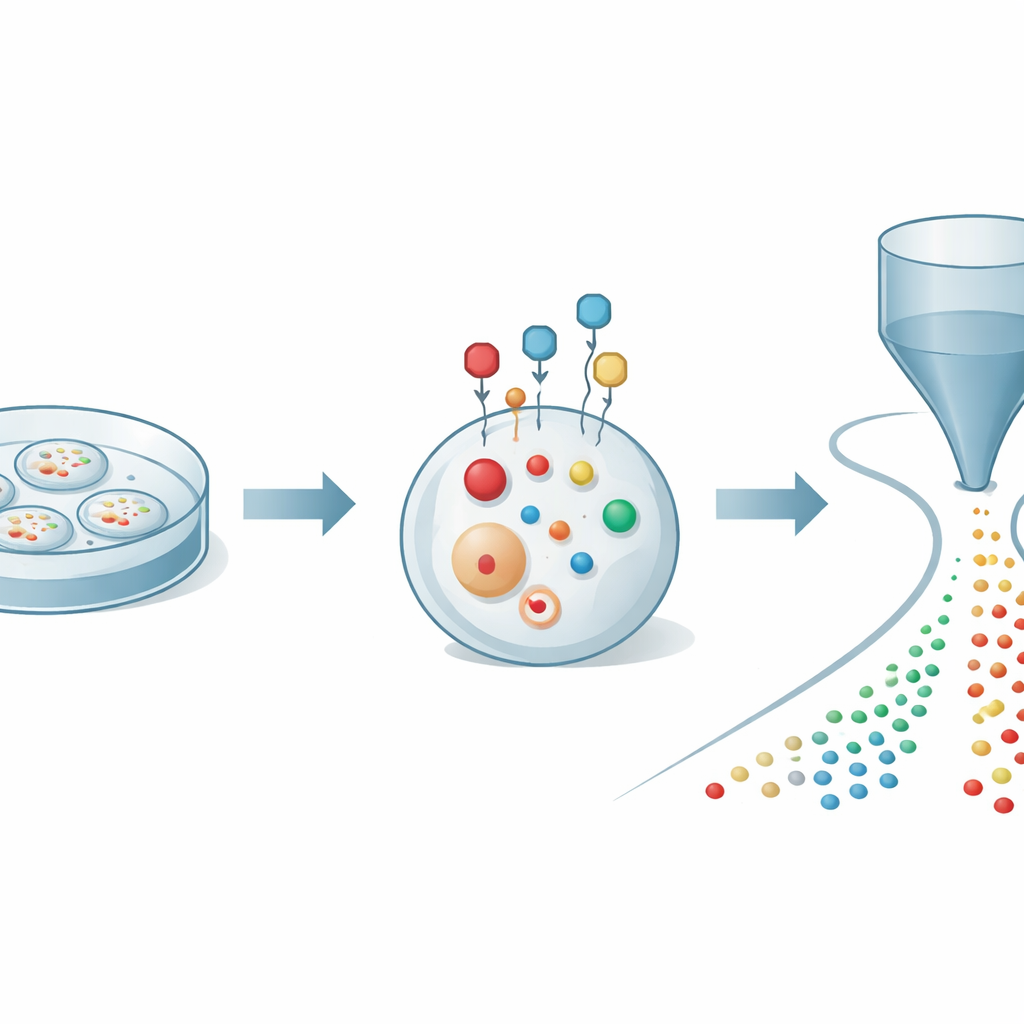
Unieruchamianie podatnych pomocników komórkowych
Autorzy zaczęli od rozwiązania podstawowego problemu: tioole szybko ulegają utlenieniu i zmieniają się, gdy komórki są rozbijane do analizy, co może dawać zniekształcony obraz rzeczywistości wewnątrz. Zaprojektowali małą sondę chemiczną, która przenika przez błonę komórkową i szybko oraz selektywnie reaguje z tioolami w żywych komórkach. Po przyłączeniu sonda działa jak ochronna klatka i wzmacniacz: stabilizuje tioole przed utlenieniem i dodaje ładunek elektryczny, co znacznie ułatwia ich wykrycie metodą spektrometrii mas. Poprzez staranne dostrojenie struktury sondy zespół znalazł warunki, które znakują tioole w ciągu minut, jednocześnie zachowując komórki w stanie zdrowym, co pozwala uchwycić wiarygodne migawki chemii tiooli w czasie rzeczywistym.
Odczytywanie setek cząsteczek z pojedynczych komórek
Aby wykorzystać to znakowanie, badacze połączyli je z zaawansowaną platformą detekcyjną znaną jako organiczna cytometria mas. W tym układzie tysiące znakowanych komórek jest delikatnie przepychanych pojedynczo przez cienką kapilarkę do źródła jonizacji podłączonego do wysokorozdzielczej spektrometrii mas. Gdy każda komórka przechodzi, jej małe cząsteczki są ekstrahowane i przekształcane w jony, tworząc krótką pulsację sygnałów unikalną dla tej komórki. Narzędzia obliczeniowe następnie identyfikują, która pulsacja należy do której komórki i przypisują każdemu zdarzeniu setki pików molekularnych. Dzięki tej zintegrowanej strategii autorzy mogli ilościowo zmierzyć 27 odrębnych znakowanych tiooli oraz ponad 300 innych metabolitów w pojedynczych komórkach nowotworowych, ujawniając bogatą mapę metabolizmu siarki i energetycznego w rozdzielczości pojedynczej komórki.
Obserwowanie, jak stres rozchodzi się w sieciach siarkowych
Zespół następnie zapytał, czy podejście to może śledzić reakcję komórek, gdy ścieżki tioolowe są celowo zakłócane. Użyli leków, które selektywnie blokują różne etapy syntezy glutationu (GSH), głównego tioolu chroniącego komórki przed uszkodzeniami oksydacyjnymi. W pojedynczych komórkach zaobserwowali precyzyjne i zgodne ze ścieżkami przesunięcia: blokada importu cystyny wyczerpywała cysteinę i wiele dalszych metabolitów siarkowych; blokada poszczególnych enzymów budujących glutation powodowała nagromadzenie komponentów upstream przy jednoczesnym spadku poziomów GSH. Poza tioolami setki innych metabolitów także zmieniały się w charakterystycznych wzorcach, odzwierciedlając szersze przesunięcia w bilansie energetycznym i redoks. Te eksperymenty pokazały, że metoda może śledzić subtelne, zlokalizowane zmiany, gdy rozprzestrzeniają się przez połączoną sieć siarkową komórki.
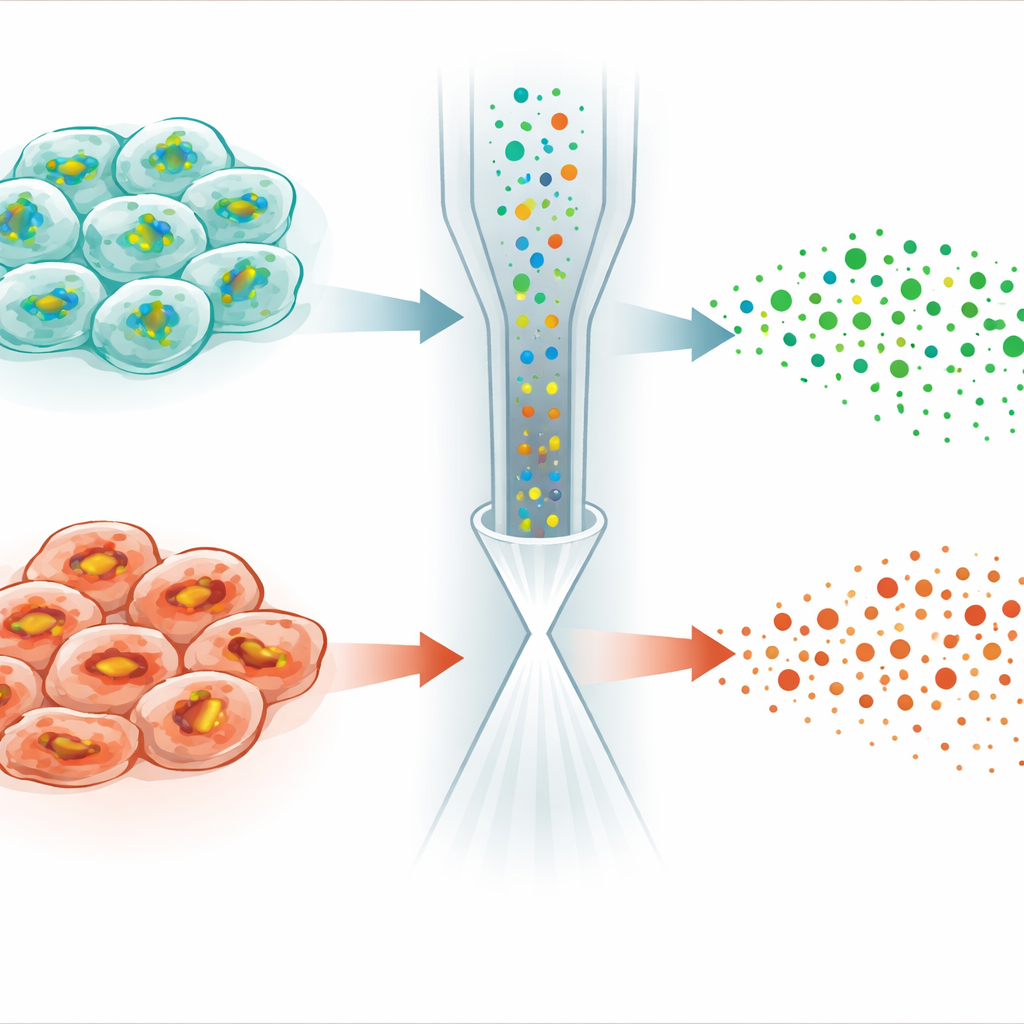
Odkrywanie ukrytych różnic w wrażliwości na śmierć komórkową
Najbardziej uderzające zastosowanie pochodzi z badania ferroptozy, formy regulowanej śmierci komórkowej napędzanej żelazozależnym uszkodzeniem błon komórkowych. Mała cząsteczka o nazwie RSL3 zabija komórki nowotworowe poprzez unieruchomienie enzymu, który normalnie wykorzystuje GSH do detoksykacji nadtlenków lipidów. Zaskakująco, gdy autorzy potraktowali komórki HeLa RSL3, poziomy GSH nie tylko stabilizowały się ani nie rosły — jak można by oczekiwać, gdy jego zużycie jest zablokowane — lecz w wielu komórkach spadły. Analiza pojedynczych komórek ujawniła, że populacja rozdzieliła się na dwie podgrupy: jedna zachowała niemal normalne profile GSH i lipidów, podczas gdy druga wykazała ostre obniżenie GSH, osłabioną produkcję GSH i wyraźne zmiany w lipidach podatnych na peroksydację. Dalsze eksperymenty powiązały te różnice z różnymi poziomami regulatora odpowiedzi na stres zwanego NRF2, który kontroluje ekspresję genów odpowiedzialnych za import cystyny oraz syntezę i recykling GSH.
Co to znaczy dla przyszłych terapii
Podsumowując, badanie pokazuje, że połączenie znakowania tiooli w żywych komórkach z organiczną cytometrią mas umożliwia stabilizację i pomiar wielu podatnych tiooli obok szerszego obrazu metabolizmu w pojedynczych komórkach. Ten potężny odczyt ujawnił, że RSL3 robi więcej niż tylko blokuje użycie GSH: tłumi także produkcję GSH poprzez oś NRF2–glutation, tworząc odrębne podpopulacje komórek opornych i wrażliwych na ferroptozę w obrębie tej samej linii nowotworowej. Dla czytelnika ogólnego kluczowa wiadomość jest taka, że komórki wyglądające identycznie pod mikroskopem mogą różnić się zasadniczo w sposobie gospodarowania ochronnymi związkami, takimi jak glutation, a te różnice mogą decydować o skuteczności terapii przeciwnowotworowej. Dzięki możliwości obserwowania tych ukrytych wariantów metabolicznych po jednej komórce naraz nowa metoda może pomóc w opracowaniu precyzyjniejszych strategii skłaniających podatne komórki do śmierci przy jednoczesnym oszczędzaniu komórek zdrowych lub opornych.
Cytowanie: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Słowa kluczowe: metabolomika pojedynczych komórek, glutation, ferroptoza, metabolizm redoks, heterogeniczność komórek nowotworowych