Clear Sky Science · sv
Encellig tiolprofilering möjliggjord av märkning i levande celler avslöjar metabolisk heterogenitet i ferroptos
Varför små cellkemikalier är viktiga
Varje cell i vår kropp är beroende av en familj små svavelhaltiga molekyler, kallade tioler, för att hålla sin kemi i balans. Dessa molekyler hjälper till att kontrollera energianvändning, skydda mot skador från reaktiva syreradikaler och avgöra om en cell överlever eller dör. Eftersom tioler är sköra och förekommer i mycket små mängder har forskare haft svårt att mäta många olika tioler i enskilda celler samtidigt. Denna studie presenterar ett sätt att fixera och läsa av tioler inuti individuella levande celler, och använder metoden för att avslöja varför vissa cancerceller drabbas av en cellformsdöd som kallas ferroptos medan andra är motståndskraftiga.
Fixera sköra cellhjälpare på plats
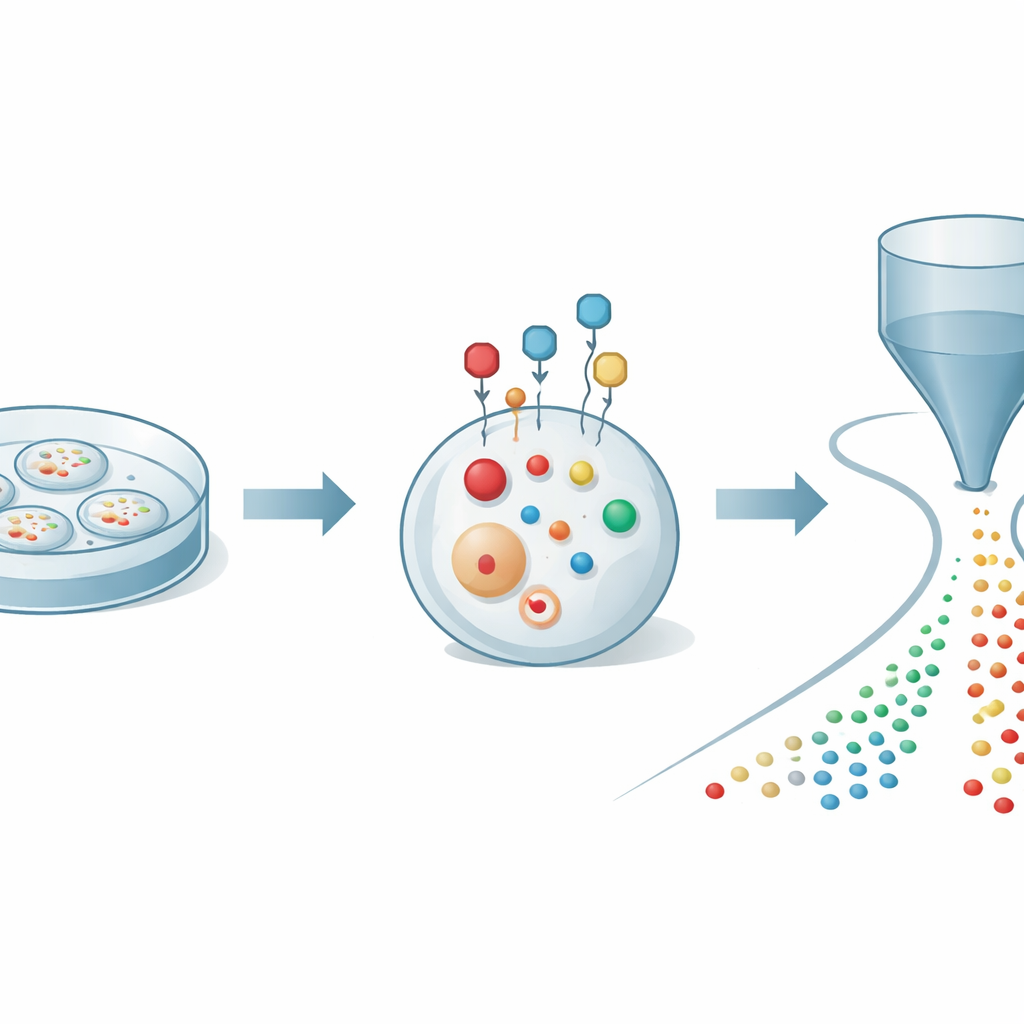
Författarna började med att ta itu med ett grundläggande problem: tioler oxiderar snabbt och förändras när celler bröts upp för analys, vilket kan ge en förvrängd bild av vad som verkligen pågår inuti. De utformade en liten kemisk probe som kan passera cellmembranet och reagera snabbt och selektivt med tioler i levande celler. När proben väl binder fungerar den som både ett skyddande hölje och en förstärkare: den stabiliserar tiolerna mot oxidation och tillsätter en elektrisk laddning som gör dem mycket lättare att detektera med masspektrometri. Genom att finjustera probens struktur fann teamet villkor som märker tioler inom några minuter samtidigt som cellerna hålls friska, vilket möjliggör ett pålitligt ögonblicksbild av tiolkemin i realtid.
Läsa hundratals molekyler från enskilda celler
För att utnyttja denna märkning kopplade forskarna den till en avancerad detektionsplattform känd som organisk masscytometri. I denna uppställning pressas tusentals märkta celler varsamt en efter en genom en tunn kapillär in i en joniseringskälla kopplad till ett högupplöst masspektrometer. När varje cell passerar extraheras och omvandlas dess små molekyler till joner, vilket skapar en kort signalpuls unik för den cellen. Beräkningsverktyg identifierar sedan vilken puls som hör till vilken cell och tilldelar hundratals molekylära toppar till varje händelse. Med denna integrerade strategi kunde författarna kvantifiera 27 distinkta märkta tioler tillsammans med mer än 300 andra metaboliter i individuella cancerceller, och därigenom skapa en rik karta över svavel- och energimetabolism på enkelskalsnivå.
Se hur stress sprider sig genom svavelnätverk
Teamet undersökte sedan om detta tillvägagångssätt kunde följa hur celler reagerar när tiolvägar medvetet störs. De använde läkemedel som selektivt blockerar olika steg i glutathionsyntesen (GSH), en huvudtiol som skyddar celler från oxidativ skada. I enskilda celler observerade de precisa och vägkonsekventa skift: blockering av cystinimport tömde cystein och många nedströms svavelmetaboliter; blockering av enskilda enzymer som bygger glutathion fick uppströmskomponenter att ansamlas medan GSH-nivåerna föll. Utöver tioler förändrades hundratals andra metaboliter också i karaktäristiska mönster, vilket speglar bredare skift i energi- och redoxbalans. Dessa experiment visade att metoden kan följa subtila, lokala förändringar när de sprider sig genom cellens sammanlänkade svavelnätverk.
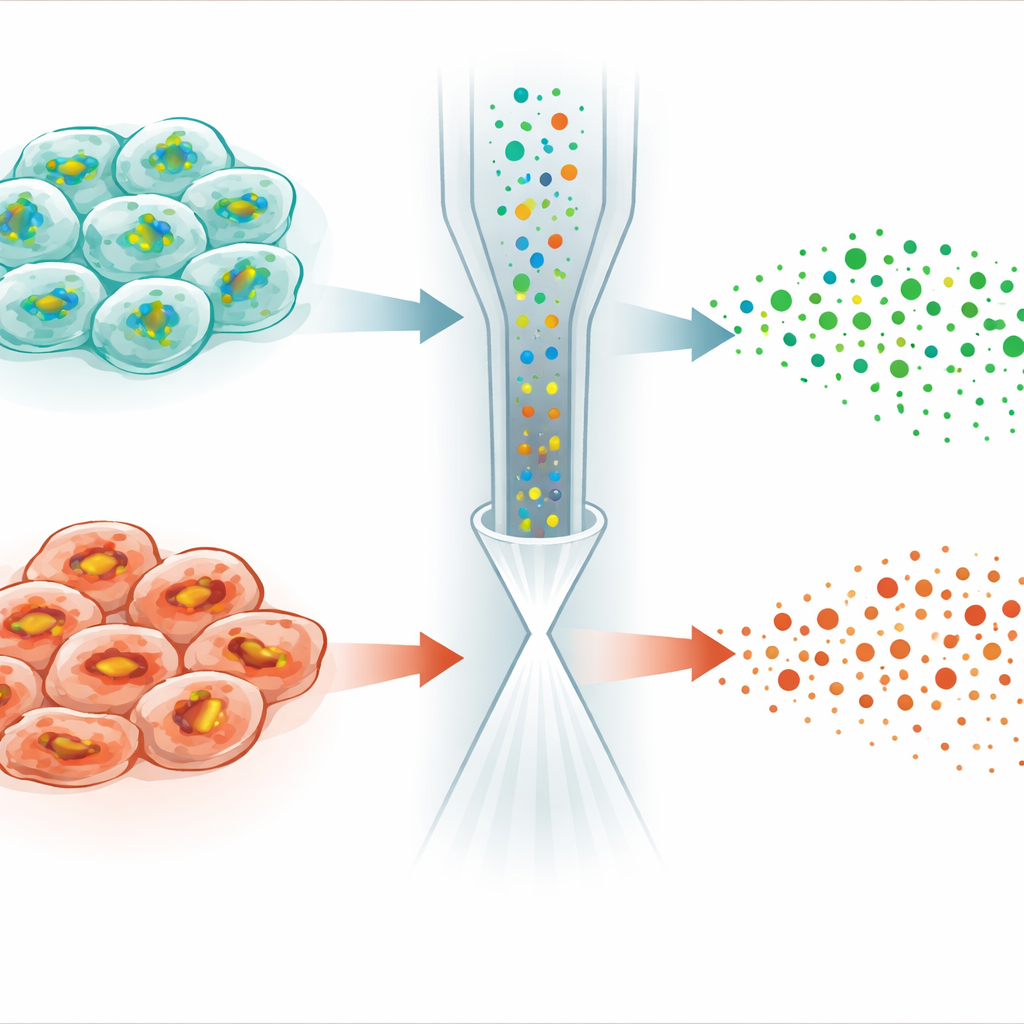
Avslöja dolda skillnader i känslighet för celldöd
Den mest slående tillämpningen kom från studier av ferroptos, en form av reglerad celldöd driven av järnavhängiga skador på cellmembran. En liten molekyl kallad RSL3 dödar cancerceller genom att inaktivera ett enzym som normalt använder GSH för att avgifta lipidperoxider. Överraskande nog, när författarna behandlade HeLa‑cancerceller med RSL3, stabiliserades eller ökade inte GSH‑nivåerna som man kanske skulle förvänta sig när dess konsumtion blockeras — i stället sjönk de i många celler. Encellanalysen visade att populationen delade sig i två undertyper: en behöll närmast normala GSH‑ och lipidprofiler, medan den andra uppvisade kraftigt reducerat GSH, försvagad GSH‑produktion och markanta förändringar i lipidmolekyler som är benägna att peroxideras. Ytterligare experiment kopplade dessa skillnader till varierande nivåer av en stressresponsregulator kallad NRF2, som styr uttrycket av gener som importerar cystin samt syntetiserar och återvinner GSH.
Vad detta innebär för framtida behandlingar
Sammantaget visar studien att kombinationen av märkning av tioler i levande celler och organisk masscytometri kan stabilisera och mäta många sköra tioler tillsammans med bredare metabolism i individuella celler. Denna kraftfulla avläsning avslöjade att RSL3 gör mer än att blockera användningen av GSH: det undertrycker också GSH‑produktionen via NRF2–glutathionaxeln, vilket skapar distinkta subpopulationer av ferroptos‑resistenta och ferroptos‑känsliga celler inom samma tumörlinje. För en allmän läsare är huvudbudskapet att celler som ser identiska ut i mikroskopet kan skilja sig djupt i hur de hanterar skyddande kemikalier som glutathion, och dessa skillnader kan avgöra om en cancerterapi fungerar. Genom att göra det möjligt att se dessa dolda metaboliska variationer en cell i taget kan den nya metoden hjälpa till att utforma mer precisa strategier för att föra sårbara celler mot död samtidigt som friska eller resistenta celler skonas.
Citering: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Nyckelord: single-cell metabolomics, glutathione, ferroptosis, redox metabolism, cancer cell heterogeneity