Clear Sky Science · it
Profilazione dei tioli a singola cellula abilitata da marcatura in cellule vive rivela eterogeneità metabolica nella ferroptosi
Perché contano le piccole sostanze chimiche cellulari
Ogni cellula del nostro corpo dipende da una famiglia di piccole molecole contenenti zolfo, chiamate tioli, per mantenere il suo funzionamento chimico. Queste molecole aiutano a controllare l’uso di energia, proteggono dai danni da ossidanti reattivi e determinano se una cellula sopravvive o muore. Tuttavia, poiché i tioli sono fragili e presenti in quantità minime, i ricercatori hanno faticato a misurare contemporaneamente molti tioli in singole cellule. Questo studio introduce un modo per “congelare” e leggere i tioli all’interno di singole cellule vive, e lo usa per scoprire perché alcune cellule tumorali soccombono a un tipo di morte cellulare chiamata ferroptosi mentre altre resistono.
Bloccare gli aiutanti fragili della cellula
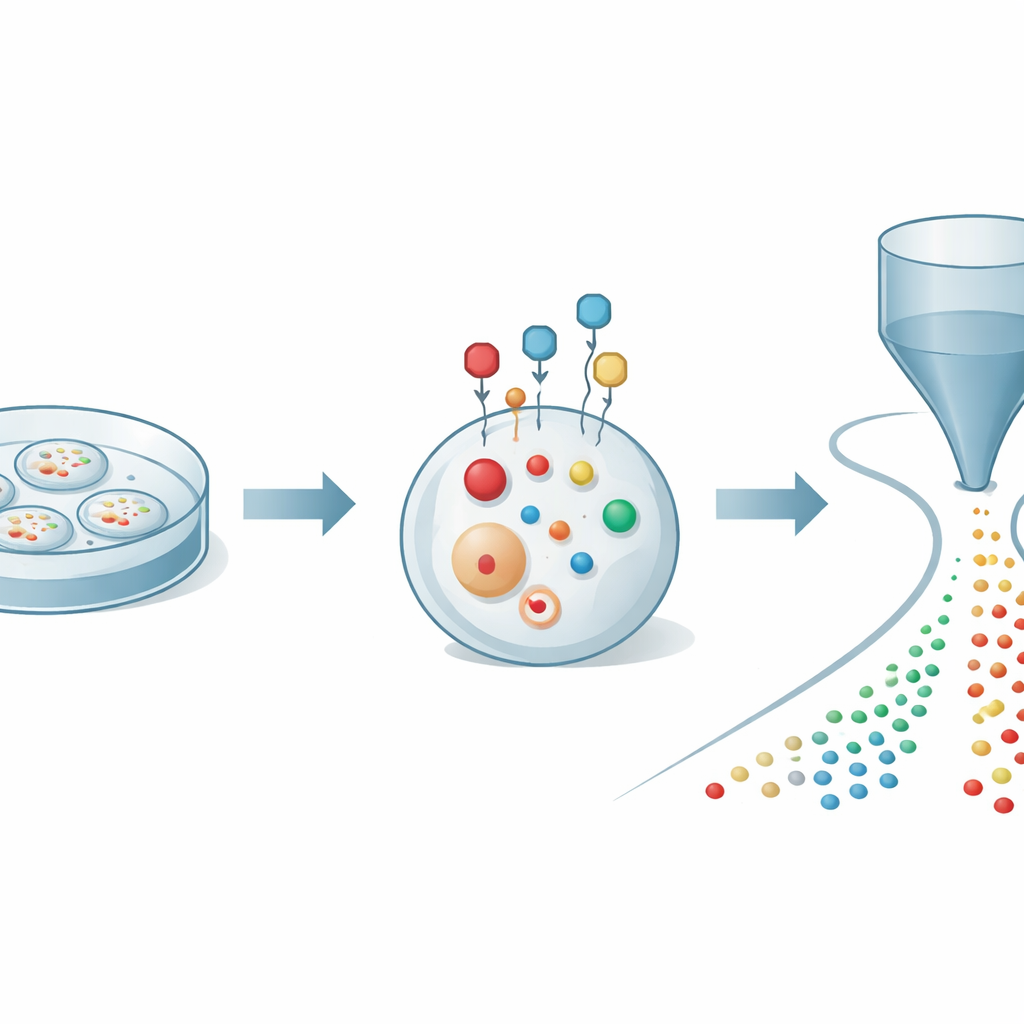
Gli autori hanno iniziato affrontando un problema di base: i tioli si ossidano e si trasformano rapidamente quando le cellule vengono aperte per l’analisi, il che può dare una visione distorta di ciò che accade realmente all’interno. Hanno progettato una piccola sonda chimica in grado di attraversare la membrana cellulare e reagire rapidamente e selettivamente con i tioli nelle cellule vive. Una volta legata, la sonda funziona come una gabbia protettiva e come un amplificatore: stabilizza i tioli contro l’ossidazione e aggiunge una carica elettrica che li rende molto più facili da rilevare mediante spettrometria di massa. Regolando con cura la struttura della sonda, il gruppo ha trovato condizioni che etichettano i tioli in pochi minuti mantenendo le cellule in buona salute, permettendo di catturare un’istantanea attendibile della chimica dei tioli in tempo reale.
Leggere centinaia di molecole da singole cellule
Per sfruttare questa marcatura, i ricercatori l’hanno abbinata a una piattaforma di rilevazione avanzata nota come citometria di massa organica. In questo sistema, migliaia di cellule etichettate vengono spinte delicatamente una alla volta attraverso un capillare sottile verso una sorgente di ionizzazione collegata a uno spettrometro di massa ad alta risoluzione. Quando ogni cellula passa, le sue piccole molecole vengono estratte e convertite in ioni, creando un breve impulso di segnali unico per quella cellula. Strumenti computazionali identificano quindi quale impulso appartiene a quale cellula e assegnano centinaia di picchi molecolari a ciascun evento. Con questa strategia integrata, gli autori sono stati in grado di quantificare 27 tioli distinti etichettati insieme a oltre 300 altri metaboliti in singole cellule tumorali, rivelando una mappa ricca del metabolismo dello zolfo e dell’energia a risoluzione di singola cellula.
Osservare come lo stress si propaga nelle reti dello zolfo
Il gruppo ha poi chiesto se questo approccio potesse tracciare come le cellule rispondono quando le vie dei tioli vengono deliberatamente interrotte. Hanno usato farmaci che bloccano selettivamente diversi passaggi della sintesi del glutatione (GSH), un tiolo principale che protegge le cellule dai danni ossidativi. Nelle singole cellule, hanno osservato spostamenti precisi e coerenti con le vie metaboliche: il blocco dell’importazione della cistina ha esaurito la cisteina e molti metaboliti solforati a valle; il blocco di singoli enzimi che costruiscono il glutatione ha causato l’accumulo dei componenti a monte mentre i livelli di GSH diminuivano. Oltre ai tioli, anche centinaia di altri metaboliti cambiarono secondo schemi caratteristici, riflettendo spostamenti più ampi nell’equilibrio energetico e redox. Questi esperimenti hanno dimostrato che il metodo può seguire cambiamenti sottili e localizzati mentre si propagano attraverso la rete interconnessa dello zolfo della cellula.
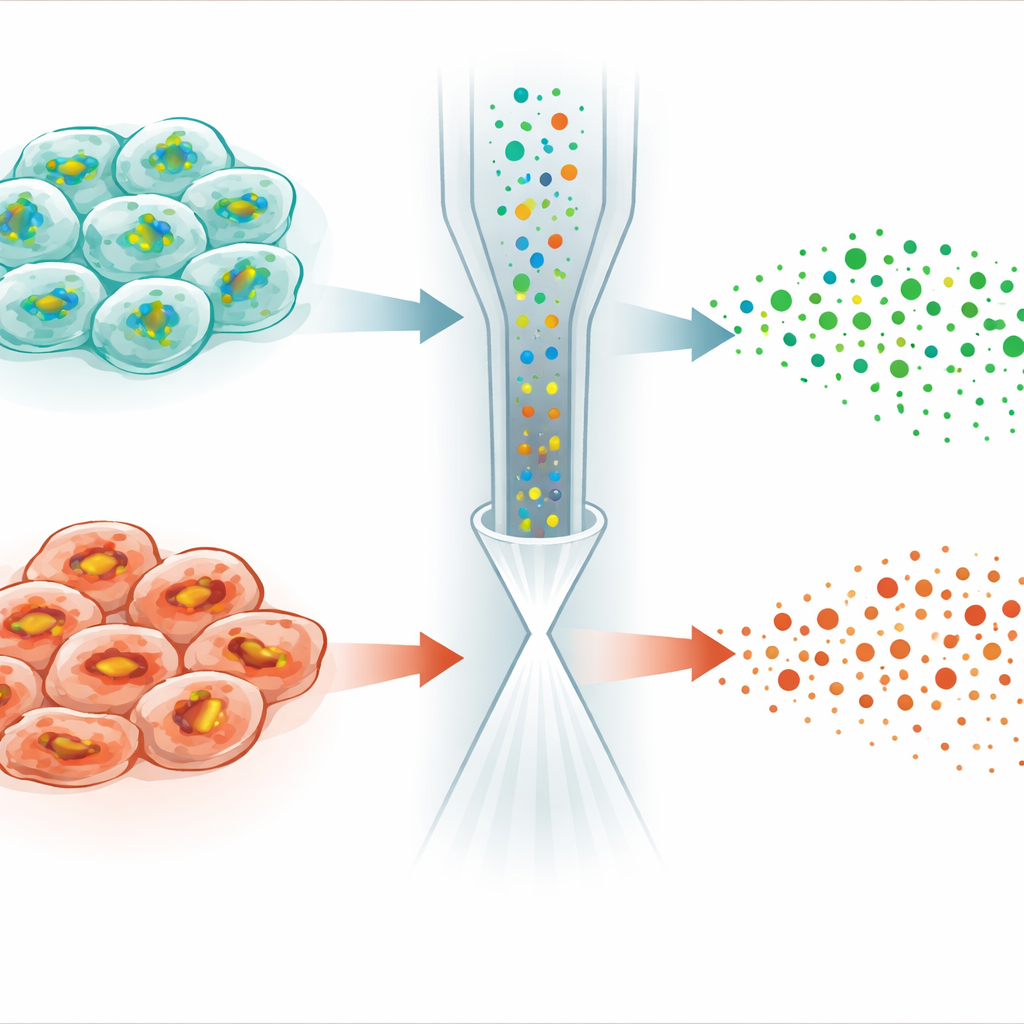
Scoprire differenze nascoste nella sensibilità alla morte cellulare
L’applicazione più sorprendente è emersa dallo studio della ferroptosi, una forma di morte cellulare regolata guidata da danni alle membrane cellulari dipendenti dal ferro. Una piccola molecola chiamata RSL3 uccide le cellule tumorali disattivando un enzima che normalmente usa il GSH per detossificare i perossidi lipidici. Sorprendentemente, quando gli autori trattarono cellule HeLa con RSL3, i livelli di GSH non si stabilizzarono o aumentarono semplicemente — come ci si potrebbe aspettare quando il suo consumo è bloccato — ma diminuirono in molte cellule. L’analisi a singola cellula rivelò che la popolazione si divise in due sottotipi: uno manteneva profili di GSH e lipidi quasi normali, mentre l’altro mostrava GSH fortemente ridotto, una produzione di GSH indebolita e cambiamenti marcati nei lipidi predisposti alla perossidazione. Ulteriori esperimenti collegarono queste differenze a livelli variabili di un regolatore della risposta allo stress chiamato NRF2, che controlla l’espressione di geni che importano cistina e sintetizzano e riciclano il GSH.
Cosa significa per le terapie future
Nel complesso, lo studio mostra che combinare la marcatura dei tioli nelle cellule vive con la citometria di massa organica può stabilizzare e misurare molti tioli fragili insieme al metabolismo più ampio in singole cellule. Questo potente readout ha rivelato che RSL3 fa più che bloccare l’uso del GSH: sopprime anche la produzione di GSH attraverso l’asse NRF2–glutatione, creando sottopopolazioni distinte di cellule resistenti e sensibili alla ferroptosi all’interno della stessa linea tumorale. Per il lettore non specialista, il messaggio chiave è che cellule che appaiono identiche al microscopio possono differire profondamente nel modo in cui gestiscono sostanze protettive come il glutatione, e queste differenze possono determinare se una terapia contro il cancro funziona. Rendendo possibile vedere queste variazioni metaboliche nascoste una cellula alla volta, il nuovo metodo potrebbe aiutare a progettare strategie più precise per spingere le cellule vulnerabili verso la morte risparmiando quelle sane o resistenti.
Citazione: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Parole chiave: metabolomica a singola cellula, glutatione, ferroptosi, metabolismo redox, eterogeneità delle cellule tumorali