Clear Sky Science · nl
Enkel‑cel thiolprofilering mogelijk gemaakt door live‑cel labeling onthult metabole heterogeniteit in ferroptose
Waarom kleine celchemicaliën ertoe doen
Elke cel in ons lichaam is afhankelijk van een familie van kleine zwavelhoudende moleculen, thiolen genoemd, om zijn chemie soepel te laten verlopen. Deze moleculen helpen het energiegebruik te regelen, beschermen tegen schade door reactieve zuurstofsoorten en bepalen of een cel overleeft of sterft. Omdat thiolen echter fragiel zijn en in zeer kleine hoeveelheden voorkomen, hebben onderzoekers moeite gehad om meerdere verschillende thiolen tegelijk in afzonderlijke cellen te meten. Deze studie introduceert een manier om thiolen binnen levende individuele cellen te vergrendelen en af te lezen, en gebruikt die methode om te achterhalen waarom sommige kankercellen bezwijken aan een vorm van celdood die ferroptose wordt genoemd, terwijl andere resistent blijven.
Fragiele celhelpers op hun plaats vergrendelen
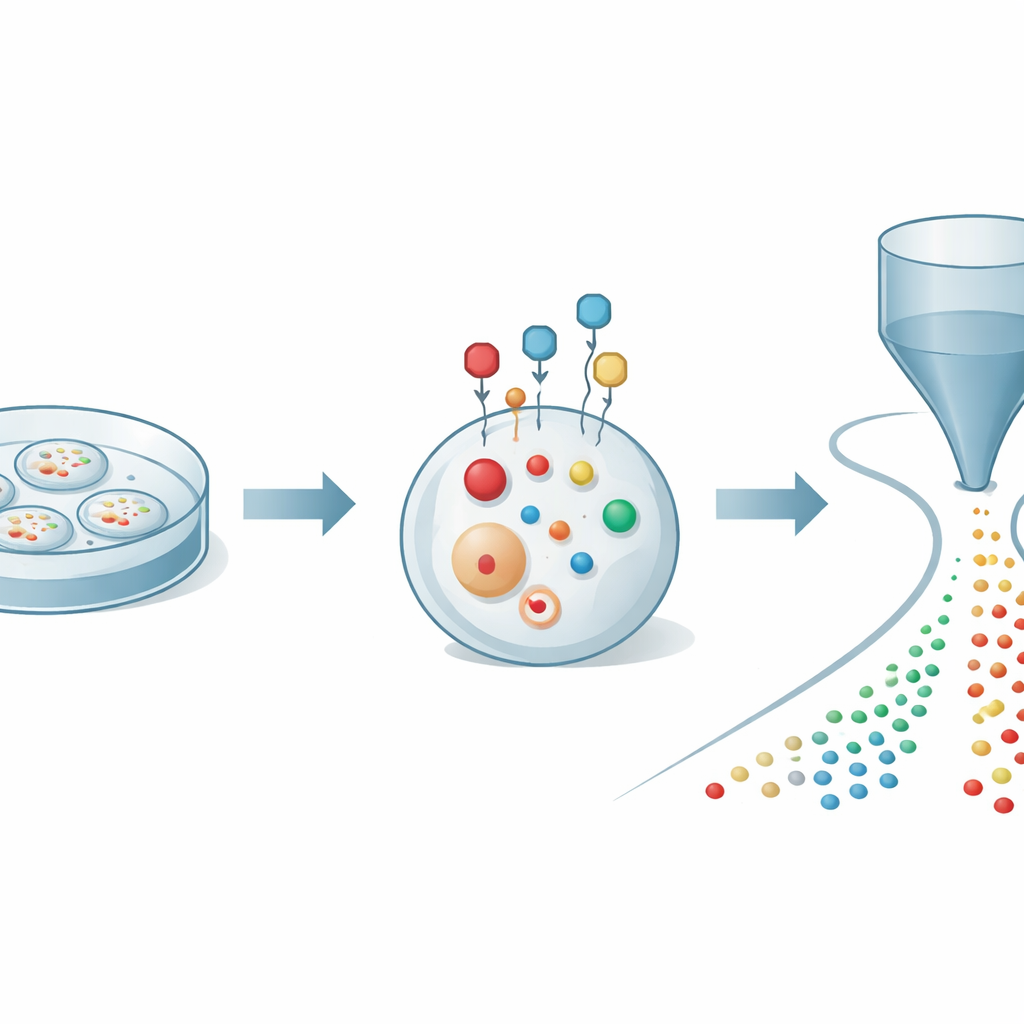
De auteurs begonnen met het aanpakken van een fundamenteel probleem: thiolen oxideren snel en veranderen wanneer cellen worden opengebroken voor analyse, wat een vertekend beeld kan geven van wat er werkelijk binnenin gebeurt. Ze ontwierpen een kleine chemische probe die door het celmembraan kan glippen en snel en selectief reageert met thiolen in levende cellen. Eenmaal bevestigd fungeert de probe als een beschermende kooi en een versterker: hij stabiliseert de thiolen tegen oxidatie en voegt een elektrische lading toe die ze veel gemakkelijker detecteerbaar maakt met massaspectrometrie. Door de structuur van de probe zorgvuldig af te stemmen, vond het team condities die thiolen binnen enkele minuten labelen terwijl de cellen gezond blijven, zodat ze een betrouwbare momentopname van thiolchemie in realtime kunnen vastleggen.
Honderden moleculen uitlezen uit enkele cellen
Om van deze labeling gebruik te maken, koppelden de onderzoekers die aan een geavanceerd detectieplatform dat bekendstaat als organische massacytometrie. In deze opstelling worden duizenden gelabelde cellen één voor één zacht door een dunne capillair in een ionisatiebron geleid die verbonden is met een hogeresolutie‑massaspectrometer. Terwijl elke cel passeert, worden zijn kleine moleculen geëxtraheerd en omgezet in ionen, waardoor een korte puls van signalen ontstaat die uniek is voor die cel. Computationele tools identificeren vervolgens welke puls bij welke cel hoort en wijzen honderden moleculaire pieken toe aan elk evenement. Met deze geïntegreerde strategie konden de auteurs 27 verschillende gelabelde thiolen kwantificeren samen met meer dan 300 andere metabolieten in individuele kankercellen, wat een rijk kaartbeeld van zwavel‑ en energiemetabolisme op enkel‑celresolutie opleverde.
Stress zien doorwerken in zwavelnetwerken
Het team vroeg zich vervolgens af of deze aanpak kon volgen hoe cellen reageren wanneer thiolroutes doelbewust worden verstoord. Ze gebruikten geneesmiddelen die selectief verschillende stappen van de glutathionsynthese (GSH) blokkeren, een belangrijk thiolmolecuul dat cellen beschermt tegen oxidatieve schade. In individuele cellen observeerden ze precieze en routes‑consistente verschuivingen: het blokkeren van cystine‑import leidde tot uitputting van cysteïne en vele downstream zwavelmetabolieten; het blokkeren van afzonderlijke glutathion‑opbouwende enzymen veroorzaakte dat upstream componenten zich ophoopten terwijl de GSH‑niveaus daalden. Buiten de thiolen veranderden ook honderden andere metabolieten in karakteristieke patronen, wat bredere verschuivingen in energie‑ en redoxbalans weerspiegelde. Deze experimenten toonden aan dat de methode subtiele, gelokaliseerde veranderingen kan volgen terwijl ze zich door het onderling verbonden zwavelnetwerk van de cel verspreiden.
Verborgen verschillen in gevoeligheid voor celdood onthullen
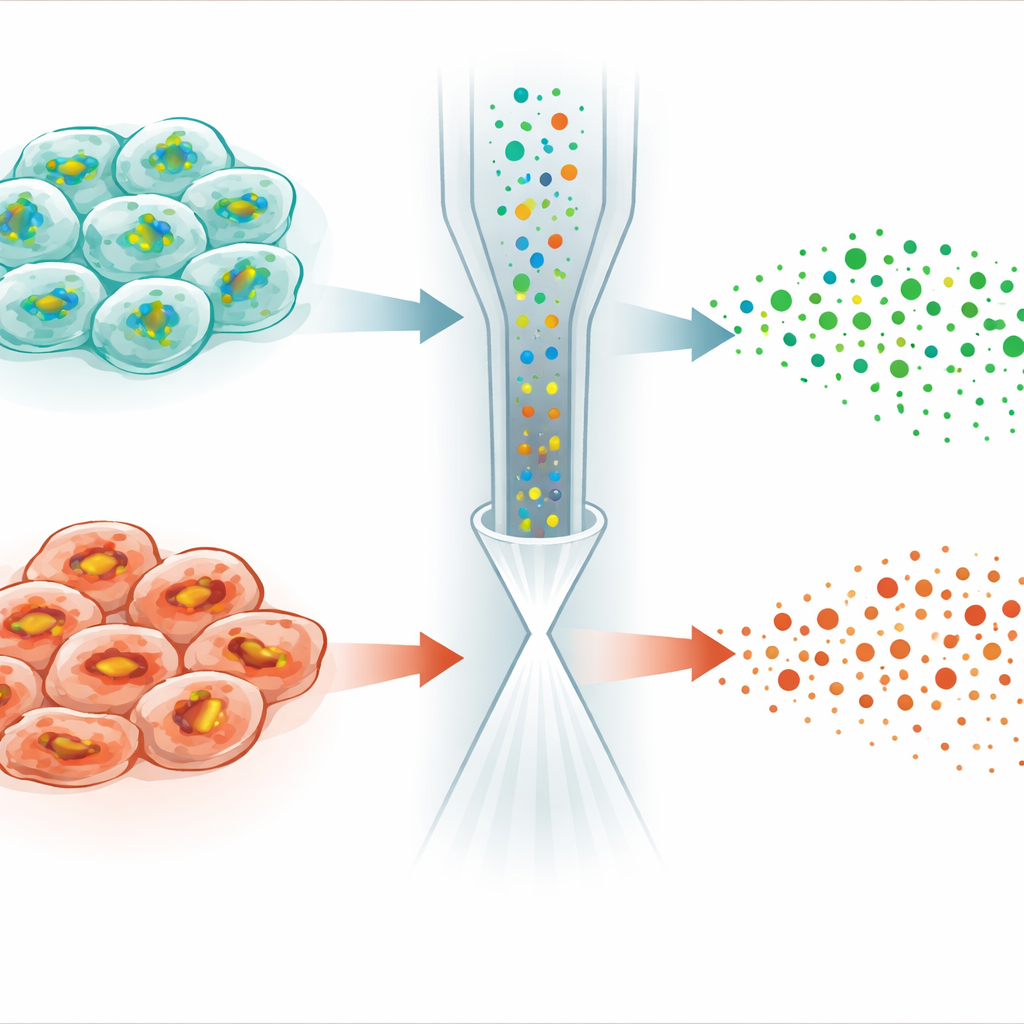
De meest opvallende toepassing kwam uit het bestuderen van ferroptose, een vorm van gereguleerde celdood die wordt aangedreven door ijzerafhankelijke beschadiging van celmembranen. Een klein molecuul genaamd RSL3 doodt kankercellen door een enzym uit te schakelen dat normaal GSH gebruikt om lipideperoxiden te detoxificeren. Verrassend genoeg daalden de GSH‑niveaus in veel cellen toen de auteurs HeLa‑kankercellen met RSL3 behandelden, in plaats van zich simpelweg te stabiliseren of te stijgen—zoals men zou verwachten wanneer het verbruik wordt geblokkeerd. Enkel‑celanalyse onthulde dat de populatie zich splitste in twee subtypen: het ene behield bijna normale GSH‑ en lipideprofielen, terwijl het andere scherp gereduceerde GSH, verzwakte GSH‑productie en duidelijke veranderingen in lipidemoleculen die gevoelig zijn voor peroxidatie vertoonde. Aanvullende experimenten koppelden deze verschillen aan wisselende niveaus van een stressrespons‑regelaar genaamd NRF2, die de expressie van genen regelt die cystine importeren en GSH synthetiseren en recyclen.
Wat dit betekent voor toekomstige therapieën
Samengevat laat de studie zien dat het combineren van live‑cel thiollabeling met organische massacytometrie veel fragiele thiolen samen met bredere metabolismecomponenten in individuele cellen kan stabiliseren en meten. Deze krachtige aflezing onthulde dat RSL3 meer doet dan alleen het gebruik van GSH blokkeren: het onderdrukt ook de GSH‑productie via de NRF2–glutathion‑as, waardoor binnen dezelfde kweeklijn duidelijke subpopulaties van ferroptose‑resistente en ferroptose‑gevoelige cellen ontstaan. Voor een algemeen publiek is de kernboodschap dat cellen die er onder de microscoop identiek uitzien, diepgaand kunnen verschillen in hoe ze beschermende chemicaliën zoals glutathion beheren, en dat die verschillen kunnen bepalen of een kankertherapie werkt. Door het mogelijk te maken deze verborgen metabole variaties cel‑voor‑cel te zien, kan de nieuwe methode helpen bij het ontwerpen van meer gerichte strategieën om kwetsbare cellen naar de dood te duwen terwijl gezonde of resistente cellen worden gespaard.
Bronvermelding: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Trefwoorden: single‑cell metabolomics, glutathion, ferroptose, redoxmetabolisme, heterogeniteit van kankercellen