Clear Sky Science · pt
Perfilamento de tiol em célula única possibilitado por marcação em células vivas revela heterogeneidade metabólica na ferroptose
Por que pequenas moléculas celulares importam
Cada célula do nosso corpo depende de uma família de pequenas moléculas que contêm enxofre, chamadas tióis, para manter sua química funcionando corretamente. Essas moléculas ajudam a controlar o uso de energia, proteger contra danos de oxigênio reativo e determinar se uma célula sobrevive ou morre. No entanto, porque os tióis são frágeis e existem em quantidades ínfimas, os pesquisadores têm dificuldade em medir muitos tióis diferentes em células individuais ao mesmo tempo. Este estudo apresenta uma maneira de congelar e ler tióis dentro de células vivas individuais, e a usa para revelar por que algumas células cancerígenas sucumbem a um tipo de morte celular chamada ferroptose enquanto outras resistem.
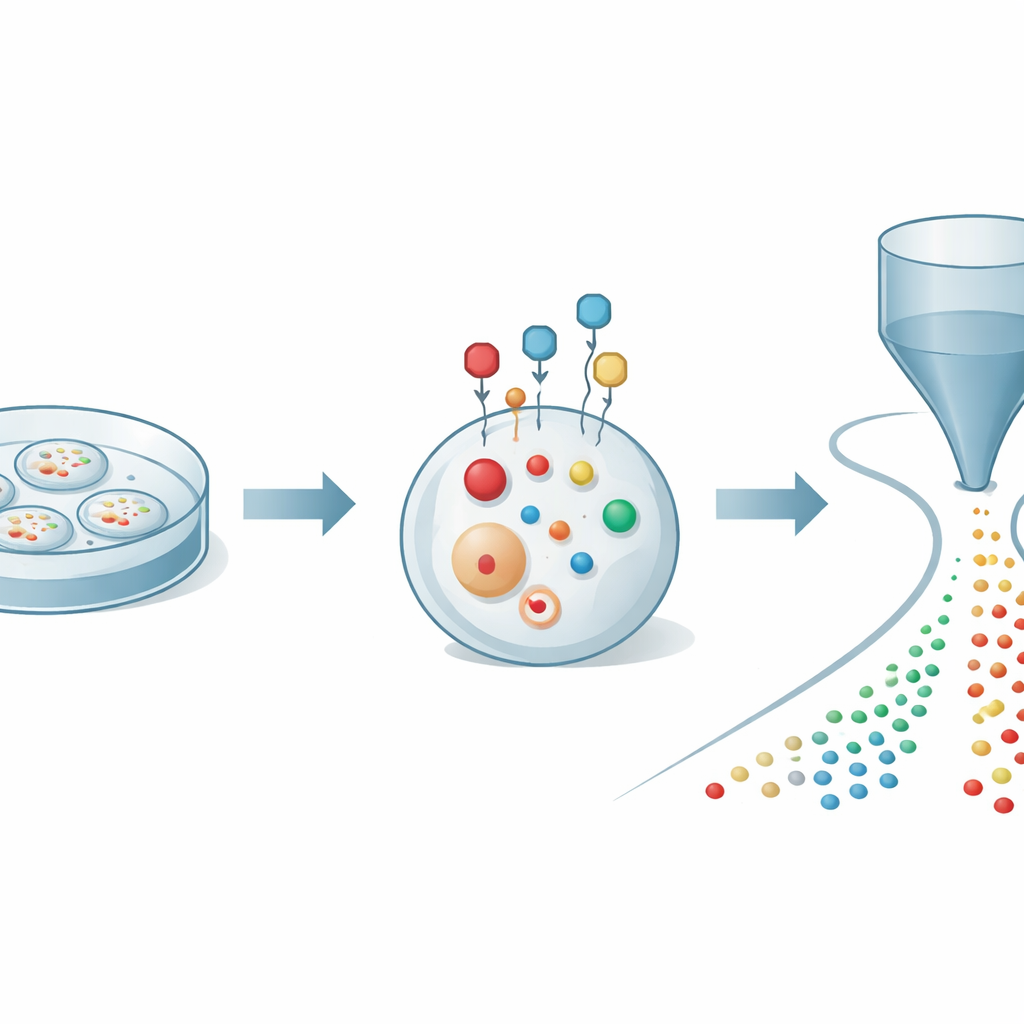
Fixando ajudantes celulares frágeis no lugar
Os autores começaram abordando um problema básico: os tióis oxidam-se rapidamente e mudam quando as células são abertas para análise, o que pode dar uma visão distorcida do que realmente acontece no interior. Eles conceberam uma pequena sonda química que pode atravessar a membrana celular e reagir rápida e seletivamente com tióis em células vivas. Uma vez ligada, a sonda atua como uma gaiola protetora e um amplificador: estabiliza os tióis contra oxidação e adiciona uma carga elétrica que os torna muito mais fáceis de detectar por espectrometria de massa. Ao ajustar cuidadosamente a estrutura da sonda, a equipe encontrou condições que rotulam tióis em minutos mantendo as células saudáveis, permitindo capturar um instantâneo confiável da química dos tióis em tempo real.
Lendo centenas de moléculas de células únicas
Para aproveitar essa marcação, os pesquisadores a acoplaram a uma plataforma de detecção avançada conhecida como citometria de massa orgânica. Nesse arranjo, milhares de células marcadas são gentilmente empurradas uma a uma por um capilar fino até uma fonte de ionização acoplada a um espectrômetro de massa de alta resolução. À medida que cada célula passa, suas pequenas moléculas são extraídas e convertidas em íons, gerando um breve pulso de sinais único para aquela célula. Ferramentas computacionais então identificam a qual célula pertence cada pulso e atribuem centenas de picos moleculares a cada evento. Com essa estratégia integrada, os autores puderam quantificar 27 tióis distintos marcados junto com mais de 300 outros metabólitos em células cancerígenas individuais, revelando um mapa rico do metabolismo de enxofre e energia em resolução de célula única.
Observando como o estresse se propaga pelas redes de enxofre
A equipe em seguida investigou se essa abordagem poderia rastrear como as células respondem quando as vias dos tióis são deliberadamente perturbadas. Eles usaram fármacos que bloqueiam seletivamente diferentes etapas da síntese de glutationa (GSH), um tiol importante que protege as células contra danos oxidativos. Em células individuais, observaram mudanças precisas e consistentes com as vias: bloquear a importação de cistina esgotou a cisteína e muitos metabólitos de enxofre a jusante; bloquear enzimas individuais que sintetizam glutationa fez com que componentes a montante se acumulassem enquanto os níveis de GSH caíam. Além dos tióis, centenas de outros metabólitos também mudaram em padrões característicos, refletindo alterações mais amplas no balanço energético e redox. Esses experimentos mostraram que o método pode acompanhar mudanças sutis e localizadas enquanto se espalham pela rede interconectada de enxofre da célula.
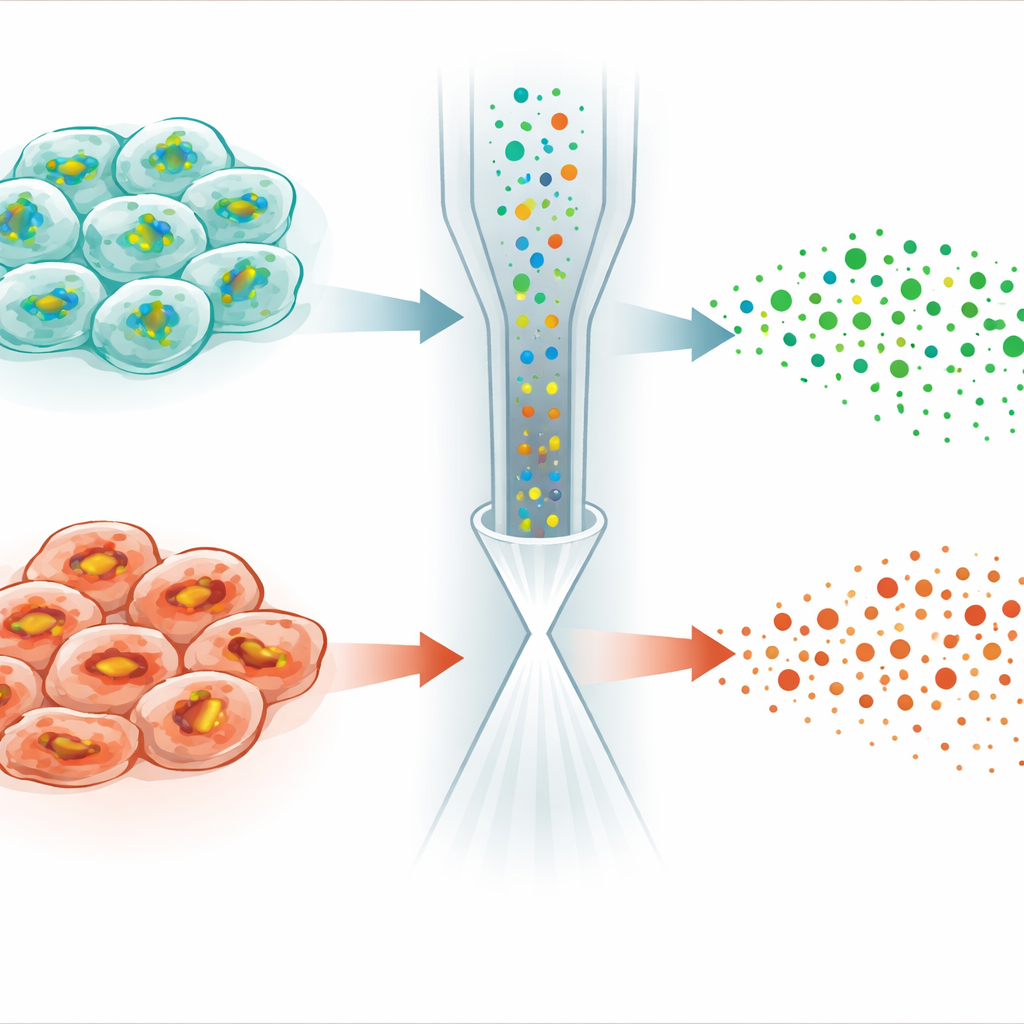
Revelando diferenças ocultas na sensibilidade à morte celular
A aplicação mais notável veio do estudo da ferroptose, uma forma de morte celular regulada impulsionada por danos dependentes de ferro às membranas celulares. Uma pequena molécula chamada RSL3 mata células cancerígenas desabilitando uma enzima que normalmente usa GSH para desintoxicar peróxidos lipídicos. Surpreendentemente, quando os autores trataram células HeLa com RSL3, os níveis de GSH não se estabilizaram ou aumentaram — como se poderia esperar quando seu consumo é bloqueado — mas, em vez disso, caíram em muitas células. A análise em célula única revelou que a população se dividiu em dois subtipos: um manteve perfis quase normais de GSH e lipídios, enquanto o outro mostrou GSH fortemente reduzida, produção de GSH enfraquecida e mudanças marcantes em lipídios propensos à peroxidação. Experimentos adicionais relacionaram essas diferenças a níveis variáveis de um regulador de resposta ao estresse chamado NRF2, que controla a expressão de genes que importam cistina e sintetizam e reciclam GSH.
O que isso significa para terapias futuras
Em conjunto, o estudo mostra que combinar marcação de tióis em células vivas com citometria de massa orgânica pode estabilizar e medir muitos tióis frágeis juntamente com o metabolismo mais amplo em células individuais. Essa leitura poderosa revelou que o RSL3 faz mais do que bloquear o uso de GSH: ele também suprime a produção de GSH por meio do eixo NRF2–glutationa, criando subpopulações distintas de células resistentes e sensíveis à ferroptose dentro da mesma linhagem tumoral. Para um leitor leigo, a mensagem-chave é que células que parecem idênticas ao microscópio podem diferir profundamente em como gerenciam substâncias protetoras como a glutationa, e essas diferenças podem determinar se uma terapia contra o câncer funciona. Ao tornar possível ver essas variações metabólicas ocultas uma célula por vez, o novo método pode ajudar a projetar estratégias mais precisas para conduzir células vulneráveis à morte enquanto poupa as saudáveis ou resistentes.
Citação: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Palavras-chave: metabolômica de célula única, glutationa, ferroptose, metabolismo redox, heterogeneidade de células cancerígenas