Clear Sky Science · fr
Profilage des thiols au niveau unicellulaire permis par un marquage des cellules vivantes révèle l’hétérogénéité métabolique dans la ferroptose
Pourquoi les petites molécules cellulaires comptent
Chaque cellule de notre organisme dépend d’une famille de petites molécules contenant du soufre, appelées thiols, pour maintenir son fonctionnement chimique. Ces molécules aident à contrôler l’utilisation de l’énergie, protègent contre les dommages causés par les espèces réactives de l’oxygène et déterminent si une cellule survit ou meurt. Cependant, parce que les thiols sont fragiles et présents en quantités infimes, les chercheurs ont eu du mal à mesurer simultanément de nombreux thiols dans des cellules individuelles. Cette étude introduit une méthode pour « figer » et lire les thiols à l’intérieur de cellules vivantes individuelles, et l’utilise pour expliquer pourquoi certaines cellules cancéreuses succombent à un type de mort cellulaire appelé ferroptose tandis que d’autres résistent.
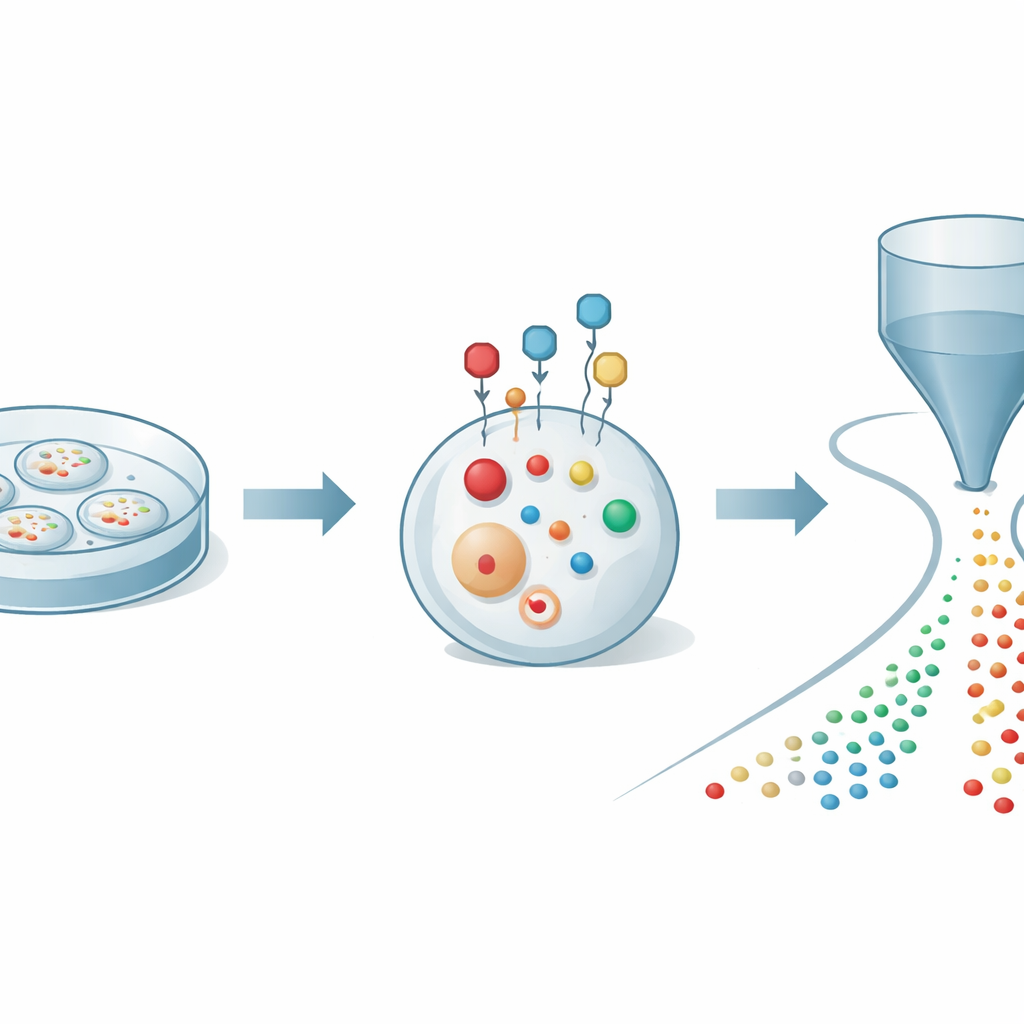
Bloquer les aides cellulaires fragiles en place
Les auteurs ont commencé par s’attaquer à un problème fondamental : les thiols s’oxydent rapidement et se modifient lorsque les cellules sont lysées pour analyse, ce qui peut donner une vision faussée de ce qui se passe réellement à l’intérieur. Ils ont conçu une petite sonde chimique capable de traverser la membrane cellulaire et de réagir rapidement et sélectivement avec les thiols dans les cellules vivantes. Une fois liée, la sonde agit comme une cage protectrice et un amplificateur : elle stabilise les thiols contre l’oxydation et ajoute une charge électrique qui les rend bien plus faciles à détecter par spectrométrie de masse. En ajustant soigneusement la structure de la sonde, l’équipe a trouvé des conditions qui étiquettent les thiols en quelques minutes tout en préservant la santé des cellules, leur permettant de capturer un instantané fiable de la chimie des thiols en temps réel.
Lire des centaines de molécules à partir de cellules individuelles
Pour exploiter ce marquage, les chercheurs l’ont couplé à une plateforme de détection avancée connue sous le nom de cytométrie de masse organique. Dans ce dispositif, des milliers de cellules marquées sont doucement propulsées une à une à travers un capillaire fin vers une source d’ionisation connectée à un spectromètre de masse haute résolution. À mesure que chaque cellule passe, ses petites molécules sont extraites et converties en ions, produisant une brève impulsion de signaux propre à cette cellule. Des outils computationnels identifient ensuite quelle impulsion correspond à quelle cellule et attribuent des centaines de pics moléculaires à chaque événement. Avec cette stratégie intégrée, les auteurs ont pu quantifier 27 thiols marqués distincts ainsi que plus de 300 autres métabolites dans des cellules cancéreuses individuelles, révélant une carte riche du métabolisme du soufre et de l’énergie à résolution unicellulaire.
Observer la propagation du stress dans les réseaux du soufre
L’équipe s’est ensuite demandé si cette approche pouvait suivre la réponse des cellules lorsque les voies des thiols sont délibérément perturbées. Ils ont utilisé des médicaments qui bloquent sélectivement différentes étapes de la synthèse du glutathion (GSH), un thiol majeur qui protège les cellules des dommages oxydatifs. Dans des cellules uniques, ils ont observé des changements précis et cohérents avec les voies : le blocage de l’importation de cystine a appauvri la cystéine et de nombreux métabolites sulfurés en aval ; l’inhibition d’enzymes individuelles de biosynthèse du glutathion a entraîné une accumulation des composés en amont tandis que les niveaux de GSH chutaient. Au‑delà des thiols, des centaines d’autres métabolites ont également évolué selon des schémas caractéristiques, reflétant des déplacements plus larges de l’équilibre énergétique et redox. Ces expériences ont montré que la méthode peut suivre des changements subtils et localisés à mesure qu’ils se propagent dans le réseau interconnecté du soufre de la cellule.
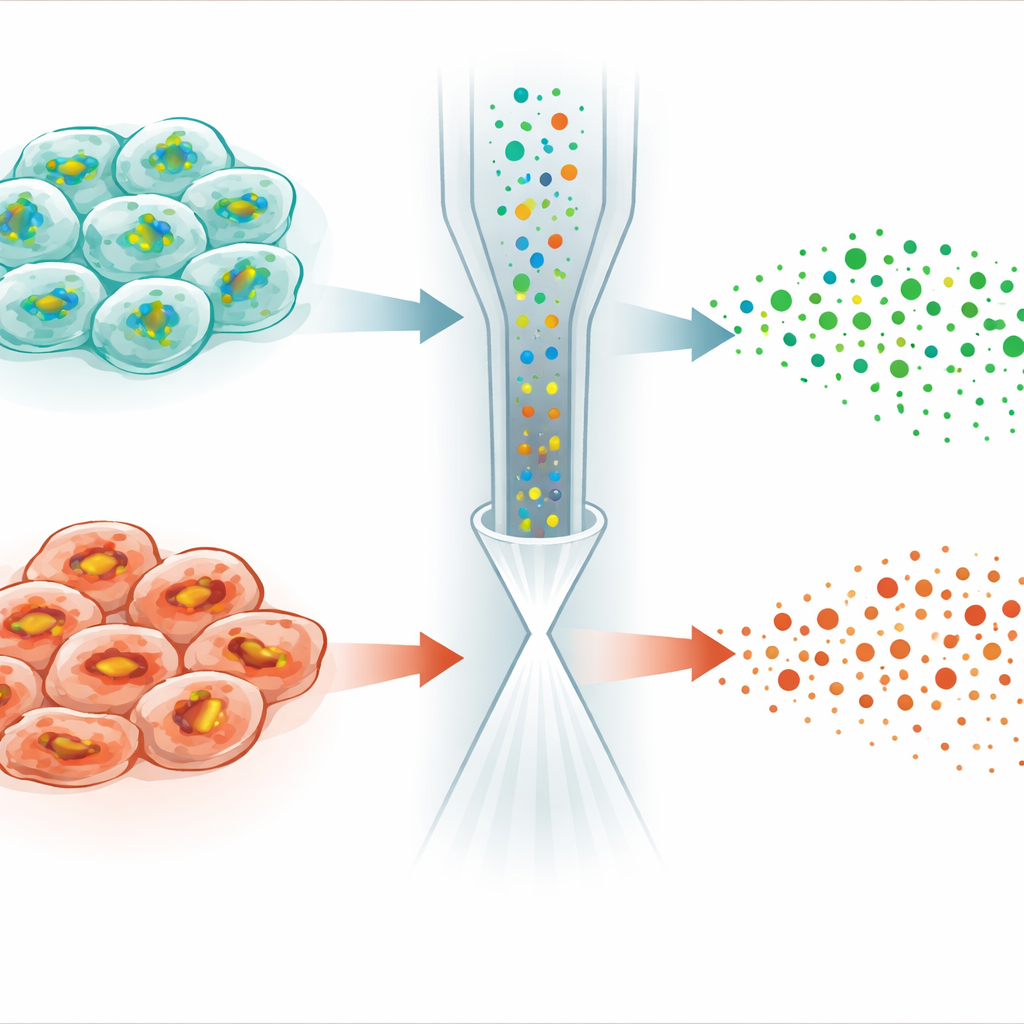
Mettre au jour des différences cachées de sensibilité à la mort cellulaire
L’application la plus frappante est venue de l’étude de la ferroptose, une forme de mort cellulaire régulée provoquée par des dommages dépendants du fer aux membranes cellulaires. Une petite molécule appelée RSL3 tue les cellules cancéreuses en désactivant une enzyme qui utilise normalement le GSH pour détoxifier les peroxydes lipidiques. De manière surprenante, lorsque les auteurs ont traité des cellules HeLa avec RSL3, les niveaux de GSH ne se sont pas simplement stabilisés ou élevés — comme on pourrait s’y attendre lorsque sa consommation est bloquée — mais ont plutôt diminué dans de nombreuses cellules. L’analyse unicellulaire a révélé que la population se divisait en deux sous‑types : l’un conservait des profils de GSH et de lipides proches de la normale, tandis que l’autre présentait une chute marquée du GSH, un affaiblissement de la production de GSH et des modifications nettes des lipides susceptibles de subir une peroxydation. Des expériences supplémentaires ont relié ces différences à des niveaux variables d’un régulateur de la réponse au stress appelé NRF2, qui contrôle l’expression des gènes responsables de l’importation de la cystine et de la synthèse et du recyclage du GSH.
Ce que cela implique pour les thérapies futures
Ensemble, l’étude montre que combiner le marquage des thiols dans les cellules vivantes avec la cytométrie de masse organique permet de stabiliser et de mesurer de nombreux thiols fragiles aux côtés d’un paysage métabolique plus large dans des cellules individuelles. Cette lecture puissante a révélé que RSL3 fait plus que bloquer l’utilisation du GSH : il supprime aussi la production de GSH via l’axe NRF2–glutathion, créant des sous‑populations distinctes de cellules résistantes et sensibles à la ferroptose au sein d’une même lignée tumorale. Pour un lecteur non spécialiste, le message clé est que des cellules qui paraissent identiques au microscope peuvent différer profondément dans la manière dont elles gèrent des molécules protectrices comme le glutathion, et que ces différences peuvent décider de l’efficacité d’une thérapie anticancéreuse. En rendant visibles ces variations métaboliques cachées cellule par cellule, la nouvelle méthode pourrait aider à concevoir des stratégies plus précises pour pousser les cellules vulnérables vers la mort tout en épargnant les cellules saines ou résistantes.
Citation: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Mots-clés: métabolomique unicellulaire, glutathion, ferroptose, métabolisme redox, hétérogénéité des cellules cancéreuses