Clear Sky Science · ru
Профилирование тиолов в отдельных клетках с помощью метки в живых клетках выявляет метаболическую гетерогенность в ферроптозе
Почему важны маленькие молекулы клетки
Каждая клетка в нашем организме зависит от семейства небольших серосодержащих молекул, называемых тиолами, чтобы поддерживать свою химическую работу. Эти молекулы помогают контролировать расход энергии, защищают от повреждений, вызванных реактивным кислородом, и определяют, выживет ли клетка или погибнет. Однако из‑за хрупкости тиолов и их мизерного содержания исследователям трудно одновременно измерять множество разных тиолов в отдельных клетках. В этом исследовании предложен способ зафиксировать и прочитать тиолы внутри отдельных живых клеток, который позволил выяснить, почему одни раковые клетки подвержены виду клеточной гибели, называемому ферроптозом, тогда как другие ему сопротивляются.
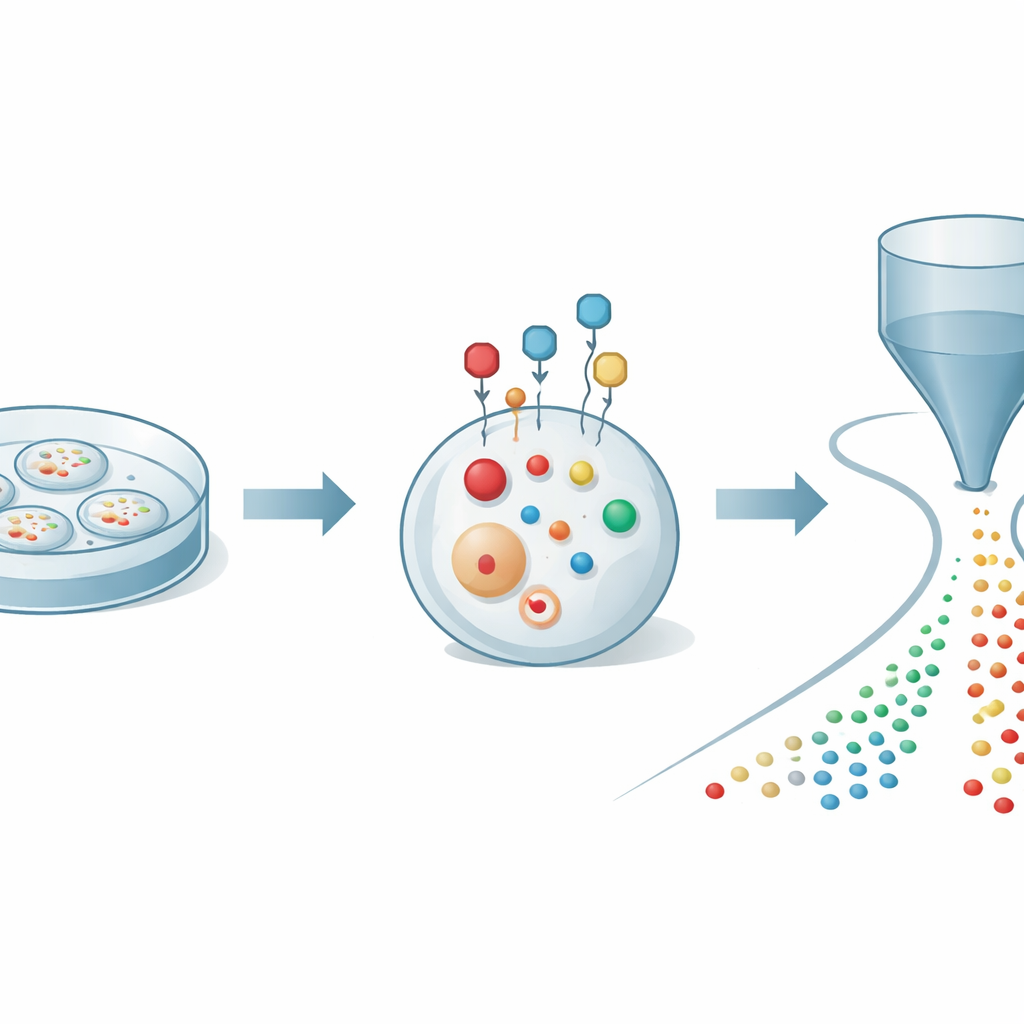
Фиксация хрупких помощников клетки
Авторы начали с решения базовой проблемы: тиолы быстро окисляются и меняются, когда клетки лизируют для анализа, что может искажать представление о том, что действительно происходит внутри. Они разработали небольшой химический зонд, способный проходить через клеточную мембрану и быстро и селективно реагировать с тиолами в живых клетках. После присоединения зонд действует как защитная клетка и усилитель: он стабилизирует тиолы против окисления и добавляет электрический заряд, что делает их значительно проще для обнаружения масс‑спектрометрией. Тщательно настроив структуру зонда, команда нашла условия, при которых маркировка тиолов происходит за считанные минуты, не нарушая жизнеспособности клеток, позволяя получить надежный снимок тиоловой химии в реальном времени.
Чтение сотен молекул из одиночной клетки
Чтобы воспользоваться этой маркировкой, исследователи связали её с продвинутой платформой обнаружения, известной как органическая масс‑цитометрия. В этой системе тысячи маркированных клеток бережно пропускают по одной через тонкую капиллярную трубку в источник ионизации, подключенный к высокоразрешающему масс‑спектрометру. По мере прохождения каждая клетка отдаёт свои небольшие молекулы, которые экстрагируются и превращаются в ионы, создавая краткий импульс сигналов, уникальный для этой клетки. Вычислительные инструменты затем сопоставляют, какой импульс за что отвечает, и назначают сотни молекулярных пиков каждому событию. С помощью этой интегрированной стратегии авторы смогли количественно определить 27 различных маркированных тиолов и более 300 других метаболитов в отдельных раковых клетках, открыв богатую карту серного и энергетического обмена с разрешением до одной клетки.
Наблюдение, как стресс распространяется по серным сетям
Далее команда спросила, может ли подход отслеживать, как клетки реагируют при намеренном нарушении тиоловых путей. Они применили препараты, которые селективно блокируют разные этапы синтеза глутатиона (GSH), основного тиола, защищающего клетки от окислительного повреждения. В отдельных клетках они наблюдали точные и согласованные со схемой сдвиги: блокировка импорта цистина истощала цистеин и многие последующие серные метаболиты; блокировка отдельных ферментов синтеза глутатиона приводила к накоплению предшественников, в то время как уровни GSH падали. Помимо тиолов, сотни других метаболитов также изменялись по характерным шаблонам, отражая более широкие сдвиги в энергетическом и редокс‑балансе. Эти эксперименты показали, что метод способен отслеживать тонкие локальные изменения по мере их распространения через взаимосвязанную серную сеть клетки.
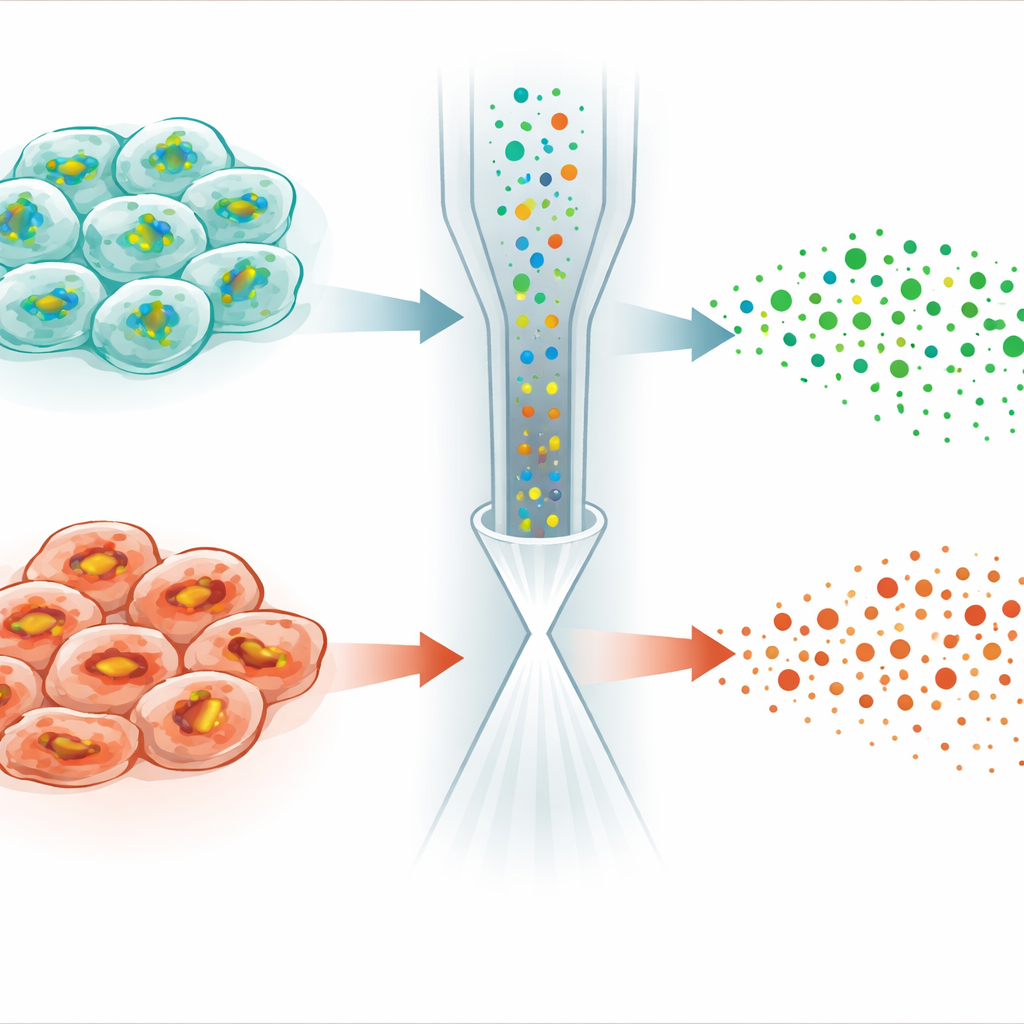
Выявление скрытых различий в чувствительности к гибели клеток
Наиболее впечатляющее применение показали исследования ферроптоза — формы регулируемой гибели клеток, вызванной железозависимым повреждением мембран. Небольшая молекула RSL3 убивает раковые клетки, отключая фермент, который обычно использует GSH для детоксикации липидных перекисей. Удивительно, но при обработке клеток HeLa RSL3 не просто стабилизировал или повышал уровни GSH — как можно было бы ожидать при блокировании его потребления — а напротив, в многих клетках GSH снижался. Анализ поодиночке показал, что популяция разделяется на два подтипа: один сохранял почти нормальные уровни GSH и липидный профиль, тогда как другой демонстрировал резкое снижение GSH, ослабленное производство GSH и заметные изменения в липидах, склонных к перекисному окислению. Дополнительные эксперименты связали эти различия с разными уровнями регулятора стресс‑ответа NRF2, который контролирует экспрессию генов, ответственных за импорт цистина и синтез и восстановление GSH.
Что это значит для будущих терапий
В совокупности исследование показывает, что сочетание маркировки тиолов в живых клетках с органической масс‑цитометрией позволяет стабилизировать и измерять множество хрупких тиолов наряду с более широким спектром метаболизма в отдельных клетках. Этот мощный метод выявил, что RSL3 делает не только блокирование использования GSH: он также подавляет производство GSH через ось NRF2–глутатион, создавая в одной и той же клеточной линии различные субпопуляции, устойчивые и чувствительные к ферроптозу. Для неспециализированного читателя ключевая мысль в том, что клетки, выглядящие одинаково под микроскопом, могут сильно различаться в том, как они управляют защитными молекулами, такими как глутатион, и эти различия могут решать, сработает ли против них противораковая терапия. Возможность видеть эти скрытые метаболические вариации по одной клетке за раз может помочь разработать более точные стратегии, чтобы направлять уязвимые клетки к гибели, щадя при этом здоровые или резистентные клетки.
Цитирование: Miao, D., Li, Q., Zhang, Y. et al. Single-cell thiol profiling enabled by live-cell labeling reveals metabolic heterogeneity in ferroptosis. Nat Commun 17, 3378 (2026). https://doi.org/10.1038/s41467-026-70336-z
Ключевые слова: одноклеточная метаболомика, глутатион, ферроптоз, редокс‑метаболизм, гетерогенность раковых клеток