Clear Sky Science · tr
NHEJ sisteminin DNA çift sarmal kırıklarını algılaması RORγt transkripsiyonel aktivitesini stabilize eder ve otoimmünitede Th17 patojenitesini şekillendirir
DNA Onarımı Dost Ateşini Hastalığa Çevirdiğinde
Bağışıklık sistemimiz enfeksiyonlara karşı T hücrelerine dayanır, ancak bazen bu savunucular kontrolden çıkarak vücudu hedef alır ve gözde üveit veya inflamatuvar bağırsak hastalığı gibi otoimmün hastalıklara yol açar. Bu çalışma şaşırtıcı bir dönüşü ortaya koyuyor: normalde hücreleri hasardan koruyan bir DNA onarım sistemi, özellikle saldırgan bir bağışıklık hücresi türü için gizli bir hızlandırıcı olarak hareket edebilir ve zararı önlemek yerine kronik iltihabı körükleyebilir.
Gizli Bir Alarm Sinyali Olarak DNA Hasarı
T hücreleri güçlü şekilde aktive olduğunda, özellikle otoimmün ortamda öz-antijenlerle karşılaştıklarında, mitokondrileri reaktif oksijen türleri üretir ve bu da DNA’da çift sarmal kırılmalarına yol açabilir. Normalde bu kadar çok kırık ölümcül olur. Buna rağmen yazarlar, patojenik olarak adlandırılan bir Th17 hücre alt grubunun bu stresten yalnızca sağ çıkmakla kalmadığını, aynı zamanda bundan avantaj sağladığını buldular. Bu hücreler, kırıkları hızla algılayan ve yanıt veren homolog olmayan uç birleştirme (NHEJ) olarak bilinen yüksek düzeyde bir DNA onarım yoluna sahiptir. Bu yalnızca DNA’yı yamalamakla ilgili değil: kırıkların algılanması kendisi, Th17 hücrelerini iltihap yapıcı ve hastalık oluşturan bir program içine çekiyor gibi görünüyor; bu özellikle fare modellerinde otoimmün üveit ve kolitte belirgindi. 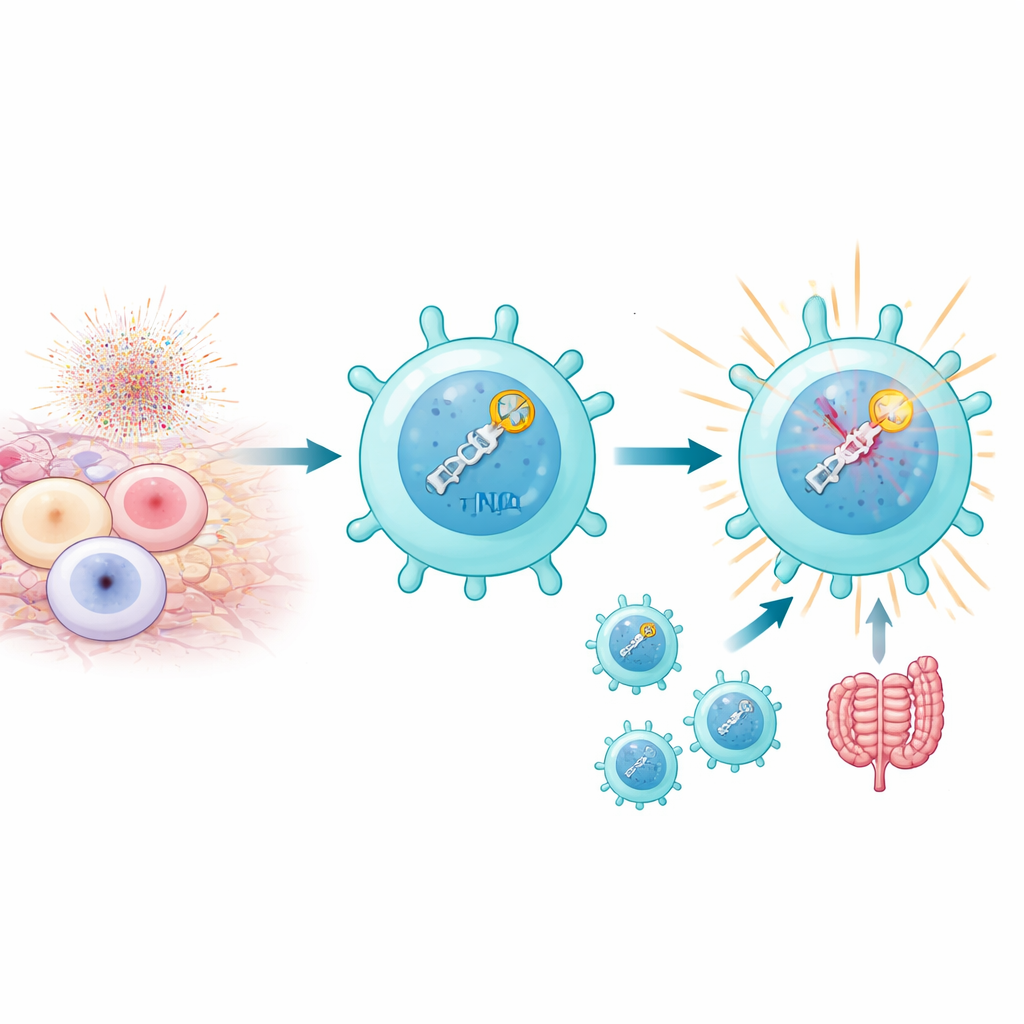
Onarım Değil, Sensörler Zararı Tetikliyor
NHEJ çok adımlı bir süreçtir; kırık DNA uçlarını yakalayan KU70 ve KU80 gibi sensör proteinleriyle başlar ve büyük bir enzim olan DNA-PKcs’yi işe çeker; DNA-PKcs ise kırığı mühürleyen ligaz proteinlerini getirir. Araştırmacılar bu yolun farklı parçalarını T hücrelerinde seçici olarak devre dışı bırakarak, erken algılama adımlarının Th17 patojenitesi için hayati olduğunu, oysa son ligasyon adımının şaşırtıcı şekilde gerekli olmadığını gösterdiler. KU80 veya DNA-PKcs’in yok edilmesi, Th17 hücrelerinin IL-17A, IL-2 ve GM-CSF gibi iltihap yapıcı moleküller üretme ve farelerde doku hasarına neden olma yeteneğini keskin biçimde azalttı. Buna karşılık, DNA ligaz IV’ün ortadan kaldırılması, hücre proliferasyonunu bozmasına rağmen hastalığı hafifletmekte az etkiliydi. Bu deneyler, otoimmünite için gerçekten önemli olanın DNA kırıklarını algılama eylemi olduğunu, onları mutlaka onarmak olmadığını gösteriyor.
Bir DNA Onarım Enzimi Gen Güçlendiricisi Olarak İkinci İş
Daha derine inildiğinde ekip, DNA-PKcs’nin kırık DNA uçlarında durmaktan fazlasını yaptığını keşfetti. KU sensörleri tarafından aktive edildiğinde, DNA-PKcs PQR kümesi olarak adlandırılan bir bölgede kimyasal olarak kendini modifiye ediyordu. Bu durumda DNA-PKcs, Th17 hücrelerini tanımlayan ana transkripsiyon faktörü RORγt ile fiziksel olarak bağlanabiliyordu. Bu ortaklık, RORγt’nin efektör genlerin yakınındaki DNA’da stabilize olmasını ve bu kromatin bölgelerinin açık ve erişilebilir kalmasını sağlıyordu. DNA-PKcs çıkarıldığında ya da PQR kümesi spesifik olarak silindiğinde, RORγt artık anahtar iltihap gen bölgelerinde etkin bir şekilde yer alamadı ve Th17 hücreleri otoimmüniteyi körükleme güçlerinin büyük bir kısmını kaybetti. Fare modellerinde, bu şekilde değişime uğramış hücreler bağışıklık sisteminde bulunmalarına rağmen retinayı iltihaplandıramadı. 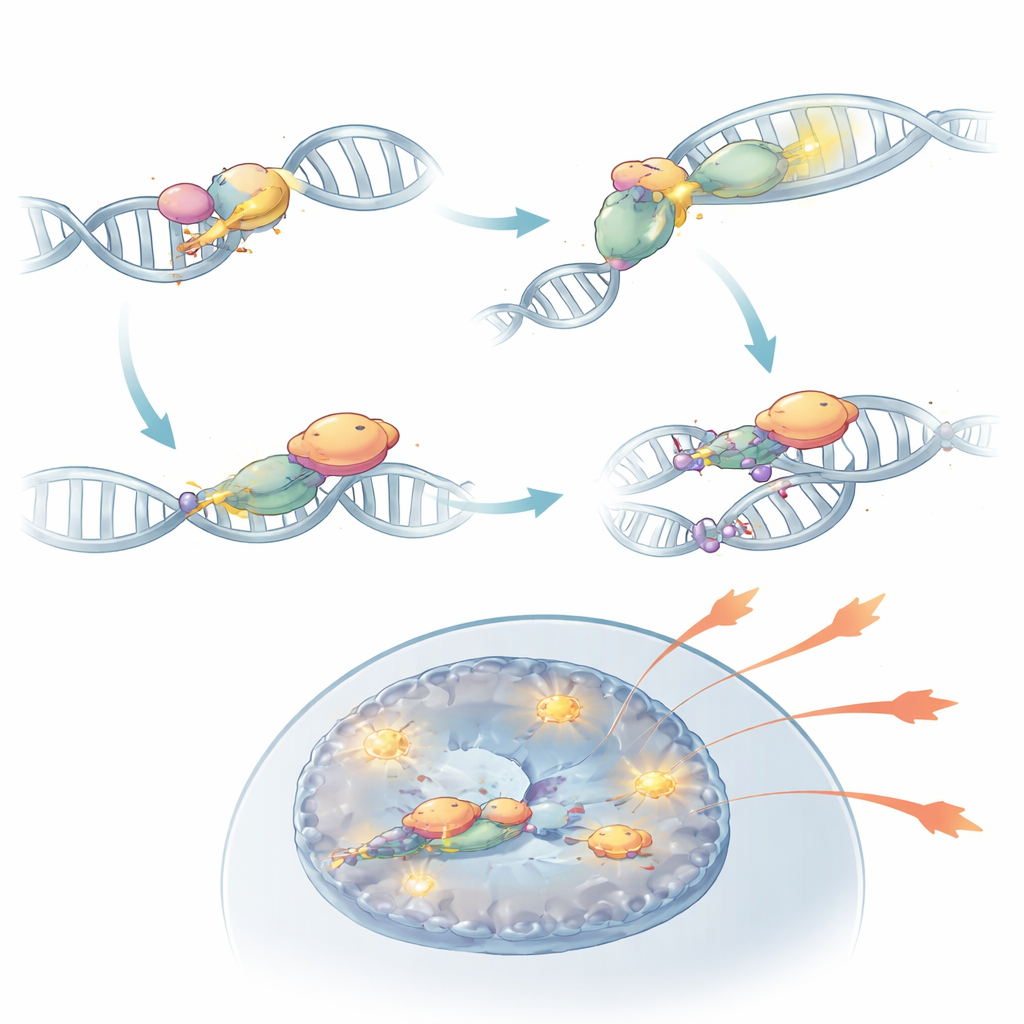
Onarımı ve İltihabı Besleyen Bir Sitokin Sinyali
Çalışma ayrıca bu DNA algılama ağını iyi bilinen bir iltihap mesajcısı olan IL-23 ile ilişkilendiriyor. IL-23, Th17 hücrelerini zararlı, dokuya zarar veren bir duruma itmesiyle tanınır. Burada IL-23’ün NHEJ aktivitesini artırdığı, DNA kırıklarının birikimini azalttığı ve DNA-PKcs’nin PQR bölgesindeki aktive edici modifikasyonunu güçlendirdiği gösterildi. Bu etki IL-23 reseptörüne bağlıydı: reseptörü olmayan Th17 hücreleri NHEJ’i etkin şekilde aktive edemedi ve daha fazla DNA hasarı biriktirdi. Büyük ölçekli protein ve RNA analizleriyle yazarlar, IL-23 sinyalleşmesi ile DNA-PKcs arasında bir köprü görevi gören daha önce az takdir edilmiş bir protein olan IER2’yi tanımladılar. IL-23 IER2’yi indükler, IER2 sonra DNA-PKcs’nin kinaz aktivitesini artırır ve hem DNA onarımını hem de RORγt kaynaklı iltihap gen ekspresyonunu sürdürür.
Hastalarda Yüksek Riskli Bir Th17 Alt Grubu
Bu mekanizmaları insan hastalığıyla ilişkilendirmek için araştırmacılar, farklı klinik aşamalardaki otoimmün üveitli hastalardan immün hücreleri profilleştirdiler. Tek hücre RNA dizilemesi kullanarak, IER2 ve NHEJ ilişkili genlerde özellikle DNA-PKcs bileşenlerinde yüksek düzeylere sahip bir Th17 alt popülasyonu keşfettiler. Bu IER2-yüksek Th17 hücreleri, aktif, nüks eden hastalığı olan hastalarda en bol bulunanlardı ve güçlü metabolik aktivite, sinyal ve iltihap imzaları gösteriyorlardı. Ayrıca daha az çözülmemiş DNA kırığıyla verimli DNA onarım belirteçleri taşıyorlardı. Hesaplamalı analiz, Th17 hücreleri IER2 ekspresyonu yönünde gelişimsel bir yola ilerledikçe iltihap potansiyellerinin paralel olarak arttığını öne sürdü ve bu alt grubu şiddetli otoimmünitenin muhtemel bir sürücü olarak işaretledi.
Korumacı Bir Sistemi Terapötik Bir Hedefe Çevirmek
Genel olarak çalışma, genomu korumayı amaçlayan bir DNA onarım sensör sisteminin tehlikeli bağışıklık yanıtları için bir kontrol düğmesi olarak da işlev gördüğünü resmediyor. Patojenik Th17 hücreleri, NHEJ algılamasını, DNA-PKcs aktivasyonunu ve IL-23–IER2 eksenini kullanarak RORγt’yi stabilize ediyor ve DNA hasarını dengede tutarken yüksek çıktılı iltihaplı bir durumu sürdürüyor. Hastalar için bu, yeni tedavi açıları öneriyor: bağışıklık sistemini geniş çapta baskılamak yerine, KU aracılı DNA kırığı algılaması, DNA-PKcs’in PQR kümesindeki aktivasyonu veya IER2–DNA-PKcs etkileşimini seçici olarak engelleyen ilaçlar Th17 patojenitesini azaltabilir ve diğer hücrelerdeki temel DNA onarımını tamamen engellemeden otoimmün hastalığı yatıştırabilir.
Atıf: Chen, GY., Zhu, WJ., Li, Z. et al. Sensing of DNA double-strand breaks by the NHEJ system stabilizes RORγt transcriptional activity and shapes Th17 pathogenicity in autoimmunity. Cell Res 36, 340–358 (2026). https://doi.org/10.1038/s41422-025-01204-6
Anahtar kelimeler: Th17 hücreleri, DNA onarımı, otoimmünite, DNA-PKcs, IL-23 sinyalleşmesi