Clear Sky Science · de
Das Erkennen von DNA-Doppelstrangbrüchen durch das NHEJ-System stabilisiert die RORγt-Transkriptionsaktivität und prägt die Pathogenität von Th17-Zellen bei Autoimmunerkrankungen
Wenn DNA-Reparatur aus Kollateralschaden Krankheit macht
Unser Immunsystem ist auf T‑Zellen angewiesen, um Infektionen abzuwehren, doch manchmal schlagen diese Verteidiger fehl und richten sich gegen den eigenen Körper, was zu Autoimmunerkrankungen wie Uveitis im Auge oder entzündlichen Darmerkrankungen führt. Diese Studie offenbart eine überraschende Wendung: Ein DNA‑Reparatursystem, das normalerweise Zellen vor Schäden schützt, kann auch als versteckter Beschleuniger eines besonders aggressiven Immunzelltyps wirken und so chronische Entzündung antreiben statt Schaden zu verhindern.
DNA‑Schäden als versteckter Alarm
Wenn T‑Zellen stark aktiviert werden, insbesondere durch Selbstantigene in autoimmunen Situationen, produzieren ihre Mitochondrien Schübe reaktiver Sauerstoffspezies, die DNA in Doppelstrangbrüche zerreißen können. Normalerweise sind zu viele dieser Brüche tödlich. Die Autoren fanden jedoch, dass eine Untergruppe, sogenannte pathogenetische Th17‑Zellen, diesen Stress nicht nur überlebt, sondern ihn zu ihrem Vorteil nutzt. Diese Zellen weisen hohe Aktivität eines DNA‑Reparaturwegs auf, der als nicht‑homologe Endverknüpfung (NHEJ) bekannt ist und Brüche rasch erkennt und darauf reagiert. Dabei geht es nicht nur um das Flicken von DNA: Das Erkennen der Brüche selbst scheint in das Programm einzuspeisen, das Th17‑Zellen entzündlich und krankheitsfördernd macht, insbesondere in Mausmodellen von autoimmuner Uveitis und Kolitis. 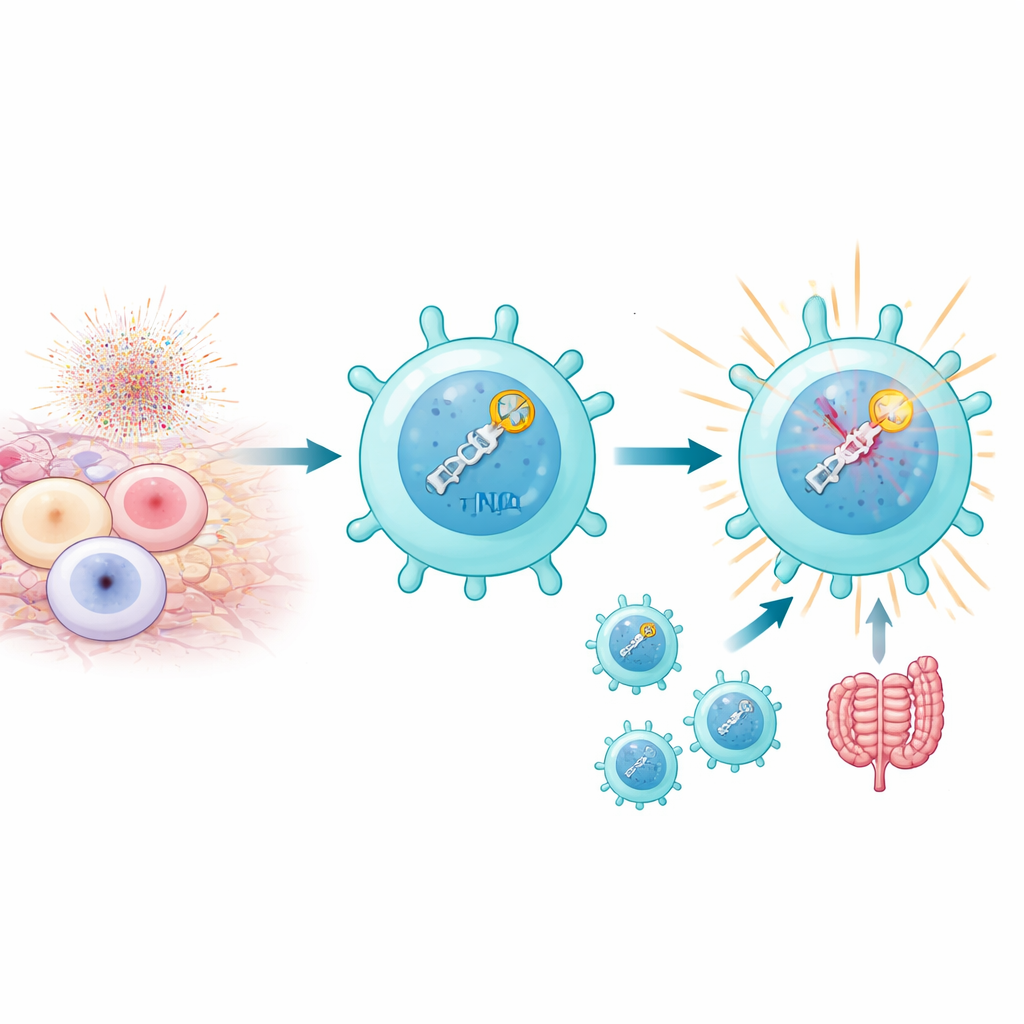
Sensoren der Reparatur, nicht die Reparatur selbst, treiben Schaden
NHEJ ist ein mehrstufiger Prozess, der mit Sensorproteinen (KU70 und KU80) beginnt, die gebrochene DNA‑Enden greifen und ein großes Enzym, DNA‑PKcs, anziehen, das wiederum Ligase‑Proteine zur Versiegelung des Bruchs rekrutiert. Durch selektives Deaktivieren verschiedener Teile dieses Pfads in T‑Zellen zeigten die Forscher, dass die frühen Sensorschritte für die Pathogenität von Th17‑Zellen entscheidend sind, während der abschließende Ligaseschritt überraschenderweise entbehrlich ist. Das Ausschalten von KU80 oder DNA‑PKcs verringerte deutlich die Fähigkeit von Th17‑Zellen, entzündungsfördernde Moleküle wie IL‑17A, IL‑2 und GM‑CSF zu produzieren und Gewebeschäden in Mäusen zu verursachen. Im Gegensatz dazu hatte das Entfernen der DNA‑Ligase IV nur geringen Einfluss auf den Krankheitsverlauf, obwohl es die Zellproliferation beeinträchtigte. Diese Experimente deuten darauf hin, dass für Autoimmunität das Erkennen von DNA‑Brüchen entscheidend ist, nicht unbedingt deren Reparatur.
Ein DNA‑Reparaturenzym fungiert als Genverstärker
Bei genaueren Untersuchungen entdeckte das Team, dass DNA‑PKcs mehr tut, als an gebrochene DNA‑Enden zu sitzen. Sobald es durch die KU‑Sensoren aktiviert ist, modifiziert es sich chemisch an einer Region, die als PQR‑Cluster bezeichnet wird. In diesem Zustand kann DNA‑PKcs physisch an RORγt binden, den Master‑Transkriptionsfaktor, der Th17‑Zellen definiert. Diese Partnerschaft stabilisiert RORγt an der DNA in der Nähe von Effektor‑Genen und hält diese Chromatinregionen offen und zugänglich. Wurde DNA‑PKcs entfernt oder der PQR‑Cluster gezielt gelöscht, konnte RORγt Schlüsselstellen entzündlicher Gene nicht mehr effektiv besetzen, und Th17‑Zellen verloren einen Großteil ihrer Fähigkeit, Autoimmunität zu befeuern. In Mausmodellen entzündeten solche veränderten Zellen die Netzhaut nicht, obwohl sie andernorts im Immunsystem vorhanden waren. 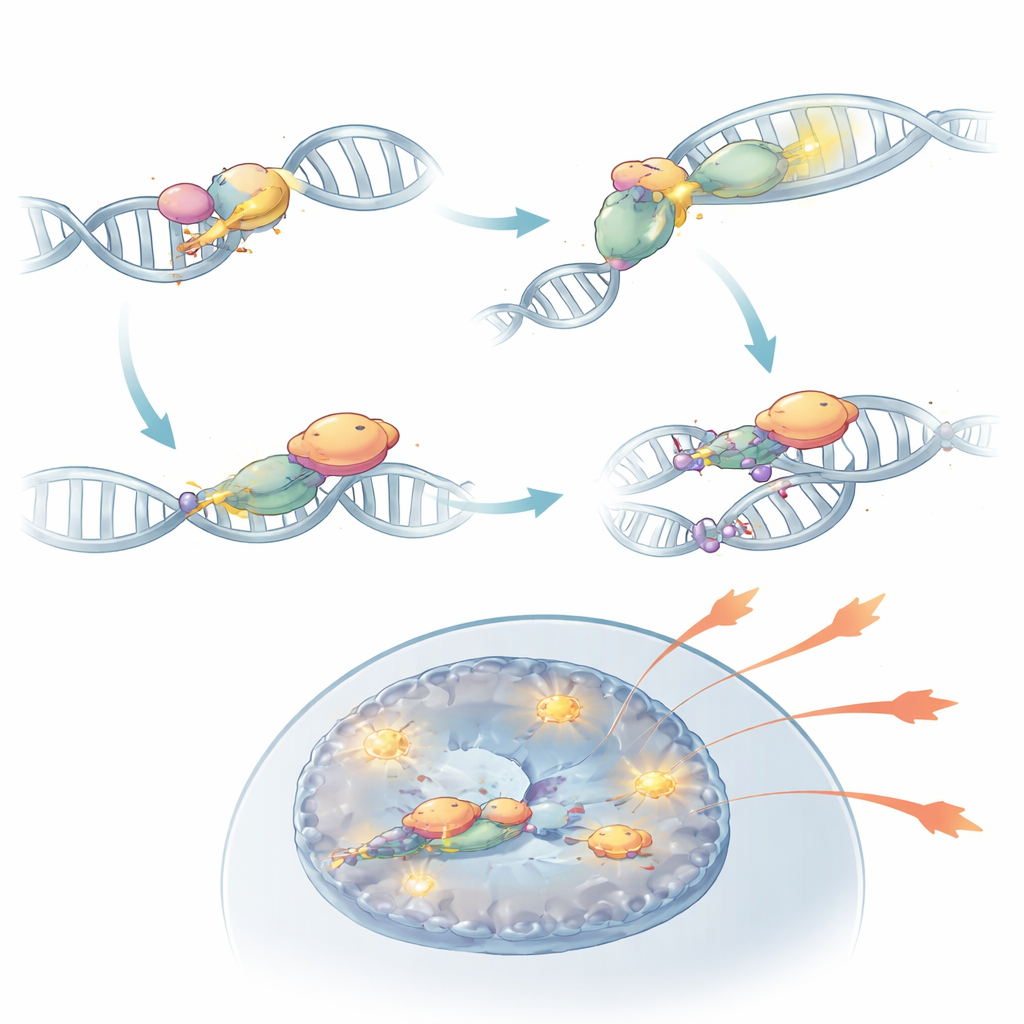
Ein Zytokinsignal, das Reparatur und Entzündung verstärkt
Die Studie verbindet dieses DNA‑Sensornetzwerk außerdem mit einem bekannten entzündlichen Botenstoff, dem Zytokin IL‑23. IL‑23 treibt Th17‑Zellen in einen schädlichen, gewebezerstörenden Zustand. Hier wurde gezeigt, dass IL‑23 die NHEJ‑Aktivität hochfährt, die Anhäufung von DNA‑Brüchen reduziert und die aktivierende Modifikation von DNA‑PKcs am PQR‑Ort fördert. Dieser Effekt hing vom IL‑23‑Rezeptor ab: Th17‑Zellen ohne Rezeptor konnten NHEJ nicht effizient aktivieren und akkumulierten mehr DNA‑Schäden. Durch groß angelegte Protein‑ und RNA‑Analysen identifizierten die Autoren ein zuvor unterschätztes Protein, IER2, als Brücke zwischen IL‑23‑Signalgebung und DNA‑PKcs. IL‑23 induziert IER2, das dann die Kinaseaktivität von DNA‑PKcs stärkt und so sowohl DNA‑Reparatur als auch die RORγt‑getriebene Expression entzündlicher Gene aufrechterhält.
Eine Hochrisiko‑Th17‑Subgruppe bei Patienten
Um diese Mechanismen mit menschlicher Krankheit zu verknüpfen, profilierten die Forscher Immunzellen von Patienten mit autoimmuner Uveitis in verschiedenen klinischen Stadien. Mithilfe der Einzelzell‑RNA‑Sequenzierung entdeckten sie eine Th17‑Subpopulation mit hohen Werten von IER2 und NHEJ‑bezogenen Genen, insbesondere Komponenten von DNA‑PKcs. Diese IER2‑reichen Th17‑Zellen waren am häufigsten bei Patienten mit aktiver, rezidivierender Erkrankung vorhanden und wiesen starke Signaturen von Stoffwechselaktivität, Signalgebung und Entzündung auf. Sie zeigten auch Marker effizienter DNA‑Reparatur mit weniger ungelösten DNA‑Brüchen. Computationale Analysen deuteten darauf hin, dass mit dem Fortschreiten von Th17‑Zellen entlang einer Entwicklungsachse hin zu höherer IER2‑Expression ihr entzündliches Potenzial parallel ansteigt, wodurch diese Subgruppe als wahrscheinlicher Treiber schwerer Autoimmunität markiert wird.
Ein schützendes System als therapeutisches Ziel
Insgesamt zeichnet die Arbeit das Bild eines DNA‑Reparatursensorsystems, das eigentlich das Genom schützen soll, das zugleich als Stellrad für gefährliche Immunantworten fungiert. Pathogene Th17‑Zellen nutzen NHEJ‑Erkennung, DNA‑PKcs‑Aktivierung und die IL‑23–IER2‑Achse, um RORγt zu stabilisieren und einen hochaktiven entzündlichen Zustand aufrechtzuerhalten, während sie DNA‑Schäden in Grenzen halten. Für Patientinnen und Patienten eröffnen sich dadurch neue therapeutische Ansätze: Statt das Immunsystem breit zu unterdrücken, könnten Medikamente, die gezielt die KU‑vermittelte Erkennung von DNA‑Brüchen, die Aktivierung von DNA‑PKcs am PQR‑Cluster oder die IER2–DNA‑PKcs‑Interaktion stören, die Pathogenität von Th17‑Zellen dämpfen und Autoimmunerkrankungen lindern, ohne die essenzielle DNA‑Reparatur in anderen Zellen vollständig zu blockieren.
Zitation: Chen, GY., Zhu, WJ., Li, Z. et al. Sensing of DNA double-strand breaks by the NHEJ system stabilizes RORγt transcriptional activity and shapes Th17 pathogenicity in autoimmunity. Cell Res 36, 340–358 (2026). https://doi.org/10.1038/s41422-025-01204-6
Schlüsselwörter: Th17-Zellen, DNA-Reparatur, Autoimmunität, DNA-PKcs, IL-23-Signalgebung