Clear Sky Science · ja
二本鎖DNA切断のNHEJシステムによる検知はRORγtの転写活性を安定化させ、自己免疫におけるTh17の病原性を形作る
DNA修復が友軍の誤射を病へと変えるとき
私たちの免疫系は感染と戦うためにT細胞に依存していますが、時にこれらの防御担当が暴走して自己の組織を攻撃し、眼のぶどう膜炎や炎症性腸疾患といった自己免疫疾患を引き起こします。本研究は意外なひねりを示します。通常は細胞を損傷から守るDNA修復システムが、ときにある種の攻撃的な免疫細胞の隠れたアクセルとなり、損傷を防ぐどころか慢性炎症を助長することがあるのです。
隠れたアラーム信号としてのDNA損傷
T細胞が強く活性化されると、特に自己抗原に反応する自己免疫環境では、ミトコンドリアが活性酸素種を大量に産生し、これがDNAの二本鎖切断を引き起こします。通常、これらの切断が過剰であれば細胞は死に至ります。しかし著者らは、病原性を持つTh17細胞の一部はこのストレスを生き延びるだけでなく、それを利用していることを発見しました。これらの細胞は非相同末端結合(NHEJ)として知られるDNA修復経路を高レベルで備えており、切断を迅速に検知して応答します。これは単にDNAをつなぐ話ではなく、切断の検知そのものがTh17細胞を炎症性かつ病原性のあるプログラムへと導く要素になっているようで、マウスの自己免疫性ぶどう膜炎や大腸炎のモデルで特に明らかでした。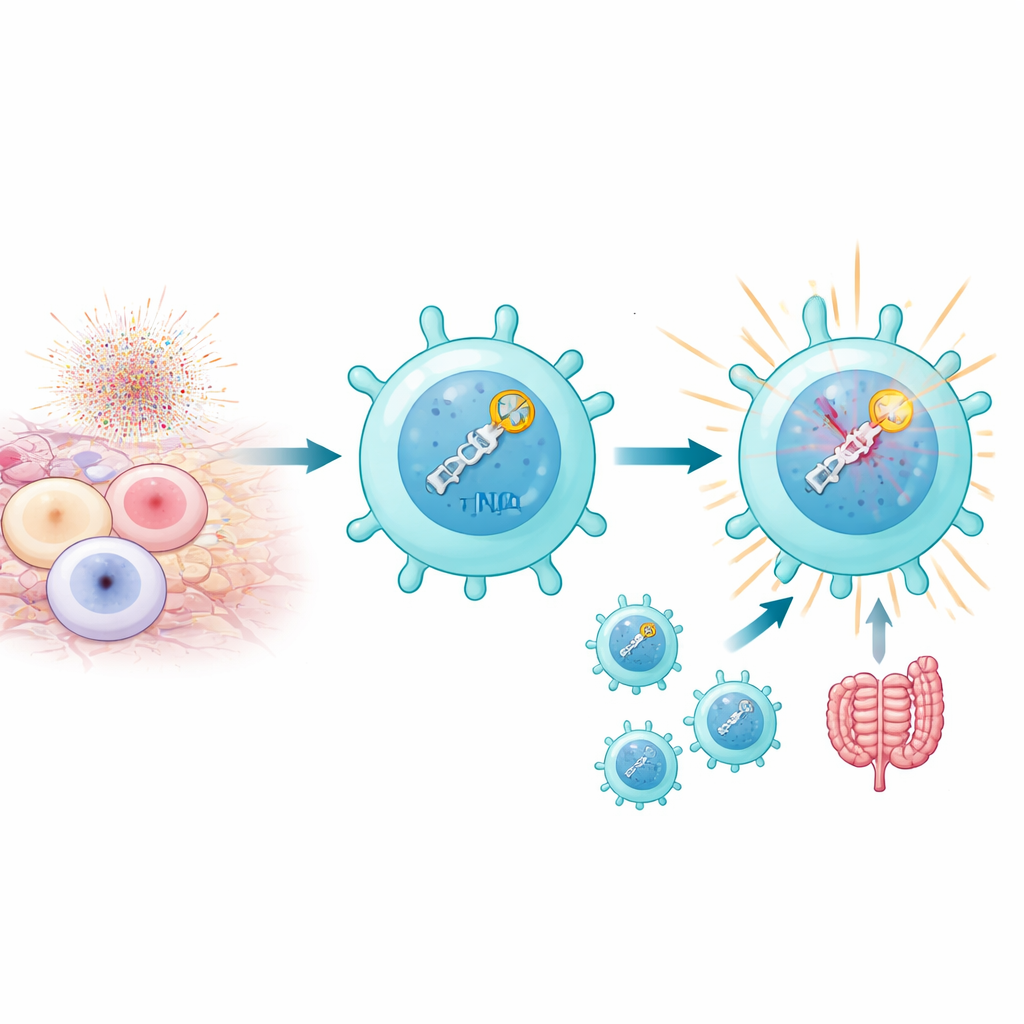
修復ではなくセンサーが害を駆動する
NHEJは多段階の過程で、まずセンサープロテイン(KU70およびKU80)が切れたDNA末端をとらえ、大きな酵素であるDNA-PKcsを呼び寄せ、さらにリガーゼ群が結合して断裂を密封します。研究者たちはT細胞でこの経路の異なる部分を選択的に無効化することで、初期の検知段階がTh17の病原性にとって決定的である一方、最終的なリガーション段階は驚くほど必須ではないことを示しました。KU80やDNA-PKcsをノックアウトすると、Th17細胞のIL-17A、IL-2、GM-CSFなどの炎症性分子の産生や、マウスにおける組織損傷を引き起こす能力が著しく低下しました。対照的に、DNAリガーゼIVを除去しても細胞増殖は阻害されたものの、疾患の抑制にはほとんど影響しませんでした。これらの実験は、自己免疫にとって本当に重要なのはDNA切断を“修復すること”ではなく、それを“検知する行為”であることを示唆しています。
遺伝子活性化装置としてのDNA修復酵素の副業
さらに掘り下げると、DNA-PKcsは壊れたDNA末端に存在するだけではないことが明らかになりました。KUセンサーによって活性化されると、DNA-PKcsはPQRクラスターと呼ばれる領域で化学修飾を受けます。この状態のDNA-PKcsはRORγt、すなわちTh17細胞を規定する主要な転写因子に物理的に結合できます。この結びつきにより、RORγtは効果分子の近くのDNAに安定してとどまり、該当するクロマチン領域を開いた状態に保ちます。DNA-PKcsを除去するかPQRクラスターを特異的に欠損させると、RORγtは重要な炎症遺伝子領域に効果的に占有できなくなり、Th17細胞は自己免疫を駆動する力を大いに失いました。マウスモデルでは、そのように変化した細胞は免疫系内には存在していても網膜を炎症化させることができませんでした。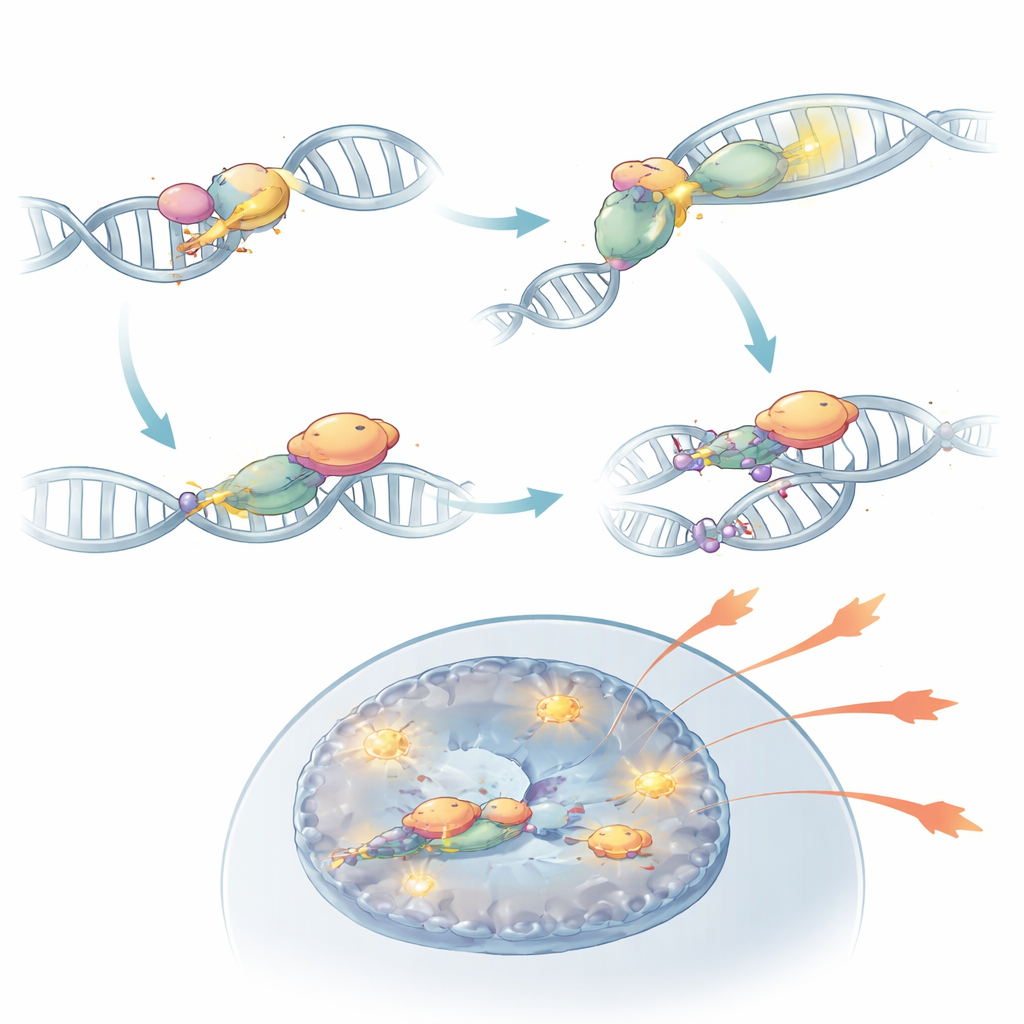
修復と炎症を促すサイトカインシグナル
本研究はまた、このDNA検知ネットワークをよく知られた炎症性メッセンジャーであるサイトカインIL-23と結びつけています。IL-23はTh17細胞を有害で組織を傷害する状態へ押しやることが知られていますが、本研究ではIL-23がNHEJ活性を高め、DNA切断の蓄積を減らし、DNA-PKcsのPQR部位の活性化修飾を促進することが示されました。この効果はIL-23受容体に依存しており、受容体を欠くTh17細胞は効率的にNHEJを活性化できず、より多くのDNA損傷を蓄積しました。大規模なタンパク質・RNA解析を通じて、著者らはIL-23シグナルとDNA-PKcsをつなぐ橋渡し役として、従来あまり注目されてこなかったタンパク質IER2を同定しました。IL-23はIER2を誘導し、IER2はDNA-PKcsのキナーゼ活性を高めて、DNA修復とRORγt駆動の炎症性遺伝子発現の両方を維持します。
患者に見られる高リスクのTh17サブセット
これらのメカニズムをヒト疾患に結びつけるために、研究者らは自己免疫性ぶどう膜炎の患者から臨床的に異なる段階の免疫細胞をプロファイリングしました。単一細胞RNAシーケンスを用いて、IER2およびNHEJ関連遺伝子、特にDNA-PKcs構成成分の高発現を示すTh17サブ集団を発見しました。これらのIER2高発現Th17細胞は、活動期や再発を繰り返す疾患を持つ患者に最も多く、代謝活性、シグナル伝達、炎症の強いシグネチャを示しました。また未解決のDNA切断が少なく、効率的なDNA修復のマーカーを帯びていました。計算解析は、Th17細胞がIER2発現の高い方向へ発達軌道をたどるにつれて、その炎症性ポテンシャルが並行して高まることを示唆しており、このサブセットが重篤な自己免疫の推進役である可能性を示しています。
保護機構を治療標的へ変える
全体として、この研究はゲノムを守るためのDNA修復センサーシステムが、危険な免疫応答の制御ノブとして二重の役割を果たす様子を描き出しています。病原性Th17細胞はNHEJの検知、DNA-PKcsの活性化、IL-23–IER2軸を利用してRORγtを安定化し、高出力の炎症状態を維持しつつDNA損傷を抑えています。患者にとって重要なのは、免疫系を広く抑制するのではなく、KUによるDNA切断検知、PQRクラスターでのDNA-PKcs活性化、あるいはIER2–DNA-PKcs相互作用を選択的に妨げる薬剤が、他の細胞での必須なDNA修復を完全に阻害することなくTh17の病原性を和らげ、自己免疫疾患を鎮める新たな治療の角度を提供する可能性があることです。
引用: Chen, GY., Zhu, WJ., Li, Z. et al. Sensing of DNA double-strand breaks by the NHEJ system stabilizes RORγt transcriptional activity and shapes Th17 pathogenicity in autoimmunity. Cell Res 36, 340–358 (2026). https://doi.org/10.1038/s41422-025-01204-6
キーワード: Th17細胞, DNA修復, 自己免疫, DNA-PKcs, IL-23シグナル伝達