Clear Sky Science · ru
Обнаружение двуцепочечных разрывов ДНК системой NHEJ стабилизирует транскрипционную активность RORγt и формирует патогенность Th17-клеток при аутоиммунных заболеваниях
Когда репарация ДНК превращает дружественный огонь в болезнь
Наша иммунная система опирается на Т-клетки для защиты от инфекций, но иногда эти защитники выходят из-под контроля и атакуют собственный организм, вызывая аутоиммунные заболевания, такие как увеит или воспалительные заболевания кишечника. В этом исследовании обнаруживается неожиданный поворот: система репарации ДНК, которая обычно защищает клетки от повреждений, может также выступать скрытым ускорителем особенно агрессивного типа иммунных клеток, способствуя хроническому воспалению вместо предотвращения вреда.
Повреждение ДНК как скрытая сигнализация тревоги
Когда Т-клетки сильно активируются, особенно в ответ на собственные антигены при аутоиммунных состояниях, их митохондрии генерируют вспышки реактивных форм кислорода, которые могут привести к двуцепочечным разрывам ДНК. Обычно слишком большое число таких разрывов смертельно. Тем не менее авторы обнаружили, что подмножество, называемое патогенными Th17-клетками, не только выживает при этом стрессе, но и использует его в своих интересах. Эти клетки обладают высоким уровнем активности пути репарации ДНК, известного как негомологичное соединение концов (NHEJ), который быстро обнаруживает разрывы и реагирует. Речь идет не только о заделывании ДНК: само обнаружение разрывов, по-видимому, вовлечено в программу, которая делает Th17-клетки провоспалительными и вызывающими болезнь, особенно в мышиных моделях аутоиммунного увеита и колита. 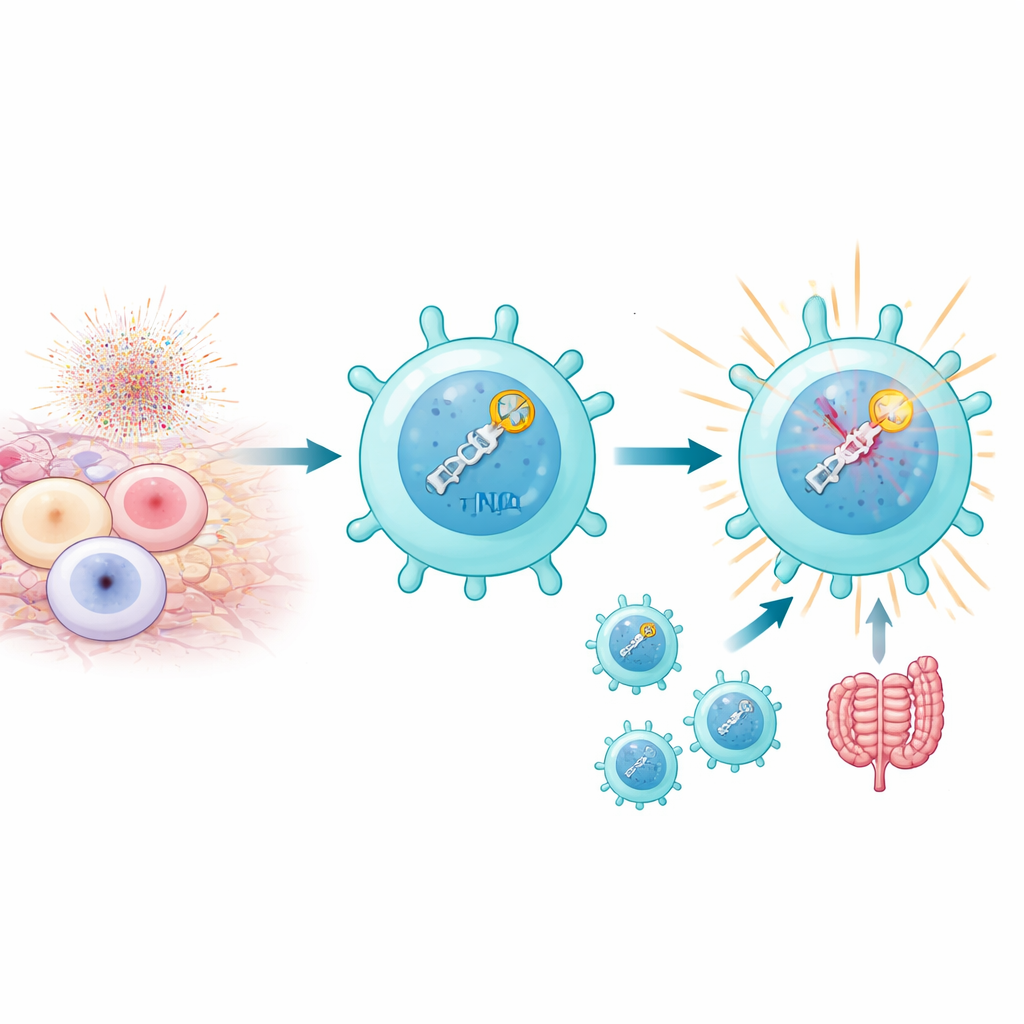
Датчики репарации, а не сама репарация, вызывают вред
NHEJ — это многоступенчатый процесс, начинающийся с белков-датчиков (KU70 и KU80), которые захватывают разорванные концы ДНК и привлекают большой фермент DNA-PKcs, который в свою очередь привлекает лигазы, запечатывающие разрыв. Селективно инактивировав разные части этого пути в Т-клетках, исследователи показали, что ранние этапы обнаружения имеют решающее значение для патогенности Th17, тогда как завершающий этап лигирования оказался, что удивительно, не столь важен. Удаление KU80 или DNA-PKcs резко снижало способность Th17-клеток продуцировать провоспалительные молекулы, такие как IL-17A, IL-2 и GM-CSF, и вызывать повреждение тканей у мышей. Напротив, удаление ДНК-лигазы IV мало ослабляло развитие болезни, хотя и нарушало пролиферацию клеток. Эти эксперименты указывают на то, что для аутоиммунитета важен сам акт обнаружения разрывов ДНК, а не обязательно их починка.
Фермент репарации ДНК, выполняющий роль усилителя генов
Углубляясь дальше, команда обнаружила, что DNA-PKcs делает больше, чем просто остается на разорванных концах ДНК. После активации датчиками KU он химически модифицируется в участке, называемом PQR-кластером. В этом состоянии DNA-PKcs может физически связываться с RORγt — главным транскрипционным фактором, определяющим Th17-клетки. Это партнерство стабилизирует RORγt на ДНК вблизи эффекторных генов и сохраняет эти области хроматина открытыми и доступными. Когда DNA-PKcs удаляли или когда специально удаляли его PQR-кластер, RORγt уже не мог эффективно занимать ключевые сайты воспалительных генов, и Th17-клетки теряли значительную часть своей способности подпитывать аутоиммунитет. В мышиных моделях такие модифицированные клетки не вызывали воспаления сетчатки, несмотря на то что присутствовали в иммунной системе. 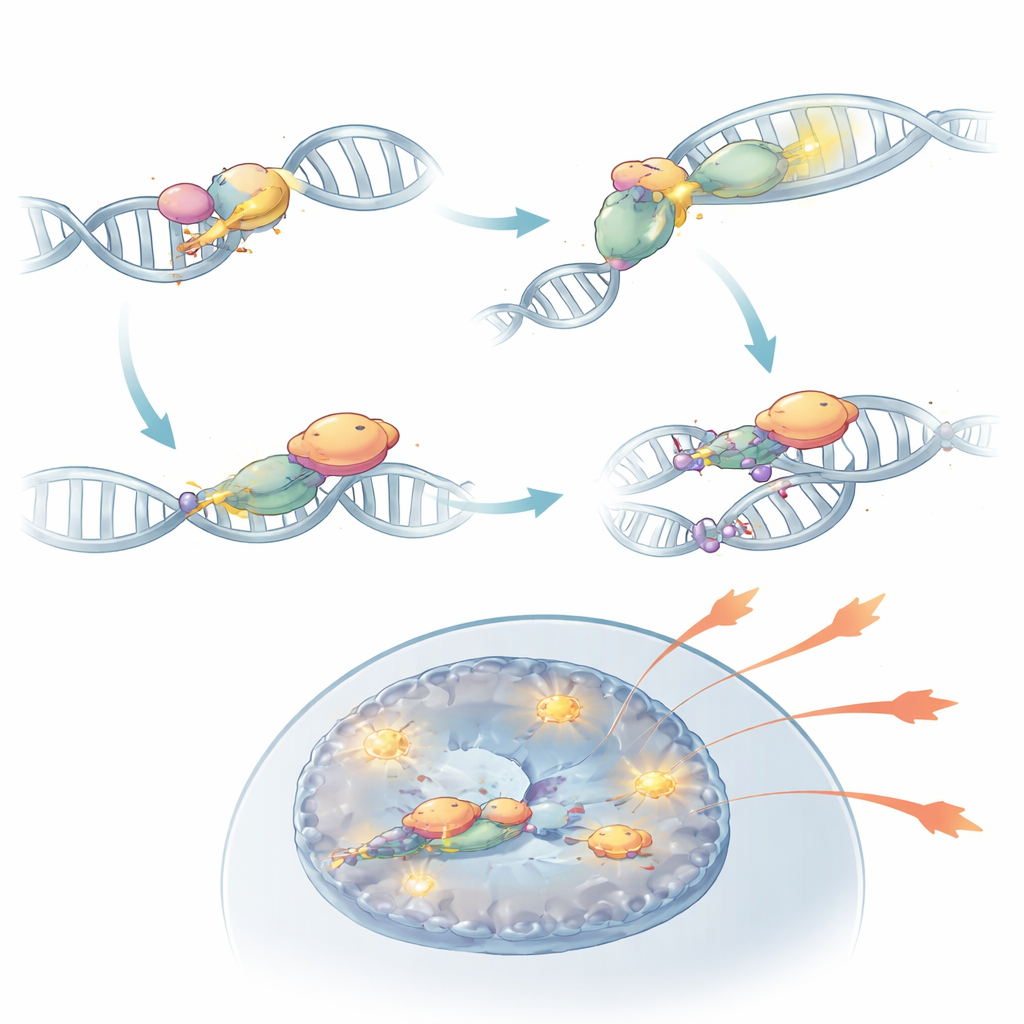
Сигнал цитокина, подпитывающий репарацию и воспаление
Исследование также связывает эту сеть обнаружения ДНК с хорошо известным провоспалительным мессенджером — цитокином IL-23. IL-23 известно, что он склоняет Th17-клетки в сторону вредоносного, разрушающего ткани состояния. Здесь показано, что IL-23 усиливает активность NHEJ, уменьшает накопление разрывов ДНК и повышает активирующую модификацию DNA-PKcs в PQR-участке. Этот эффект зависел от рецептора IL-23: Th17-клетки, лишенные рецептора, не могли эффективно активировать NHEJ и накапливали больше повреждений ДНК. С помощью крупномасштабного анализа белков и РНК авторы выявили ранее недооцененный белок IER2 как мост между сигнализацией IL-23 и DNA-PKcs. IL-23 индуцирует IER2, который затем усиливает киназную активность DNA-PKcs, поддерживая одновременно и репарацию ДНК, и RORγt-опосредованную экспрессию провоспалительных генов.
Высокорисковое подмножество Th17 у пациентов
Чтобы связать эти механизмы с человеческими заболеваниями, исследователи профилировали иммунные клетки пациентов с аутоиммунным увеитом на разных клинических стадиях. С помощью одноклеточного РНК-секвенирования они обнаружили подпопуляцию Th17 с высоким уровнем IER2 и генов, связанных с NHEJ, в частности компонентов DNA-PKcs. Эти Th17-клетки с высоким уровнем IER2 были наиболее многочисленны у пациентов с активным, рецидивирующим заболеванием и демонстрировали сильные признаки метаболической активности, сигнализации и воспаления. Они также несли маркеры эффективной репарации ДНК с меньшим числом неразрешенных разрывов. Вычислительный анализ предположил, что по мере развития Th17-клеток вдоль траектории дифференцировки и роста экспрессии IER2 их провоспалительный потенциал одновременно увеличивается, отмечая эту подгруппу как вероятный драйвер тяжёлого аутоиммунитета.
Превращение защитной системы в терапевтическую мишень
В целом работа рисует картину, в которой сенсорная система репарации ДНК — предназначенная для защиты генома — также выполняет роль регулятора опасных иммунных ответов. Патогенные Th17-клетки задействуют сенсинг NHEJ, активацию DNA-PKcs и ось IL-23–IER2 для стабилизации RORγt и поддержания высокого уровня провоспалительной активности, одновременно удерживая повреждения ДНК под контролем. Для пациентов это указывает на новые терапевтические подходы: вместо широкого подавления иммунной системы препараты, избирательно вмешивающиеся в KU-опосредованное обнаружение разрывов ДНК, активацию DNA-PKcs в PQR-кластере или взаимодействие IER2–DNA-PKcs, могли бы ослабить патогенность Th17 и унять аутоиммунное заболевание, не блокируя при этом полностью важную репарацию ДНК в других клетках.
Цитирование: Chen, GY., Zhu, WJ., Li, Z. et al. Sensing of DNA double-strand breaks by the NHEJ system stabilizes RORγt transcriptional activity and shapes Th17 pathogenicity in autoimmunity. Cell Res 36, 340–358 (2026). https://doi.org/10.1038/s41422-025-01204-6
Ключевые слова: Th17-клетки, репарация ДНК, аутоиммунитет, DNA-PKcs, сигнализация IL-23