Clear Sky Science · he
חישה של שברים כפולים ב-DNA על ידי מערכת NHEJ מייצבת את פעילות הטרנסקריפציה של RORγt ומעצבת את הפטוגניות של Th17 באוטואימוניות
כשמערכת תיקון ה-DNA הופכת אש ידידותית למחלה
מערכת החיסון שלנו מסתמכת על תאי T להדוף זיהומים, אך לעיתים המגינים האלה סטים מהמסלול ותוקפים את הגוף עצמו, וגורמים למחלות אוטואימוניות כמו דלקת הלחמית בעין או מחלות מעי דלקתיות. המחקר הזה חושף תפנית מפתיעה: מערכת תיקון DNA, שלרוב מגינה על התא מפגיעה, יכולה גם לשמש כמאיץ סמוי לסוג תאי חיסון אגרסיבי במיוחד, ובכך לתרום לדלקת כרונית במקום למנוע נזק.
נזק ל-DNA כאות אזעקה סמוי
כשתאי T מונעים בחוזקה, במיוחד על ידי אנטיגנים עצמייים בהקשרים אוטואימוניים, המיטוכונדריה שלהם מייצרת פרצי סוגי חמצן פעילים שיכולים לגרום לשברים כפולים ב-DNA. בדרך כלל, כמות גדולה של שברים כאלה היא קטלנית. עם זאת, המחברים גילו שתת‑אוכלוסייה שנקראת תאי Th17 פטוגניים לא רק שורדת את הלחץ הזה אלא מנצלת אותו לטובתה. תאים אלה נושאים רמות גבוהות של מסלול תיקון DNA הידוע כ-Non-Homologous End Joining (NHEJ), שמזהה במהירות שברים ומגיב. זה לא רק על מִרקַם ה‑DNA: עצם חישת השברים נראית כחלק מהתכנית שהופכת את תאי Th17 לדלקתיים ולגרמיים למחלות, במיוחד במודלי עכבר של דלקת לחמית אוטואימונית וקוליטיס. 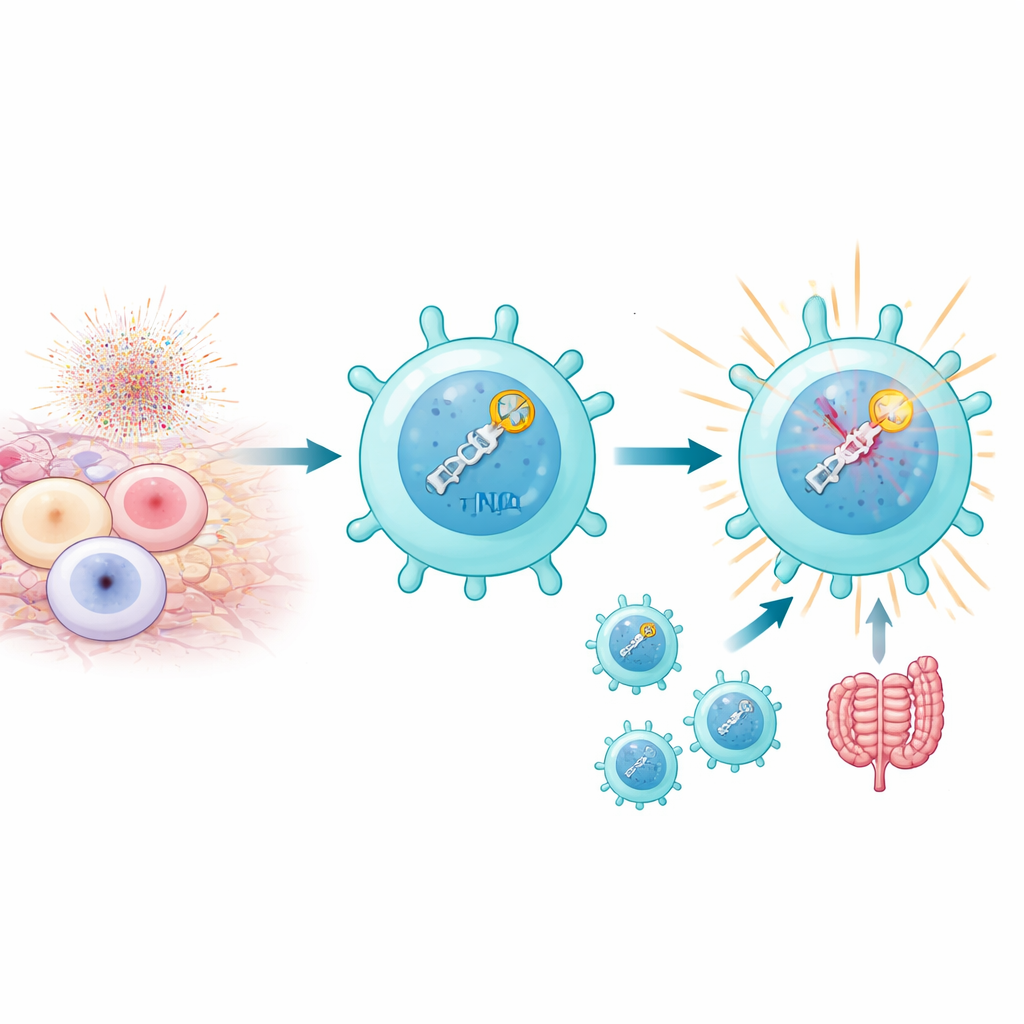
חיישני תיקון, לא התיקון עצמו, מניעים נזק
NHEJ הוא תהליך רב‑שלבי, שמתחיל בחלבוני חישה (KU70 ו-KU80) שתופסים קצוות DNA שבורים ומגייסים אנזים גדול, DNA-PKcs, שמביא בתורו חלבוני ליגאז שמאפסים את השבר. על ידי השבתה סלקטיבית של חלקים שונים מהמסלול בתאי T, החוקרים הראו שקווי החישה הראשוניים חשובים לפטוגניות של Th17, בעוד ששלב הליגציה הסופי מפתיע ואינו הכרחי. חיסול KU80 או DNA-PKcs קטע משמעותית את היכולת של תאי Th17 לייצר מולקולות דלקתיות כגון IL-17A, IL-2 ו-GM-CSF ולגרום לנזק רקמתי בעכברים. לעומת זאת, הסרת DNA ligase IV עשתה מעט כדי להפחית את המחלה, אף על פי שהשפיעה על התפשטות התאים. ניסויים אלה מרמזים שעל מה שבאמת חשוב באוטואימוניות הוא מעשה זיהוי שברי ה-DNA, ולא בהכרח תיקונם.
אנזים תיקון DNA כפונקציה משנית כמגביר גנטי
בהעמקה נוספת, הצוות גילה ש-DNA-PKcs עושה יותר מאשר לשבת על קצוות DNA שבורים. לאחר הפעלה על ידי חיישני KU, הוא משנה כימית את עצמו באזור שנקרא אשכול PQR. במצב זה, DNA-PKcs יכול להיקשר פיזית ל-RORγt, גורם השעתוק הראשי שמגדיר תאי Th17. שותפות זו מייצבת את RORγt על ה-DNA בקרבת גנים אפקטוריים ושומרת על אזורי הכרומטין פתוחים ונגישים. כאשר הסירו את DNA-PKcs, או כאשר מחקו ספציפית את אשכול ה-PQR שלו, RORγt כבר לא יכול לתפוס את אתרי הגנים הדלקתיים המרכזיים ביעילות, ותאי Th17 איבדו חלק גדול מיכולתם להניע אוטואימוניות. במודלי עכבר, תאים משונים כאלה לא הצליחו לדלק את הרשתית על אף נוכחותם במערכת החיסון. 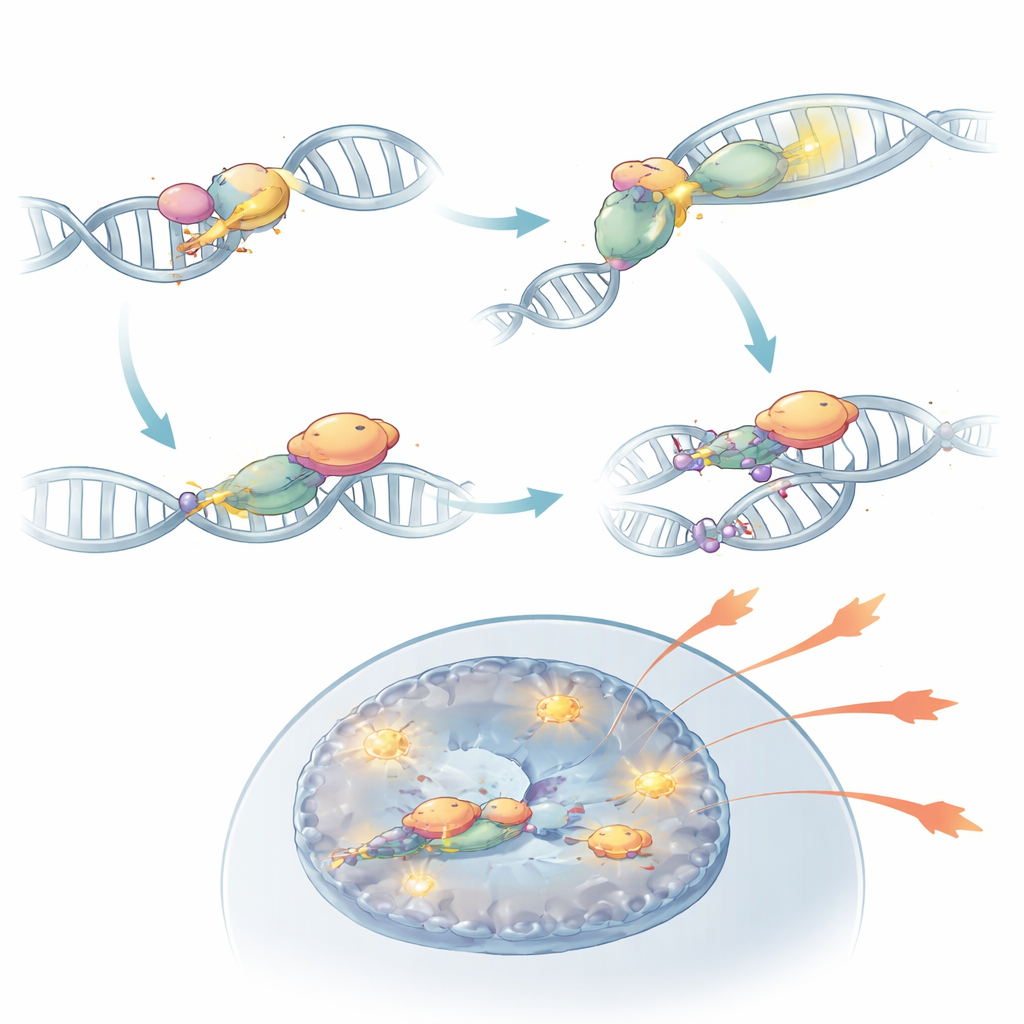
אות ציטוקיני שמזין תיקון ודלקת
המחקר מקשר גם את רשת חישת ה-DNA הזו למסר דלקתי ידוע, הציטוקין IL-23. ידוע ש-IL-23 דוחף את תאי Th17 למצב מזיק המזיק לרקמות. כאן הראו ש-IL-23 מגביר את פעילות NHEJ, מצמצם הצטברות שברי DNA ומעצים את המודיפיקציה המפעילה של DNA-PKcs באתר ה-PQR. ההשפעה הזו היתה תלויית רצפטור IL-23: תאי Th17 חסרי הרצפטור לא יכלו להפעיל ביעילות את NHEJ והצטברו בהם יותר נזקי DNA. באמצעות ניתוחים רחבי-היקף של חלבונים ו-RNA, זיהו המחברים חלבון שעד כה לא הוערך כראוי, IER2, כגשר בין איתות IL-23 ו-DNA-PKcs. IL-23 מסיט ביטוי של IER2, ולאחריו IER2 מחזקת את פעילות הקינאז של DNA-PKcs, מה שמקיים הן את תיקון ה-DNA והן את ביטוי הגנים הדלקתיים המנוהל על ידי RORγt.
תת‑אוכלוסיית Th17 בסיכון גבוה אצל מטופלים
כדי לקשר את המנגנונים הללו למחלה אנושית, החוקרים פרופיילו תאי חיסון ממטופלים עם דלקת לחמית אוטואימונית בשלבים קליניים שונים. באמצעות רצף RNA חד‑תאי הם גילו תת‑אוכלוסיית Th17 עם רמות גבוהות של IER2 וגנים הקשורים ל-NHEJ, במיוחד רכיבי DNA-PKcs. תאי Th17 עם IER2 גבוהים אלה היו השכיחים ביותר במטופלים עם מחלה פעילה וחוזרת והציגו חתימות חזקות של פעילות מטבולית, איתות ודלקת. כמו כן נשאו סמנים של תיקון DNA יעיל עם פחות שברים בלתי פתורים. ניתוח חישובי רמז שכאשר תאי Th17 מתקדמים לאורך מסלול התפתחותי לכיוון ביטוי IER2 גבוה יותר, הפוטנציאל הדלקתי שלהם עולה במקביל, וסימון תת‑האוכלוסייה הזו כגורם סביר לדרייב משמעותי של אוטואימוניות חמורה.
הפיכת מערכת מגוננת למטרה טיפולית
בסך הכל, העבודה מציירת תמונה שבה מערכת חיישני תיקון DNA—שנועדה להגן על הגנום—משמשת גם ככפתור בקרה לתגובות חיסוניות מסוכנות. תאי Th17 פטוגניים מנצלים חישת NHEJ, הפעלת DNA-PKcs וציר IL-23–IER2 כדי לייצב את RORγt ולשמור על מצב דלקתי חזק תוך שמירה על נזקי DNA תחת שליטה. עבור מטופלים, זה מצביע על זוויות טיפוליות חדשות: במקום לדכא את המערכת החיסונית באופן גורף, תרופות המתערבות סלקטיבית בחישת שברי DNA בתיווך KU, בהפעלת DNA-PKcs באשכול PQR, או באינטראקציה בין IER2 ל-DNA-PKcs עשויות להפחית את הפטוגניות של Th17 ולהרגיע מחלות אוטואימוניות בלי לחסום לחלוטין תיקון DNA חיוני בתאים אחרים.
ציטוט: Chen, GY., Zhu, WJ., Li, Z. et al. Sensing of DNA double-strand breaks by the NHEJ system stabilizes RORγt transcriptional activity and shapes Th17 pathogenicity in autoimmunity. Cell Res 36, 340–358 (2026). https://doi.org/10.1038/s41422-025-01204-6
מילות מפתח: תאי Th17, תיקון DNA, אוטואימוניות, DNA-PKcs, אותות IL-23