Clear Sky Science · ar
استشعار كسور مزدوجة السلسلة في الحمض النووي بواسطة نظام NHEJ يثبت نشاط النسخ لـ RORγt ويشكّل ضراوة خلايا Th17 في أمراض المناعة الذاتية
عندما يتحول إصلاح الحمض النووي إلى «نيران صديقة» ممرضة للمرض
يعتمد جهازنا المناعي على الخلايا التائية لصدّ العدوى، لكن أحيانًا ينحرف هؤلاء المدافعون ويهاجمون الجسم نفسه، مسببين أمراضًا مناعية ذاتية مثل التهاب المشيمية في العين أو داء الأمعاء الالتهابي. تكشف هذه الدراسة مفاجأة: نظام إصلاح الحمض النووي الذي يحمي الخلايا عادة من الضرر يمكنه أيضًا أن يعمل كمسرّع خفي لنوع صارم من الخلايا المناعية، مساهماً في دفع الالتهاب المزمن عوضًا عن منع الضرر.
ضرر الحمض النووي كإشارة إنذار مخفية
عندما تُنشَّط الخلايا التائية بقوة، وخاصة بواسطة مولدات الضد الذاتية في سياقات المناعة الذاتية، تنتج الميتوكوندريا موجات من أنواع الأكسجين التفاعلية التي قد تسبب كسورًا مزدوجة السلسلة في الحمض النووي. عادةً تكون الكميات الكبيرة من هذه الكسور قاتلة. ومع ذلك وجد الباحثون أن فئة تدعى خلايا Th17 الممرِضة لا تنجو من هذا الإجهاد فحسب، بل تستفيد منه أيضًا. هذه الخلايا تمتلك مستويات مرتفعة من مسار إصلاح يعرف باسم الربط غير المتجانس للنهايات (NHEJ)، الذي يستشعر الكسور بسرعة ويستجيب لها. الأمر لا يقتصر على رقع الحمض النووي: فاستشعار الكسور بحد ذاته يبدو أنه يتغذى على البرنامج الذي يجعل خلايا Th17 ملتهبة ومسببة للمرض، لا سيما في نماذج الفأر لالتهاب المشيمية المناعي والتهاب القولون. 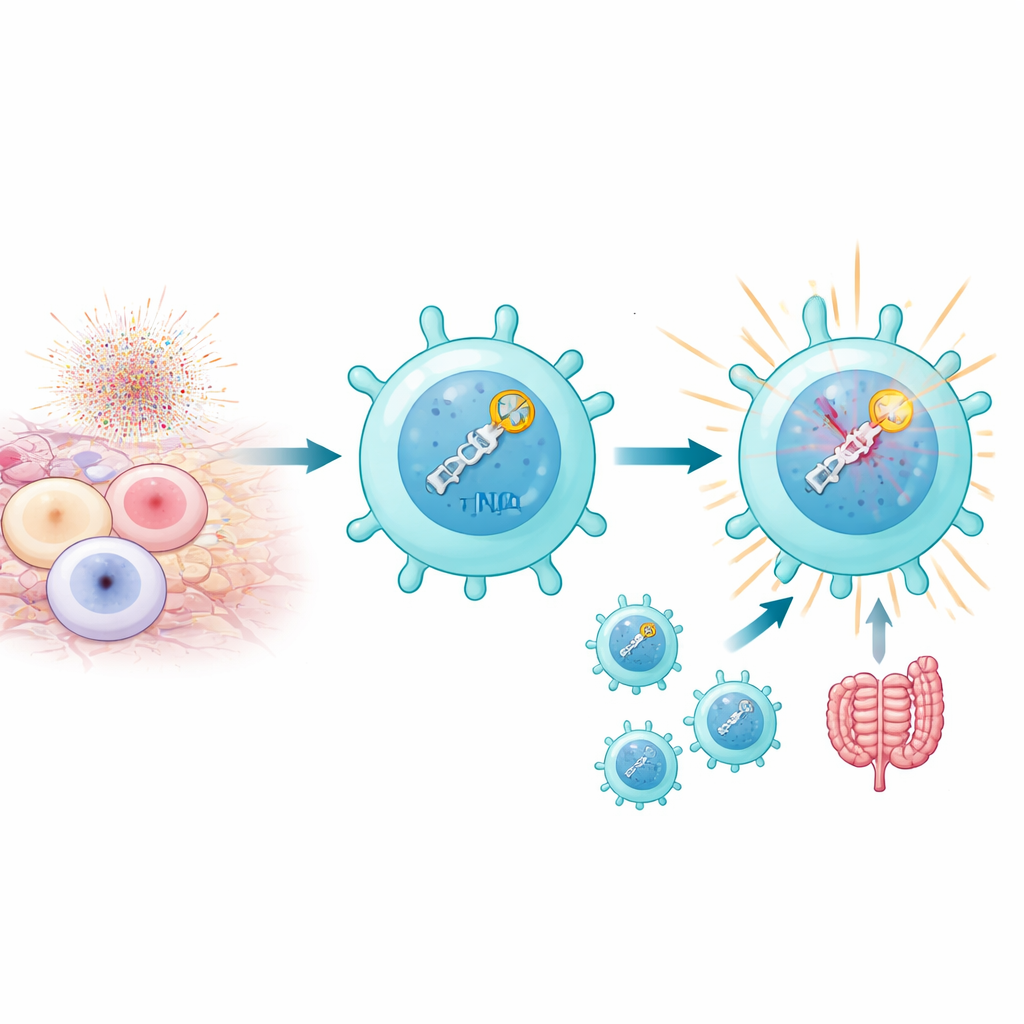
مستشعرات الإصلاح، وليس الإصلاح نفسه، هي المسببة للضرر
يُعد NHEJ عملية متعددة الخطوات، تبدأ ببروتينات استشعار (KU70 وKU80) التي تمسك نهايات الحمض النووي المكسورة وتستدعي إنزيمًا كبيرًا، DNA-PKcs، الذي يجلب بدوره بروتينات لايغاز تقوم بسد الفجوة. من خلال تعطيل أجزاء مختلفة من هذا المسار في الخلايا التائية بشكل انتقائي، أظهر الباحثون أن خطوات الاستشعار المبكرة حاسمة لضراوة Th17، بينما تبدو خطوة الربط النهائية غير ضرورية بشكل مدهش. أدى تعطيل KU80 أو DNA-PKcs إلى خفض حاد في قدرة خلايا Th17 على إنتاج جزيئات التهابية مثل IL-17A وIL-2 وGM-CSF وعلى إحداث تلف نسيجي في الفئران. بالمقابل، لم يؤدِ إزالة DNA ligase IV إلى تراجع كبير في المرض، رغم أنه أضعف تكاثر الخلايا. تشير هذه التجارب إلى أن ما يهم فعلاً في المناعة الذاتية هو فعل اكتشاف كسور الحمض النووي، لا بالضرورة إصلاحها.
إنزيم إصلاح الحمض النووي يؤدّي دورًا ثانويًا كمقوٍ للجينات
بتعمق أكثر، اكتشف الفريق أن DNA-PKcs يفعل أكثر من مجرد التواجد عند نهايات الحمض النووي المكسورة. بمجرد تنشيطه بواسطة مستشعرات KU، يقوم بتعديل نفسه كيميائيًا في منطقة تسمى كتلة PQR. في هذه الحالة، يمكن لـ DNA-PKcs أن يرتبط فعليًا بـ RORγt، عامل النسخ الرئيسي الذي يحدد خلايا Th17. هذا التعاون يثبت RORγt على الحمض النووي بالقرب من جينات المؤثرات ويحافظ على تلك المناطق من الكروماتين مفتوحة ومتاحة. عندما أزيل DNA-PKcs، أو عندما حُذفت كتلة PQR تحديدًا، عجز RORγt عن احتلال مواقع الجينات الالتهابية الأساسية بفاعلية، وفقدت خلايا Th17 جزءًا كبيرًا من قدرتها على تأجيج المناعة الذاتية. في نماذج الفأر، فشلت مثل هذه الخلايا المعدّلة في إحداث التهاب الشبكية رغم وجودها في الجهاز المناعي. 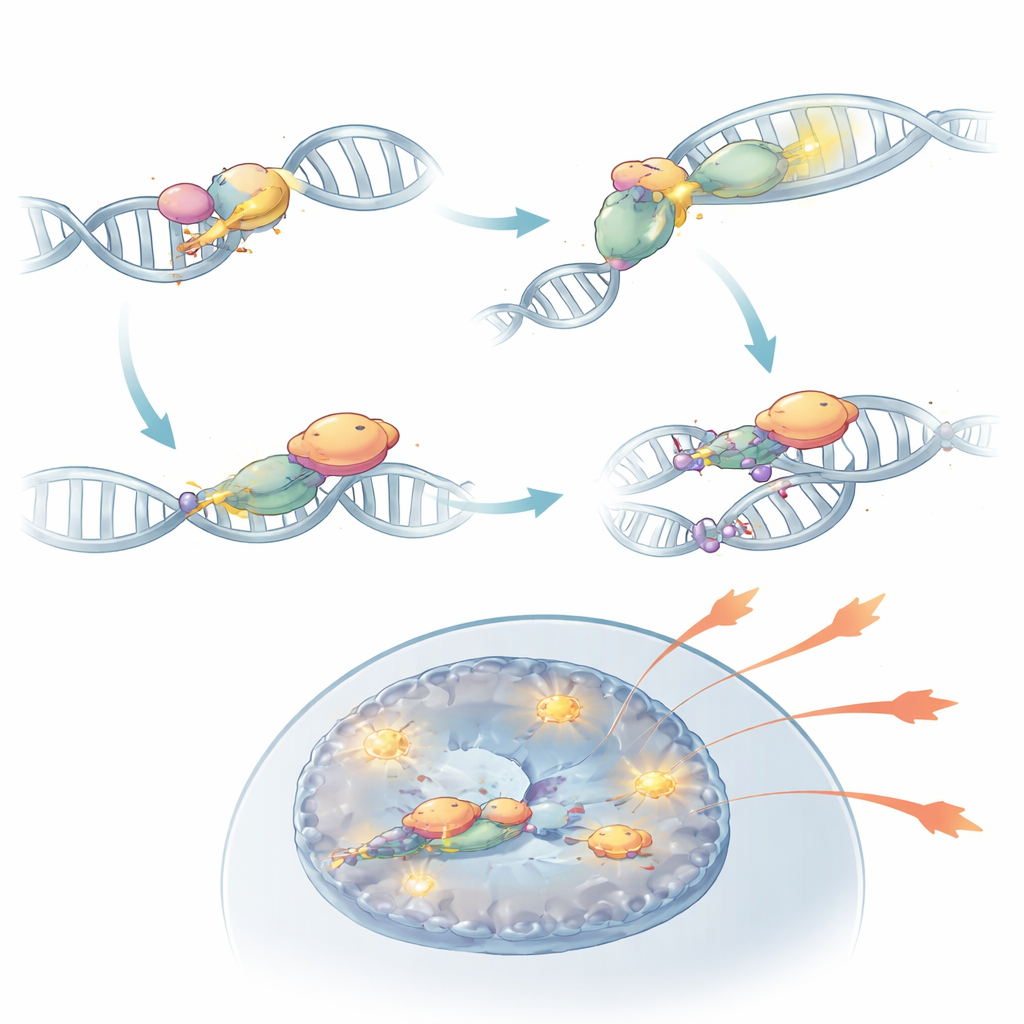
إشارة سيتوكين تغذي الإصلاح والالتهاب
ترتبط الدراسة أيضًا بشحنة إشارية معروفة بالالتهاب، السيتوكين IL-23. من المعروف أن IL-23 يدفع خلايا Th17 نحو حالة ضارة مدمرة للأنسجة. هنا، وُضح أن IL-23 يرفع نشاط NHEJ، ويقلل تراكم كسور الحمض النووي، ويعزز التعديل المنشط لـ DNA-PKcs عند موقع PQR. اعتمد هذا التأثير على مستقبل IL-23: فخلايا Th17 التي تفتقد المستقبل لم تستطع تنشيط NHEJ بكفاءة وتراكمت لديها المزيد من أضرار الحمض النووي. من خلال تحليلات بروتينية ومرئية للحمض النووي الريبوزي على نطاق واسع، حدد المؤلفون بروتينًا قلّما نُسجِل له اهتمامًا سابقًا، IER2، كجسر بين إشارة IL-23 وDNA-PKcs. يستحث IL-23 تعبير IER2، الذي يعزز بعد ذلك نشاط كيناز DNA-PKcs، محافظًا على كل من إصلاح الحمض النووي وتعبير الجينات الالتهابية المدفوع بـ RORγt.
تحت مجموعة Th17 عالية الخطورة لدى المرضى
لربط هذه الآليات بمرض الإنسان، حلل الباحثون خلايا مناعية من مرضى التهاب المشيمية المناعي في مراحل سريرية مختلفة. باستخدام تسلسل الرنا أحادي الخلية، كشفوا عن فئة فرعية من Th17 بمستويات مرتفعة من IER2 وجينات مرتبطة بـ NHEJ، لا سيما مكوّنات DNA-PKcs. كانت خلايا Th17 مرتفعة IER2 أكثر تواجدًا لدى المرضى ذوي المرض النشط والمتكرر وأظهرت توقيعات قوية لنشاط أيضي وإشاري وملائم التهابي. كما حملت علامات إصلاح حمض نووي فعّال مع عدد أقل من الكسور غير المحلولة. أشارت تحليلات حاسوبية إلى أنه كلما تقدمت خلايا Th17 على مسار تطوري نحو تعبير أعلى لـ IER2، ارتفعت قدرتها الالتهابية بالتوازي، مما يجعل هذه الفئة على الأرجح محركًا للمناعة الذاتية الشديدة.
تحويل نظام وقائي إلى هدف علاجي
بشكل عام، يرسم العمل صورة لنظام استشعار إصلاح الحمض النووي—المقصود به حماية الجينوم—يعمل أيضًا كمقبض تحكم للاستجابات المناعية الخطرة. تستغل خلايا Th17 الممرِضة استشعار NHEJ وتنشيط DNA-PKcs ومحور IL-23–IER2 لتثبيت RORγt والحفاظ على حالة التهابية ذات إنتاج مرتفع مع الحفاظ على ضرر الحمض النووي تحت السيطرة. للمرضى، يقترح هذا اتجاهات علاجية جديدة: بدلاً من كبح الجهاز المناعي بشكل شامل، قد تُخفّض الأدوية التي تتدخل انتقائيًا في استشعار كسور الحمض النووي عبر KU أو تنشيط DNA-PKcs عند كتلة PQR أو التفاعل بين IER2 وDNA-PKcs ضراوة Th17 وتهدئ الأمراض المناعية الذاتية دون إعاقة إصلاح الحمض النووي الأساسي في خلايا أخرى.
الاستشهاد: Chen, GY., Zhu, WJ., Li, Z. et al. Sensing of DNA double-strand breaks by the NHEJ system stabilizes RORγt transcriptional activity and shapes Th17 pathogenicity in autoimmunity. Cell Res 36, 340–358 (2026). https://doi.org/10.1038/s41422-025-01204-6
الكلمات المفتاحية: خلايا Th17, إصلاح الحمض النووي, المناعة الذاتية, DNA-PKcs, إشارة IL-23