Clear Sky Science · tr
Liver kinaz B1, redoks homeostazını düzenleyerek doğal öldürücü hücrelerin hayatta kalmasını sağlar
Neden Bağışıklığımızın “İlk Müdahale Ekibinin” de Korunmaya İhtiyacı Var
Doğal öldürücü (NK) hücreler, diğer bağışıklık gücü gelmeden önce virüsle enfekte olmuş ve kanserleşmiş hücreleri denetleyen hızlı yanıt askerleridir. Bu çalışma, görünüşte basit ama sonuçları büyük olan bir soruyu sorguluyor: bu güçlü hücreleri ihtiyaç duyulana kadar sağlıklı ve dengede tutan iç güvenlik sistemi nedir ve o sistem çöktüğünde ne olur? Karaciğer kinaz B1 (Lkb1) adlı tek bir proteinin NK hücrelerini içsel kimyasal hasardan nasıl koruduğunu ortaya koyarak, bu kritik savunucuları tükenmeden erken kanser gözetimini güçlendirmenin yeni yollarına işaret ediyor.
Bağışıklık Hücrelerinin İçindeki Bir Koruyucu Anahtar
NK hücreleri ince bir çizgide yürümek zorunda. Harekete geçecek kadar enerjiye ihtiyaçları var, ama aşırı aktif, tükenmiş veya ölür hâle gelmeyecek kadar da sakin olmalılar. Yazarlar, Lkb1’in NK hücrelerinin sessiz ve hazır bir durumda kalmasına yardımcı olan kilit bir iç “koruyucu anahtar” işlevi gördüğünü gösteriyor. Birkaç mühendislik fare modeli kullanarak, NK hücrelerinin farklı gelişim aşamalarında Lkb1’i seçici olarak kaldırdılar. Nasıl yaparlarsa yapsınlar sonuç çarpıcıydı: birçok organda NK hücreleri nadirleşti, olgunlaşma aşamalarında takılı kaldılar ve normalde savaşmaya tam hazır olduklarını gösteren yüzey işaretlerini kaybettiler. Bu etkiler hücre‑özündü; yani sorunlar çevrelerinden değil, doğrudan NK hücrelerinin içinden kaynaklanıyordu.
Hücresel Temizlik Bozulduğunda
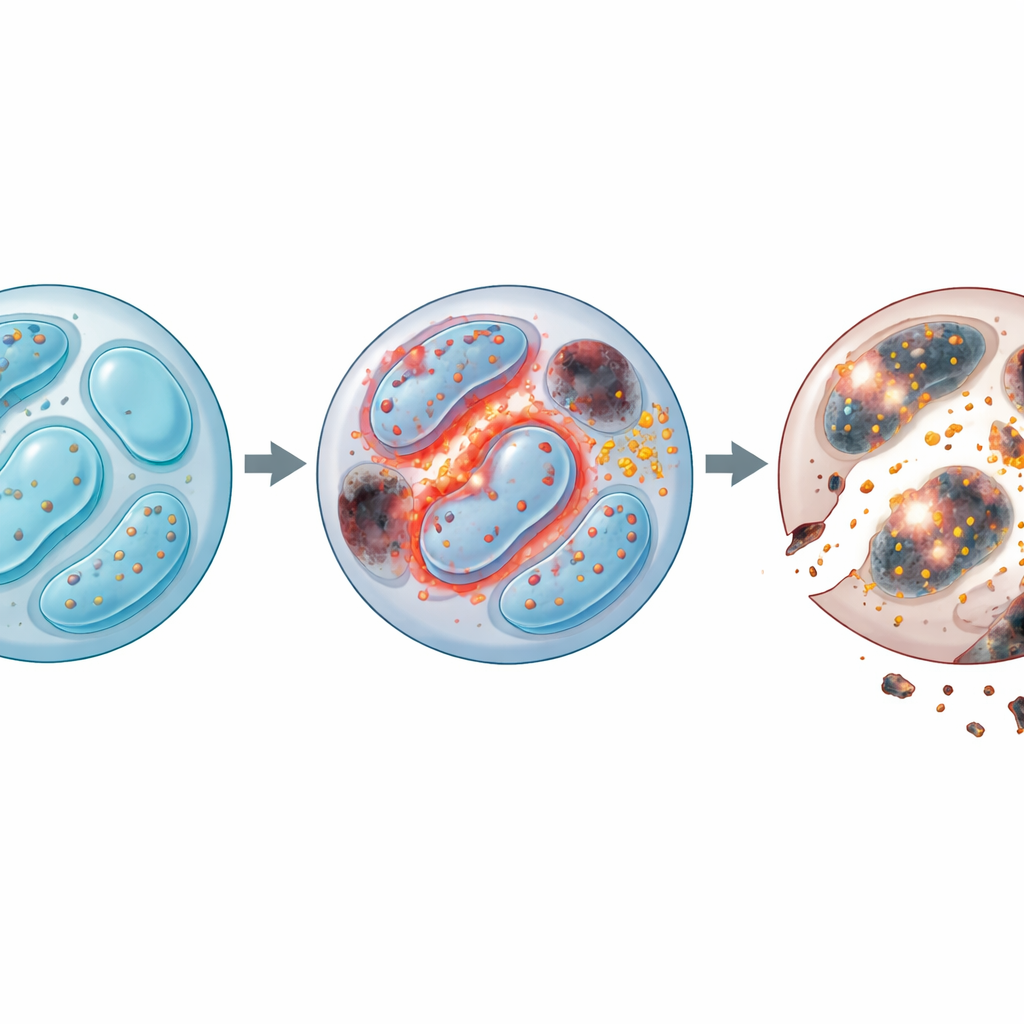
Daha derine indiklerinde, Lkb1 yokken hangi genlerin değiştiğini incelediler. Enerji kullanımı, hücre bölünmesi, atık geri dönüşümü ve hücre ölümü ile ilişkili binlerce gen değişmişti. Özellikle, Lkb1’siz NK hücrelerinde hücrenin eskimiş parçaları, örn. hasarlı mitokondriler, temizleyen otonomi (otofaji) sisteminde bir çöküş gözlendi. Normal koşullarda bu temizlik zararlı yan ürünlerin birikmesini önler. Lkb1 yokken otofaji tıkandı: hücreler anormal yüksek membran potansiyeline sahip fazladan mitokondri biriktirdi ve bu kusurlu yapılar büyük miktarda reaktif oksijen türleri (ROS) saçtı — proteinlere, yağlara ve DNA’ya zarar verebilen kararsız moleküller. Lkb1 eksik NK hücreleri daha fazla bölünerek telafi etmeye çalışsa da daha yüksek oranda öldüler; hayatta kalmanın, büyümenin değil, temel sorun olduğunu gösterdiler.
Demir Aşırı Yüklenmesi ve Çifte Hücre Ölümü Darbesi
Sorun ROS ile sınırlı kalmadı. Araştırmacılar, Lkb1’i eksik NK hücrelerinin demir dengesini de kaybettiklerini buldular. Bu hücreler demiri depoladı ve ana demir alma reseptörünü artırdı; bu da hücre zarlarına saldıran toksik “lipid ROS” oluşumunu körükledi. Bu desen, demire bağlı bir hücre ölümü türü olan ferroptozisi andırıyor. Hücreleri demiri bağlayan bir ilaç veya ferroptozis engelleyicisiyle tedavi ederek hayatta kalma kusurunun büyük bir kısmı düzeltilebildi. Aynı zamanda klasik programlı hücre ölümü yolları da aşırı aktiftir: koruyucu proteinler azaldı, cell‑execution enzimleri arttı ve apoptozu tetikleyen kaspazların engellenmesi hücre canlılığını iyileştirdi. Demiri uzaklaştırma ile kaspaz inhibisyonunu birleştirmek ek bir fayda sağladı; bu da Lkb1’siz NK hücrelerinin iki bağımsız ama birleşen ölüm yoluyla —demir kaynaklı membran hasarı ve mitokondri kaynaklı apoptoz— saldırıya uğradığını gösteriyor.
Tükenmiş Askerler ve Zayıflamış Tümör Devriyesi
Hayatta kalmanın ötesinde, NK hücrelerin etkili çalışması gerekiyor. Lkb1 eksik NK hücreleri ana savunma molekülü interferon‑γ’yi daha az üretti ve yüzeylerinde PD‑1 ve TIGIT gibi daha yüksek düzeyde inhibitör “frenler” gösterdi — kronik enfeksiyonlar ve kanserde görülen tükenmiş immün hücrelerle ilişkili özellikler. ROS’u azaltan veya ferroptozisi engelleyen antioksidan tedaviler bu tükenmişlik işaretlerini düşürdü ve NK hücre aktivitesini kısmen geri getirdi. Canlı farelerde sonuçlar açıktı: NK hücrelerinde Lkb1 olmayan hayvanlar normal “kendini” sinyali eksik hücreleri reddetmede çok daha başarısızdı ve NK‑duyarlı tümör hücrelerini temizlemede veya melanomanın akciğerlere yayılmasını önlemede daha az yetenekliydi. Lkb1’i NK hücresi gelişiminin daha erken safhalarında kaldırmak daha da şiddetli başarısızlıklara yol açtı; bu da onun en erken aşamalardan itibaren önemini vurguluyor.
Gelecek Tedaviler İçin Anlamı
Birçok kişi için Lkb1 kanser hücrelerinde bir tümör‑baskılayıcı protein olarak daha çok bilinir, ancak bu çalışma bunun bağışıklık hücreleri içindeki aynı derecede kritik rolünü vurguluyor. Lkb1, NK hücrelerini metabolik olarak dengede tutar, iç temizlik sistemlerini sürdürür, demir ve ROS aşırı yüklenmesini önler ve onları çift ölüm yolları ile tükenmeden korur. İlginç olarak, diğer hücrelerde Lkb1 ile ilişkilendirilen ortak enerji algılama yolları —AMPK aktivasyonu ve mTORC1 inhibisyonu— farmakolojik olarak değiştirilse bile hasarı düzeltemedi; bu da NK hücrelerinin farklı aşağı akış devrelerine dayandığını ima ediyor. Bir okuyucu için çıkarım şudur: NK hücrelerinin etkili kanser bekçileri olarak kalabilmeleri için oksidatif ve demir kaynaklı stresten korunmaya ihtiyacı var. Lkb1’i doğrudan değiştirmek kanser açısından risk taşıyabileceğinden, NK hücrelerinde redoks ve demir dengesini hassaslaştıran tedaviler, bir gün vücudun tümörlere karşı erken uyarı sistemini güçlendirmeye yardımcı olabilir.
Atıf: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Anahtar kelimeler: doğal öldürücü hücreler, LKB1, oksidatif stres, demir homeostazı, kanser immünosürveyansı