Clear Sky Science · es
La quinasa hepática B1 mantiene la supervivencia de las células asesinas naturales regulando la homeostasis redox
Por qué nuestros “primeros intervinientes” inmunitarios también necesitan protección
Las células asesinas naturales (NK) son los soldados de respuesta rápida del organismo, patrullando en busca de células infectadas por virus y cancerosas antes de que lleguen otras fuerzas inmunitarias. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿qué mantiene a estas poderosas células sanas y en calma hasta que se necesitan, y qué ocurre cuando ese sistema de seguridad interno falla? Al desvelar cómo una sola proteína, llamada quinasa hepática B1 (Lkb1), protege a las células NK del daño químico interno, el trabajo apunta a nuevas maneras de reforzar la vigilancia temprana contra el cáncer sin agotar a estos defensores cruciales.
Un interruptor guardián dentro de las células inmunitarias
Las células NK deben mantener un equilibrio delicado. Necesitan suficiente energía para entrar en acción, pero no tanta que se sobreactiven, se agoten o mueran. Los autores muestran que Lkb1 actúa como un “interruptor guardián” interno clave que ayuda a las células NK a permanecer en un estado silencioso y listo. Usando varios modelos de ratón modificados, eliminaron selectivamente Lkb1 de las células NK en distintas etapas de su desarrollo. Hiciera lo que hiciera, el resultado fue contundente: las células NK escasearon en muchos órganos, se quedaron atrapadas en estados inmaduros y perdieron los marcadores de superficie que normalmente señalan plena capacidad para combatir. Estos efectos fueron intrínsecos a las células, es decir, surgieron por problemas dentro de las propias NK y no por su entorno.
Cuando el mantenimiento celular se descompone
Al profundizar, el equipo examinó qué genes cambiaban cuando faltaba Lkb1. Miles de genes ligados al uso de energía, la división celular, el reciclaje de desechos y la muerte celular se alteraron. En particular, las NK sin Lkb1 mostraron una ruptura en la autofagia, el sistema de mantenimiento de la célula que elimina piezas desgastadas como mitocondrias dañadas. En condiciones normales, esta limpieza evita que se acumulen subproductos dañinos. Sin Lkb1, la autofagia se atascó: las células acumularon mitocondrias adicionales con potencial de membrana anormalmente alto, y estas estructuras defectuosas expulsaron grandes cantidades de especies reactivas de oxígeno (ROS), moléculas inestables que pueden dañar proteínas, lípidos y ADN. Aunque las NK deficitarias en Lkb1 intentaron compensar dividiéndose más, murieron a tasas superiores, revelando que la supervivencia, no el crecimiento, era el problema central.
Sobrecarga de hierro y un doble impacto de muerte celular
El problema no terminó con las ROS. Los investigadores hallaron que las NK sin Lkb1 también perdieron el control del equilibrio del hierro. Estas células acapararon hierro y aumentaron los niveles de un receptor clave de importación de hierro, lo que a su vez impulsó la formación de “ROS lipídicos” tóxicos que atacan las membranas celulares. Este patrón es característico de la ferroptosis, una forma de muerte celular dependiente del hierro. Al tratar las células con un fármaco quelante del hierro o con un bloqueador de la ferroptosis, el equipo pudo rescatar gran parte del defecto de supervivencia. Al mismo tiempo, las vías clásicas de muerte programada también estaban sobreactivas: las proteínas protectoras disminuyeron, las enzimas ejecutoras aumentaron, y bloquear las caspasas (las enzimas que impulsan la apoptosis) mejoró la viabilidad. Combinar la eliminación de hierro y la inhibición de caspasas dio un beneficio aditivo, indicando que las NK sin Lkb1 son golpeadas por dos vías de muerte independientes pero convergentes: daño de membrana impulsado por hierro y apoptosis impulsada por mitocondrias.
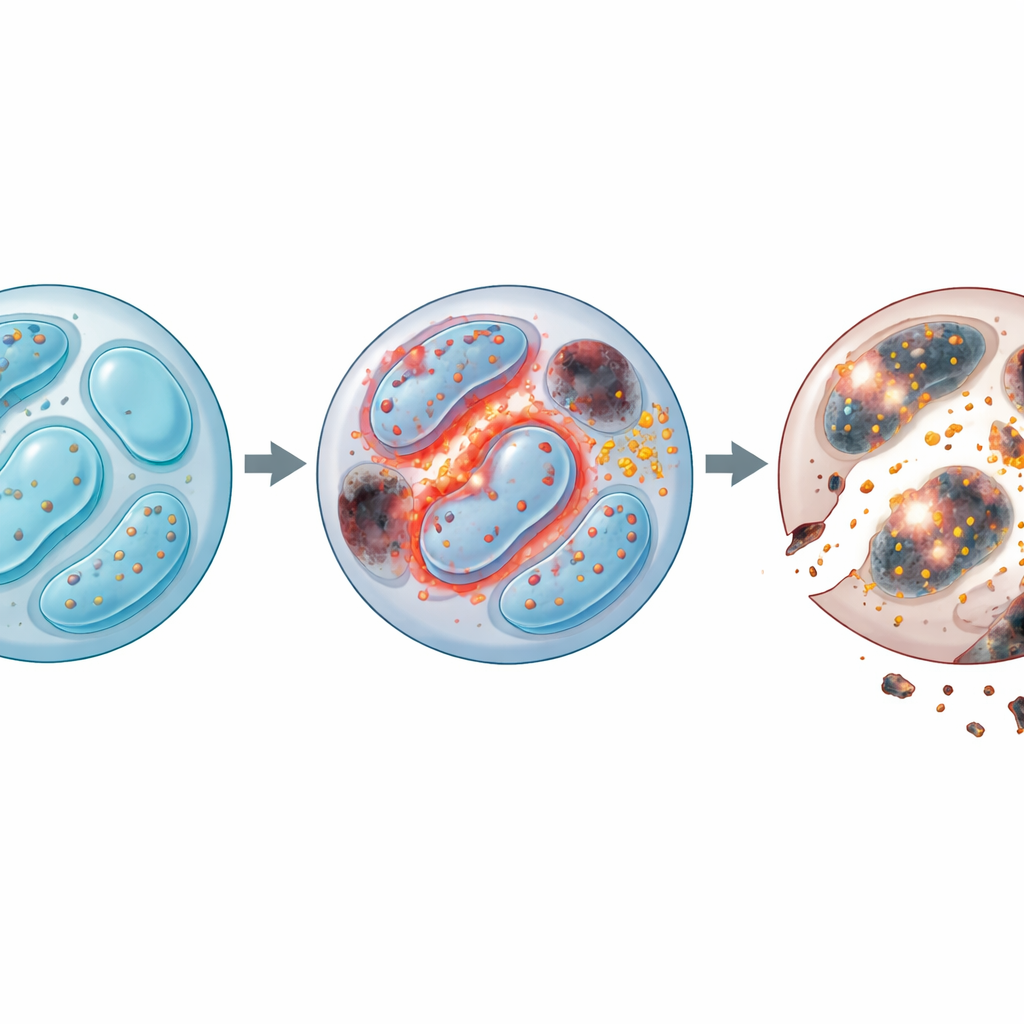
Soldados exhaustos y patrulla tumoral debilitada
Más allá de seguir vivas, las NK deben funcionar eficazmente. Las NK deficientes en Lkb1 produjeron menos de la molécula defensiva clave interferón-γ y mostraron niveles más altos de “frenos” inhibitorios en su superficie, como PD-1 y TIGIT, rasgos asociados con células inmunitarias agotadas que se observan en infecciones crónicas y cáncer. Tratamientos antioxidantes que redujeron las ROS o bloquearon la ferroptosis disminuyeron estos marcadores de agotamiento y restauraron parcialmente la actividad de las NK. En ratones vivos, las consecuencias fueron claras: los animales que carecían de Lkb1 en sus NK eran mucho peores rechazando células que carecían de señales normales de “propio” y menos capaces de eliminar células tumorales sensibles a NK o de prevenir la diseminación de melanoma a los pulmones. Eliminar Lkb1 en etapas más tempranas del desarrollo de las NK provocó fracasos aún más severos, subrayando su importancia desde las fases más iniciales.
Qué significa esto para futuras terapias
Para muchos, Lkb1 es más conocido como una proteína supresora de tumores en células cancerosas, pero este trabajo destaca su papel igualmente crítico dentro de las células inmunitarias. Lkb1 mantiene a las NK en equilibrio metabólico, sostiene sus sistemas internos de limpieza, evita la sobrecarga de hierro y ROS, y las protege de vías duales de muerte y del agotamiento. Curiosamente, las vías comunes de detección energética ligadas a Lkb1 en otras células—activación de AMPK e inhibición de mTORC1—no pudieron reparar el daño cuando se ajustaron farmacológicamente, lo que sugiere que las NK dependen de circuitos descendentes distintos. Para un lector no especializado, la conclusión es que las propias NK necesitan protección frente al estrés oxidativo y dependiente del hierro para seguir siendo centinelas efectivas contra el cáncer. En lugar de alterar directamente Lkb1, lo que podría conllevar riesgos oncológicos en otros tejidos, terapias que ajusten finamente el equilibrio redox y del hierro en las NK podrían algún día ayudar a reforzar el sistema de alerta temprana del organismo frente a los tumores.
Cita: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Palabras clave: células asesinas naturales, LKB1, estrés oxidativo, homeostasis del hierro, inmunovigilancia del cáncer