Clear Sky Science · pl
Kinaza wątroby B1 utrzymuje przeżycie komórek NK, regulując homeostazę redoks
Dlaczego nasi „pierwsi responderzy” układu odpornościowego też potrzebują ochrony
Komórki NK (natural killers) to szybkie oddziały obronne organizmu, patrolujące w poszukiwaniu komórek zakażonych wirusem i nowotworowych zanim pojawią się inne elementy odporności. Badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: co utrzymuje te potężne komórki w zdrowiu i spokoju aż do chwili potrzeby, i co się dzieje, gdy wewnętrzny system bezpieczeństwa zawiedzie? Odkrywając, jak pojedyncze białko, kinaza wątroby B1 (Lkb1), chroni komórki NK przed wewnętrznymi uszkodzeniami chemicznymi, praca ta wskazuje nowe sposoby wzmocnienia wczesnego nadzoru przeciwnowotworowego bez wypalania tych kluczowych obrońców.
Wewnętrzny przełącznik‑strażnik w komórkach odpornościowych
Komórki NK muszą poruszać się po cienkiej granicy. Potrzebują wystarczająco dużo energii, by natychmiast zareagować, ale nie tak dużo, by stać się nadaktywne, wyczerpane lub ginąć. Autorzy pokazują, że Lkb1 działa jako kluczowy wewnętrzny „przełącznik‑strażnik”, pomagający komórkom NK pozostawać w cichym, gotowym stanie. Na kilku zmodyfikowanych modelach mysich selektywnie usuwali Lkb1 z komórek NK na różnych etapach ich rozwoju. Bez względu na sposób, efekt był uderzający: komórki NK stały się rzadkie w wielu narządach, utknęły na niedojrzałych etapach i straciły markery powierzchniowe, które normalnie sygnalizują pełną gotowość do walki. Efekty te były wewnątrzkomórkowe — wynikały z problemów wewnątrz samych komórek NK, a nie z ich otoczenia.
Gdy wewnętrzne porządki komórkowe zawiodą
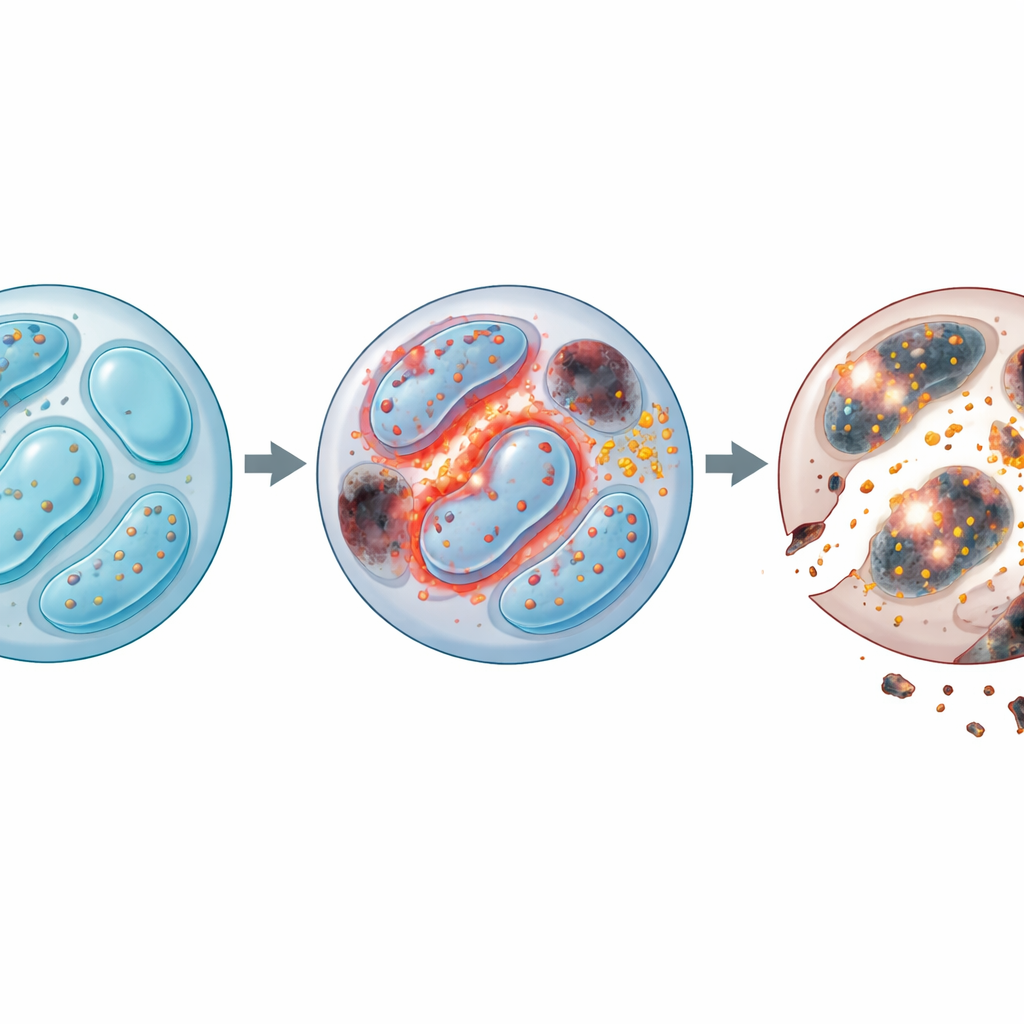
Pogłębiając analizę, zespół sprawdził, które geny zmieniały ekspresję po utracie Lkb1. Tysiące genów związanych z wykorzystaniem energii, podziałem komórek, recyklingiem odpadów i śmiercią komórkową uległo zmianom. W szczególności komórki NK pozbawione Lkb1 wykazywały zaburzenia autofagii — systemu porządkowego komórki, który usuwa zużyte elementy, takie jak uszkodzone mitochondria. W normalnych warunkach taki „sprzątanie” zapobiega nagromadzeniu szkodliwych produktów ubocznych. Bez Lkb1 autofagia zamarła: komórki gromadziły dodatkowe mitochondria o nienaturalnie wysokim potencjale błonowym, a te wadliwe struktury wydzielały duże ilości reaktywnych form tlenu (ROS) — niestabilnych cząsteczek, które mogą uszkadzać białka, lipidy i DNA. Mimo że komórki NK z defektem Lkb1 próbowały kompensować to przez częstsze dzielenie się, umierały w większych liczbach, co ujawniło, że zasadniczym problemem była przeżywalność, a nie wzrost.
Nadmiar żelaza i podwójny cios śmierci komórkowej
Problemy nie skończyły się na ROS. Badacze odkryli, że komórki NK pozbawione Lkb1 także straciły kontrolę nad równowagą żelaza. Komórki te magazynowały żelazo i zwiększały poziom kluczowego receptora importu żelaza, co z kolei napędzało powstawanie toksycznych „lipidowych ROS”, które atakują błony komórkowe. Ten wzorzec jest charakterystyczny dla ferroptozy — zależnej od żelaza formy śmierci komórki. Leczenie komórek lekiem wiążącym żelazo lub blokującym ferroptozę pozwalało uratować dużą część defektu przeżycia. Jednocześnie klasyczne szlaki zaprogramowanej śmierci komórkowej również były nadaktywne: poziomy białek ochronnych spadały, wzrastały enzymy wykonawcze, a blokowanie kaspaz (enzymów napędzających apoptozę) poprawiało przeżywalność. Połączenie usunięcia żelaza i zahamowania kaspaz dawało efekt addytywny, co wskazuje, że komórki NK bez Lkb1 są trafiane przez dwa niezależne, lecz zbieżne szlaki śmierci — uszkodzenie błon zależne od żelaza oraz apoptoza napędzana przez mitochondria.
Wyczerpane oddziały i osłabiony patrol przeciwnowotworowy
Ponadto komórki NK muszą nie tylko przetrwać, lecz także sprawnie działać. Komórki NK pozbawione Lkb1 wytwarzały mniej kluczowego czynnika obronnego interferonu-γ i wykazywały wyższy poziom hamujących „hamulców” na powierzchni, takich jak PD‑1 i TIGIT — cechy kojarzone z wyczerpaniem komórek odpornościowych obserwowanym w przewlekłych infekcjach i nowotworach. Terapie przeciwutleniające, które zmniejszały ROS lub blokowały ferroptozę, obniżały te markery wyczerpania i częściowo przywracały aktywność komórek NK. W żywych myszach skutki były wyraźne: zwierzęta pozbawione Lkb1 w komórkach NK znacznie gorzej odrzucały komórki pozbawione normalnych sygnałów „self” i miały mniejszą zdolność usuwania komórek nowotworowych wrażliwych na NK lub zapobiegania rozsiewowi czerniaka do płuc. Usunięcie Lkb1 we wcześniejszych etapach rozwoju komórek NK powodowało jeszcze poważniejsze niepowodzenia, podkreślając jego znaczenie od najwcześniejszych stadiów.
Co to oznacza dla przyszłych terapii
Dla wielu Lkb1 jest najlepiej znane jako białko supresorowe nowotworu w komórkach rakowych, jednak ta praca uwydatnia jego równie istotną rolę wewnątrz komórek odpornościowych. Lkb1 utrzymuje metaboliczną równowagę komórek NK, dba o ich systemy porządkowe, zapobiega przeciążeniu żelazem i ROS oraz chroni je przed podwójnymi szlakami śmierci i wyczerpaniem. Co ciekawe, typowe drogi wykrywania energii powiązane z Lkb1 w innych komórkach — aktywacja AMPK i hamowanie mTORC1 — nie były w stanie naprawić uszkodzeń przy farmakologicznym modulowaniu, co sugeruje, że komórki NK polegają na odrębnych obwodach downstream. Dla czytelnika nieprofesjonalnego wniosek jest taki, że same komórki NK potrzebują ochrony przed stresem oksydacyjnym i zależnym od żelaza, aby pozostać skutecznymi strażnikami nowotworowymi. Zamiast bezpośrednio modyfikować Lkb1, co mogłoby nieść ryzyko nowotworowe gdzie indziej, terapie precyzyjnie dostrajające równowagę redoks i żelaza w komórkach NK mogą w przyszłości pomóc wzmocnić wczesny alarm organizmu przeciw guzom.
Cytowanie: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Słowa kluczowe: komórki natural killers, LKB1, stres oksydacyjny, homeostaza żelaza, immunonadzór przeciwnowotworowy