Clear Sky Science · it
Liver kinase B1 mantiene la sopravvivenza delle cellule natural killer regolando l’omeostasi redox
Perché anche i nostri “primi soccorritori” del sistema immunitario hanno bisogno di protezione
Le cellule natural killer (NK) sono i soldati della risposta rapida dell’organismo, in pattugliamento alla ricerca di cellule infettate da virus e di cellule tumorali prima dell’intervento di altre forze immunitarie. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: cosa mantiene queste potenti cellule sane e calme fino al momento in cui servono, e cosa succede quando quel sistema di sicurezza interno viene meno? Scoprendo come una singola proteina, chiamata liver kinase B1 (Lkb1), protegga le NK dal danno chimico interno, il lavoro indica nuove strade per rafforzare la sorveglianza antitumorale precoce senza esaurire questi difensori cruciali.
Un interruttore guardiano all’interno delle cellule immunitarie
Le NK devono camminare su una linea sottile. Hanno bisogno di abbastanza energia per scattare in azione, ma non così tanta da diventare iperattive, esaurite o morire. Gli autori mostrano che Lkb1 funziona come un importante “interruttore guardiano” interno che aiuta le NK a rimanere in uno stato tranquillo e pronto. Utilizzando diversi modelli murini ingegnerizzati, hanno rimosso selettivamente Lkb1 dalle NK in varie fasi del loro sviluppo. Indipendentemente dal metodo, il risultato è stato netto: le NK sono diventate scarse in molti organi, si sono bloccate in stadi immaturi e hanno perso i marcatori di superficie che normalmente indicano la piena prontezza al combattimento. Questi effetti erano intrinseci alle cellule, cioè derivavano da problemi dentro le NK stesse piuttosto che dall’ambiente circostante.
Quando la manutenzione cellulare si guasta
Approfondendo, il gruppo ha esaminato quali geni cambiavano in assenza di Lkb1. Migliaia di geni legati all’uso dell’energia, alla divisione cellulare, al riciclo dei rifiuti e alla morte cellulare risultavano alterati. In particolare, le NK prive di Lkb1 mostravano un cedimento nell’autofagia, il sistema di manutenzione della cellula che elimina componenti usurati come mitocondri danneggiati. In condizioni normali questo smaltimento evita l’accumulo di sottoprodotti dannosi. Senza Lkb1, l’autofagia si arrestava: le cellule accumulavano mitocondri in eccesso con un potenziale di membrana anormalmente elevato, e queste strutture difettose sprigionavano grandi quantità di specie reattive dell’ossigeno (ROS) – molecole instabili che possono danneggiare proteine, lipidi e DNA. Anche se le NK carenti di Lkb1 cercavano di compensare dividendosi di più, morivano a tassi più elevati, rivelando che il problema centrale era la sopravvivenza, non la crescita.
Sovraccarico di ferro e un doppio colpo di morte cellulare
I problemi non si fermavano ai ROS. I ricercatori hanno scoperto che le NK prive di Lkb1 perdevano anche il controllo del bilancio del ferro. Queste cellule accumulavano ferro e aumentavano l’espressione di un recettore chiave per l’importazione del ferro, il che a sua volta alimentava la formazione di “lipid ROS” tossici che attaccano le membrane cellulari. Questo quadro è caratteristico della ferroptosi, una forma di morte cellulare dipendente dal ferro. Trattando le cellule con un farmaco che lega il ferro o con un inibitore della ferroptosi, il team è riuscito a recuperare gran parte del difetto di sopravvivenza. Allo stesso tempo, anche le vie classiche della morte programmata erano iperattive: le proteine protettive calavano, gli enzimi esecutori aumentavano e il blocco delle caspasi (gli enzimi che guidano l’apoptosi) migliorava la vitalità. Combinare la rimozione del ferro e l’inibizione delle caspasi forniva un beneficio additivo, indicando che le NK senza Lkb1 sono colpite da due vie di morte indipendenti ma convergenti—danni alle membrane guidati dal ferro e apoptosi guidata dai mitocondri.
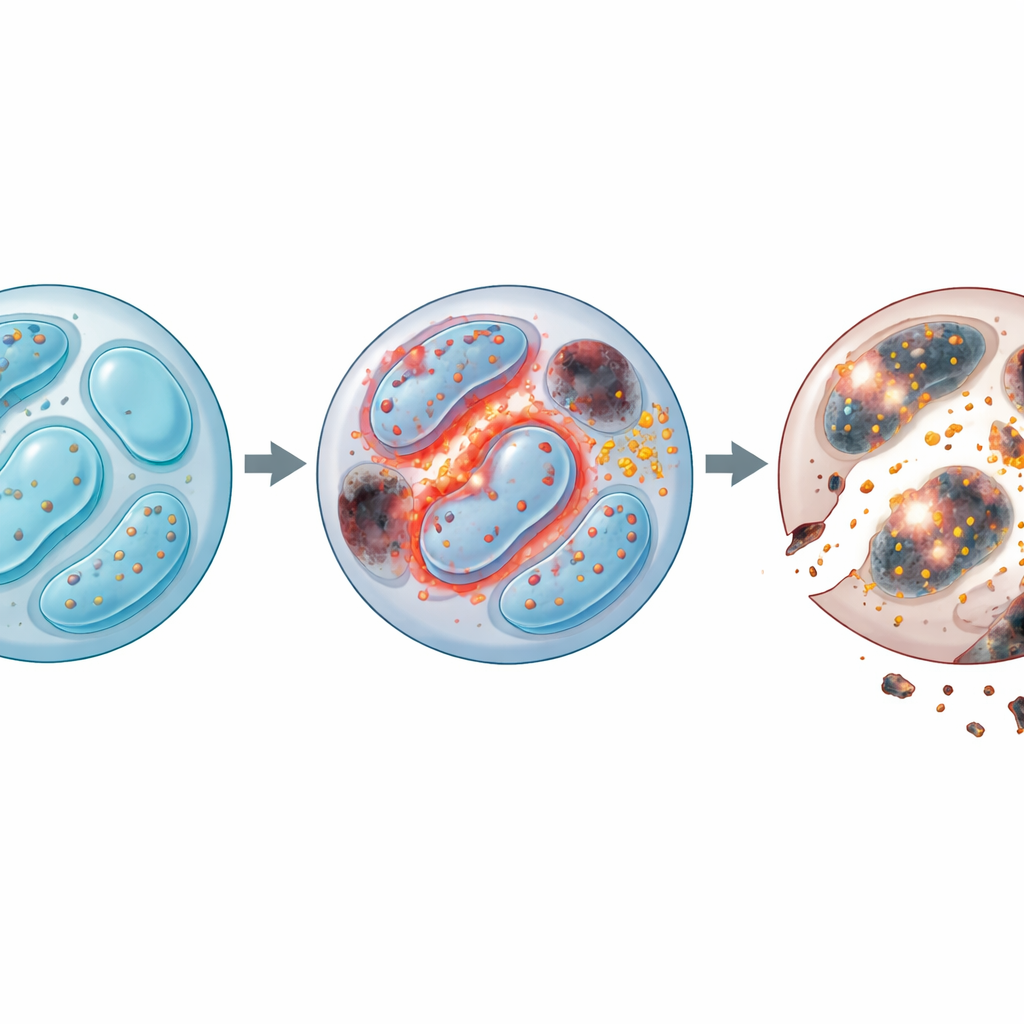
Soldati esausti e pattugliamento tumorale indebolito
Oltre a restare in vita, le NK devono funzionare efficacemente. Le NK prive di Lkb1 producevano meno della molecola chiave della difesa interferone-γ e mostravano livelli più alti di “freni” inibitori sulla loro superficie, come PD‑1 e TIGIT—caratteristiche associate a cellule immunitarie esauste osservate nelle infezioni croniche e nel cancro. Trattamenti antiossidanti che riducevano i ROS o bloccavano la ferroptosi abbassavano questi marcatori di esaurimento e ristabilivano parzialmente l’attività delle NK. Nei topi vivi, le conseguenze erano chiare: gli animali privi di Lkb1 nelle NK erano molto meno efficaci nel rigettare cellule che mancavano di segnali di “self” normali e meno capaci di eliminare cellule tumorali sensibili alle NK o di prevenire la diffusione del melanoma ai polmoni. Rimuovere Lkb1 nelle fasi più precoci dello sviluppo delle NK causava fallimenti ancora più gravi, sottolineandone l’importanza fin dalle fasi iniziali.
Cosa significa per le terapie future
Per molti, Lkb1 è più noto come proteina oncosoppressore nelle cellule tumorali, ma questo lavoro mette in luce il suo ruolo altrettanto critico all’interno delle cellule immunitarie. Lkb1 mantiene le NK in equilibrio metabolico, sostiene i loro sistemi di pulizia interna, previene il sovraccarico di ferro e di ROS e le protegge da doppie vie di morte e dall’esaurimento. È interessante che le vie comuni di rilevamento energetico collegate a Lkb1 in altre cellule—attivazione di AMPK e inibizione di mTORC1—non siano riuscite a riparare il danno quando manipolate farmacologicamente, suggerendo che le NK dipendono da circuiti a valle distinti. Per il lettore non specialistico, la conclusione è che anche le NK hanno bisogno di protezione dallo stress ossidativo e indotto dal ferro per restare sentinelle efficaci contro il cancro. Piuttosto che modificare direttamente Lkb1, operazione che potrebbe comportare rischi onco‑biologici altrove, terapie che modulano finemente il bilancio redox e del ferro nelle NK potrebbero un giorno aiutare a rafforzare il sistema di allerta precoce dell’organismo contro i tumori.
Citazione: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Parole chiave: cellule natural killer, LKB1, stress ossidativo, omeostasi del ferro, immunosorveglianza del cancro