Clear Sky Science · pt
A quinase hepática B1 mantém a sobrevivência de células natural killer regulando a homeostase redox
Por que nossos “primeiros respondedores” do sistema imune também precisam de proteção
As células natural killer (NK) são os soldados de resposta rápida do organismo, patrulhando em busca de células infectadas por vírus e cancerosas antes que outras forças imunes cheguem. Este estudo coloca uma pergunta aparentemente simples, com grandes implicações: o que mantém essas células potentes saudáveis e em estado de prontidão até que sejam necessárias, e o que ocorre quando esse sistema interno de segurança falha? Ao revelar como uma única proteína, chamada quinase hepática B1 (Lkb1), protege as NKs de danos químicos internos, o trabalho aponta novas formas de fortalecer a vigilância precoce do câncer sem exaurir esses defensores cruciais.
Um interruptor guardião dentro das células imunes
As NKs precisam caminhar numa linha tênue. Elas necessitam de energia suficiente para entrar em ação, mas não tanto a ponto de ficarem hiperativas, exauridas ou morrerem. Os autores mostram que Lkb1 atua como um “interruptor guardião” interno que ajuda as NKs a permanecerem num estado silencioso e pronto. Usando vários modelos de camundongos geneticamente modificados, removeram seletivamente Lkb1 das NKs em diferentes estágios do desenvolvimento. Seja qual for a estratégia, o resultado foi marcante: as NKs ficaram escassas em vários órgãos, permaneceram presas em estágios imaturos e perderam marcadores de superfície que normalmente sinalizam prontidão plena para o combate. Esses efeitos foram intrínsecos às células—ou seja, surgiram de problemas dentro das próprias NKs e não do ambiente ao redor.
Quando a manutenção celular entra em colapso
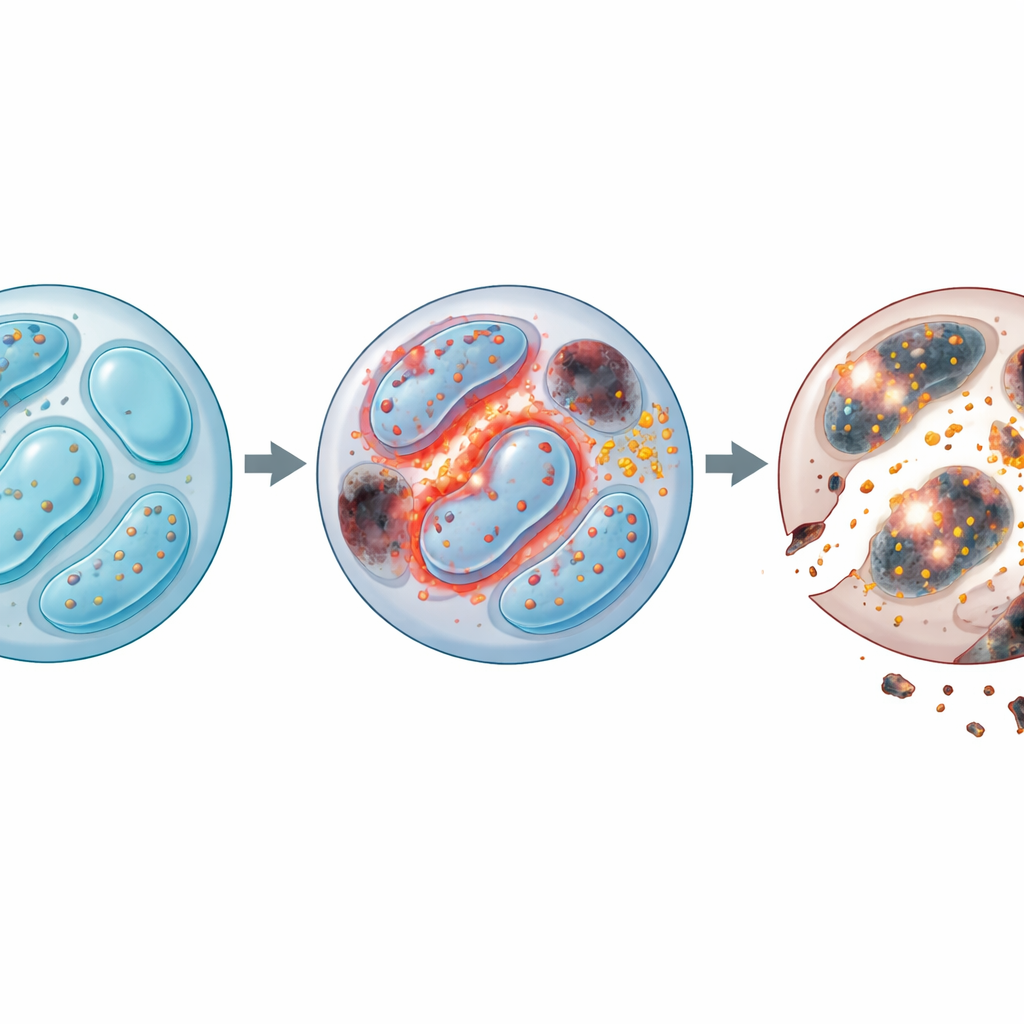
Ao aprofundar, a equipe examinou quais genes mudaram quando Lkb1 estava ausente. Milhares de genes ligados ao uso de energia, divisão celular, reciclagem de resíduos e morte celular foram alterados. Em particular, as NKs sem Lkb1 apresentaram falhas na autofagia, o sistema de manutenção celular que remove partes desgastadas, como mitocôndrias danificadas. Em condições normais, essa limpeza evita que subprodutos nocivos se acumulem. Sem Lkb1, a autofagia estagnou: as células acumularam mitocôndrias extras com potencial de membrana anormalmente alto, e essas estruturas defeituosas liberaram grandes quantidades de espécies reativas de oxigênio (ROS) — moléculas instáveis que podem danificar proteínas, lipídeos e DNA. Mesmo que as NKs deficientes em Lkb1 tentassem compensar dividindo‑se mais, morreram em taxas maiores, revelando que a sobrevivência, e não o crescimento, era o problema central.
Sobrecarga de ferro e um duplo ataque de morte celular
O problema não parou nas ROS. Os pesquisadores descobriram que as NKs sem Lkb1 também perderam o controle do equilíbrio do ferro. Essas células acumularam ferro e aumentaram um receptor-chave de importação de ferro, o que por sua vez alimentou a formação de “lipid ROS” tóxicas que atacam as membranas celulares. Esse padrão é característico da ferroptose, uma forma de morte celular dependente de ferro. Tratando as células com um fármaco quelante de ferro ou com um bloqueador de ferroptose, a equipe conseguiu resgatar boa parte do defeito de sobrevivência. Ao mesmo tempo, vias clássicas de morte celular programada também estavam hiperativas: proteínas protetoras diminuíram, enzimas executoras aumentaram, e bloquear as caspases (as enzimas que conduzem a apoptose) melhorou a viabilidade. Combinar remoção do ferro e inibição de caspases trouxe um benefício aditivo, indicando que as NKs sem Lkb1 sofrem dois caminhos de morte independentes, porém convergentes—danos à membrana dirigidos pelo ferro e apoptose dirigida por mitocôndrias.
Soldados exauridos e patrulha tumoral enfraquecida
Além de permanecer vivas, as NKs precisam funcionar efetivamente. As NKs deficientes em Lkb1 produziram menos da molécula defensiva chave interferon‑γ e exibiram níveis mais altos de “freios” inibitórios na superfície, como PD‑1 e TIGIT—características associadas à exaustão de células imunes observada em infecções crônicas e câncer. Tratamentos antioxidantes que reduziram ROS ou bloquearam a ferroptose diminuíram esses marcadores de exaustão e restauraram parcialmente a atividade das NKs. Em camundongos vivos, as consequências foram claras: animais sem Lkb1 nas NKs foram muito piores em rejeitar células que careciam de sinais normais de “self” e menos capazes de eliminar células tumorais sensíveis a NKs ou prevenir a disseminação de melanoma para os pulmões. Remover Lkb1 mais cedo no desenvolvimento das NKs causou falhas ainda mais graves, reforçando sua importância desde os estágios iniciais.
O que isso significa para terapias futuras
Para muitos, Lkb1 é mais conhecido como uma proteína supressora de tumor em células cancerosas, mas este trabalho destaca seu papel igualmente crítico dentro das células imunes. Lkb1 mantém o equilíbrio metabólico das NKs, sustenta seus sistemas internos de limpeza, evita sobrecarga de ferro e ROS e protege‑as contra vias duplas de morte e exaustão. Curiosamente, rotas comuns de sensoriamento de energia ligadas a Lkb1 em outras células—ativação de AMPK e inibição de mTORC1—não conseguiram reparar o dano quando manipuladas farmacologicamente, sugerindo que as NKs dependem de circuitos downstream distintos. Para o leitor leigo, a conclusão é que as próprias NKs precisam de proteção contra estresse oxidativo e por ferro para permanecerem sentinelas eficazes contra o câncer. Em vez de alterar diretamente Lkb1, o que poderia acarretar riscos oncológicos em outros tecidos, terapias que ajustem finamente o balanço redox e do ferro nas NKs poderão, um dia, ajudar a reforçar o sistema de alerta precoce do corpo contra tumores.
Citação: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Palavras-chave: células natural killer, LKB1, estresse oxidativo, homeostase do ferro, imunovigilância do câncer