Clear Sky Science · ru
Киназа печени B1 поддерживает выживание натуральных киллеров, регулируя редокс‑гомеостаз
Почему нашим «первым реагирующим» иммунным клеткам тоже нужна защита
Натуральные киллеры (NK‑клетки) — это быстро реагирующие солдаты организма, патрулирующие в поисках инфицированных вирусом и раковых клеток до прибытия других сил иммунной системы. В этом исследовании задается обманчиво простой вопрос с большими последствиями: что поддерживает эти мощные клетки здоровыми и спокойными до момента их необходимости, и что происходит, когда внутренняя система безопасности даёт сбой? Раскрыв, как один белок, называемый киназой печени B1 (Lkb1), защищает NK‑клетки от внутреннего химического повреждения, работа указывает на новые способы укрепить ранний иммунный надзор за раком, не истощая этих ключевых защитников.
Защитный переключатель внутри иммунных клеток
NK‑клетки вынуждены идти по тонкой грани. Им нужна достаточная энергия, чтобы мгновенно включиться в ответ, но не настолько много, чтобы они стали гиперактивными, истощились или погибли. Авторы показывают, что Lkb1 действует как ключевой внутренний «защитный переключатель», который помогает NK‑клеткам оставаться в спокойном, готовом состоянии. Используя несколько генетически модифицированных моделей мышей, они избирательно удаляли Lkb1 из NK‑клеток на разных стадиях их развития. Независимо от подхода результат был поразительным: NK‑клеток становилось мало во многих органах, они застревали на незрелых стадиях и теряли поверхностные маркеры, которые обычно сигнализируют о полной готовности к бою. Эти эффекты были клеточно‑встроенными, то есть возникали вследствие проблем внутри самих NK‑клеток, а не из‑за внешней среды.
Когда внутреннее обслуживание клетки нарушается
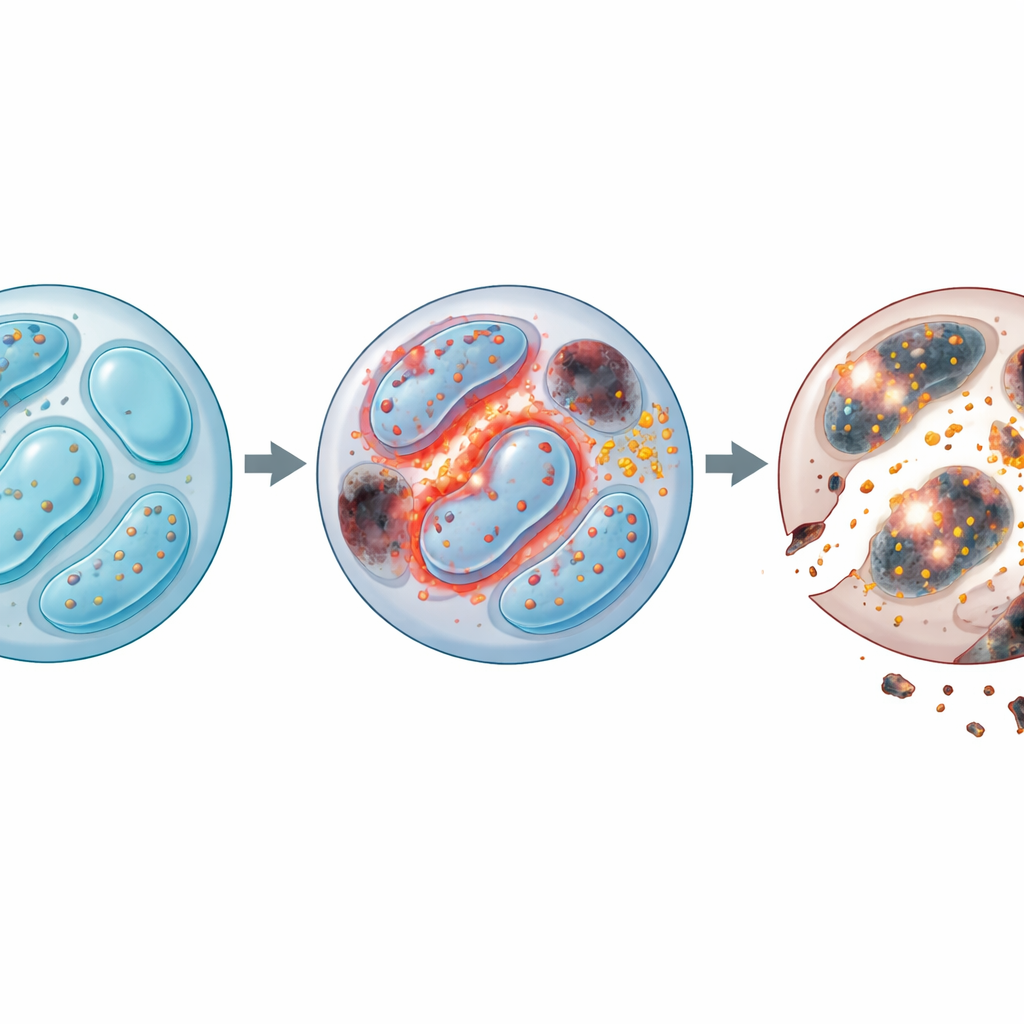
Углубившись, команда изучила, какие гены меняли свою экспрессию при отсутствии Lkb1. Тысячи генов, связанных с использованием энергии, делением клеток, переработкой отходов и смертью клеток, оказались изменены. В частности, в NK‑клетках без Lkb1 наблюдался сбой автопагии — системы клеточного «уборки», удаляющей изношенные компоненты, такие как повреждённые митохондрии. При нормальных условиях эта уборка не даёт накапливаться вредным побочным продуктам. Без Lkb1 автопагия останавливалась: клетки накапливали лишние митохондрии с аномально высоким мембранным потенциалом, и эти дефектные структуры выбрасывали большое количество реактивных форм кислорода (ROS) — нестабильных молекул, которые могут повреждать белки, липиды и ДНК. Хотя NK‑клетки, лишённые Lkb1, пытались компенсировать, делясь чаще, они умирали с большей частотой, что показало: ключевая проблема — выживание, а не рост.
Перегрузка железом и двойной удар клеточной смерти
Проблемы не ограничивались ROS. Исследователи обнаружили, что NK‑клетки без Lkb1 также теряли контроль над балансом железа. Эти клетки запасали железо и усиливали экспрессию ключевого рецептора импорта железа, что, в свою очередь, подпитывало образование токсичных «липидных ROS», атакующих клеточные мембраны. Такая картина характерна для ферроптоза — зависимого от железа типа гибели клетки. Лечение клеток препаратом, связывающим железо, или блокатором ферроптоза позволяло частично восстановить выживаемость. В то же время классические пути запрограммированной клеточной смерти также были чрезмерно активны: уровни защитных белков падали, возрастало содержание «касспаз‑исполнителей», и блокирование каспаз (ферментов, запускающих апоптоз) улучшало жизнеспособность. Совместное удаление железа и ингибирование каспаз давало складывающийся эффект, что указывает на то, что NK‑клетки без Lkb1 поражаются двумя независимыми, но сходящимися путями смерти — повреждением мембран, вызванным железом, и митохондриально‑опосредованным апоптозом.
Истощённые солдаты и ослабленный патруль против опухолей
Помимо выживания, NK‑клетки должны эффективно выполнять функции. NK‑клетки с дефицитом Lkb1 вырабатывали меньше ключевого защитного молекулы интерферона‑γ и демонстрировали повышенные уровни ингибирующих «тормозов» на поверхности, таких как PD‑1 и TIGIT — признаки истощённых иммунных клеток, наблюдаемых при хронических инфекциях и раке. Антиоксидантные обработки, снижавшие ROS или блокировавшие ферроптоз, уменьшали эти маркеры истощения и частично восстанавливали активность NK‑клеток. В живых мышах последствия были очевидны: животные с удалённым Lkb1 в NK‑клетках хуже отторгали клетки, лишённые нормальных «маркёров себя», и хуже очищали опухолевые клетки, чувствительные к NK, а также не могли эффективно предотвратить распространение меланомы в лёгкие. Удаление Lkb1 на более ранних этапах развития NK‑клеток вызывало ещё более тяжёлые нарушения, подчёркивая его важность с самых ранних стадий.
Что это означает для будущих терапий
Для многих Lkb1 известен прежде всего как белок‑супрессор опухолей в раковых клетках, но эта работа подчёркивает его не менее критическую роль внутри иммунных клеток. Lkb1 поддерживает метаболическое равновесие NK‑клеток, сохраняет их системы внутренней уборки, предотвращает перегрузку железом и ROS и защищает их от двух путей гибели и истощения. Интересно, что общие пути детектирования энергии, связанные с Lkb1 в других клетках — активация AMPK и ингибирование mTORC1 — не могли устранить повреждение при фармакологической модификации, что намекает на то, что NK‑клетки опираются на отличные нисходящие цепи сигнализации. Для неспециалиста вывод таков: сами NK‑клетки нуждаются в защите от окислительного и железосвязанного стресса, чтобы оставаться эффективными «часовыми» против опухолей. Вместо прямой модуляции Lkb1, что потенциально несёт риски для подавления опухолей в других тканях, терапевтические подходы, тонко настраивающие редокс‑и железный баланс в NK‑клетках, могли бы в будущем помочь укрепить собственную систему раннего предупреждения организма против опухолей.
Цитирование: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Ключевые слова: натуральные киллеры, LKB1, окислительный стресс, гомеостаз железа, иммунный надзор за раком