Clear Sky Science · ar
كيناز الكبد B1 يحافظ على بقاء الخلايا القاتلة الطبيعية من خلال تنظيم التوازن الاختزالي-الأكسدي
لماذا يحتاج «المستجيبون الأوائل» في جهازنا المناعي إلى الحماية أيضاً
الخلايا القاتلة الطبيعية (NK) هي جنود الاستجابة السريعة في الجسم، تجوب للبحث عن الخلايا المصابة بالفيروسات والخلايا السرطانية قبل وصول بقية قوات المناعة. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو آثار واسعة: ما الذي يحافظ على هذه الخلايا القوية بصحة وهدوء حتى يحين وقت الحاجة إليها، وماذا يحدث عندما يفشل ذلك النظام الداخلي للحماية؟ من خلال الكشف عن كيفية حماية بروتين واحد، يسمى كيناز الكبد B1 (Lkb1)، للخلايا القاتلة الطبيعية من الأضرار الكيميائية الداخلية، تشير النتائج إلى سبل جديدة لتعزيز المراقبة المبكرة للسرطان دون إجهاد أو استنزاف هؤلاء المدافعين الحيويين.
مفتاح الحماية داخل الخلايا المناعية
على الخلايا القاتلة الطبيعية أن تحافظ على توازن دقيق. تحتاج إلى طاقة كافية للانقضاض حين الحاجة، لكن ليس إلى حد يجعلها مفرطة النشاط أو منهكة أو تموت. يوضح المؤلفون أن Lkb1 يعمل كمفتاح حماية داخلي رئيسي يساعد الخلايا القاتلة الطبيعية على البقاء في حالة هادئة وجاهزة. باستخدام عدة نماذج فئران مُعدَّلة وراثياً، أزالوا Lkb1 انتقائياً من الخلايا القاتلة الطبيعية في مراحل مختلفة من تطورها. وبغض النظر عن الطريقة، كانت النتيجة لافتة: تقلصت أعداد الخلايا القاتلة الطبيعية في عدة أعضاء، وعلِقت في مراحل نمو غير ناضجة، وفقدت العلامات السطحية التي تشير عادة إلى الجاهزية الكاملة للقتال. وكانت هذه التأثيرات داخلية الخلية بطبيعتها، أي أنها ناتجة عن مشاكل داخل الخلايا نفسها وليس عن بيئتها المحيطة.
عندما ينهار نظام تنظيف الخلايا
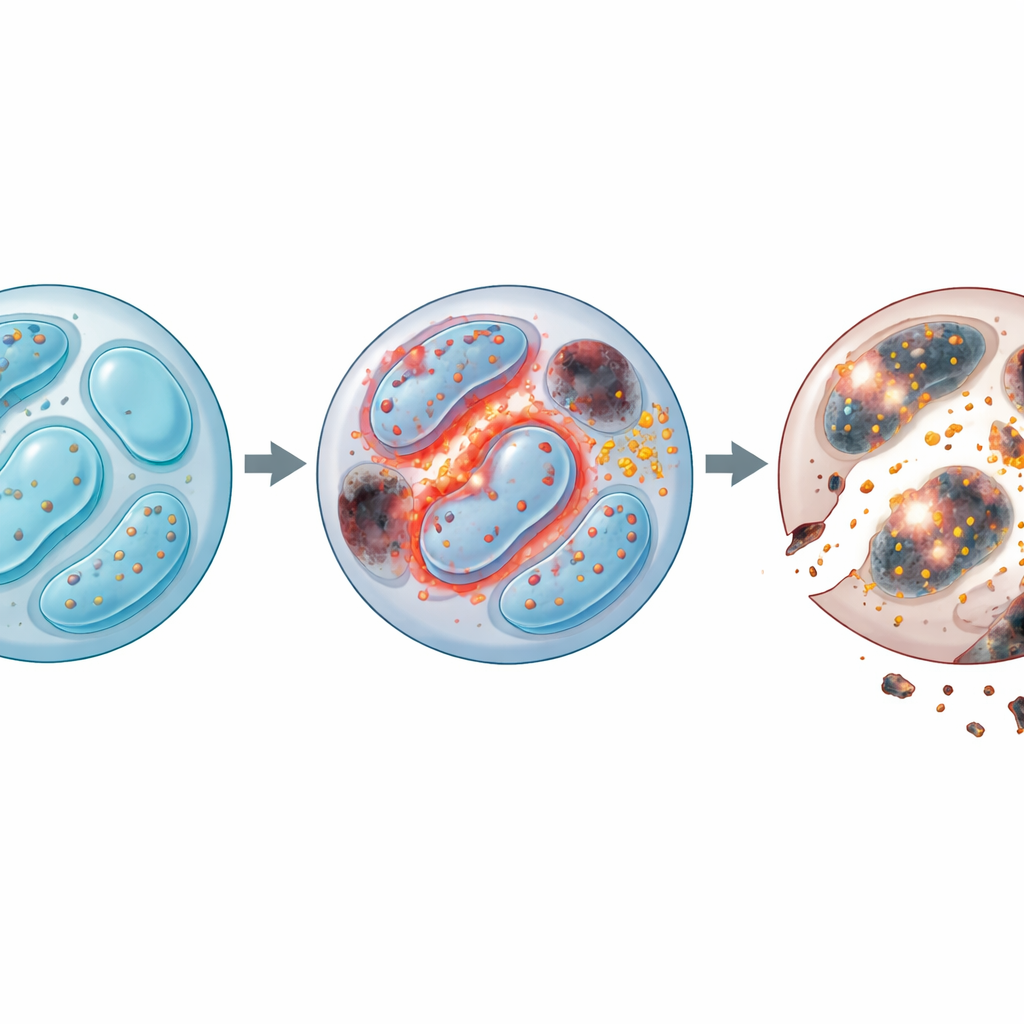
بتعمق أكبر، فحص الفريق أي الجينات تغيرت عند غياب Lkb1. تغيّرت آلاف الجينات المرتبطة باستخدام الطاقة، وانقسام الخلايا، وإعادة تدوير النفايات، والموت الخلوي. على وجه الخصوص، أظهرت الخلايا القاتلة الطبيعية الخالية من Lkb1 انهياراً في الالتهام الذاتي (autophagy)، وهو نظام تنظيف الخلية الذي يزيح الأجزاء البالية مثل الميتوكوندريا التالفة. في الظروف الطبيعية، يمنع هذا التنظيف تراكم المنتجات الثانوية الضارة. بدون Lkb1، تعطل الالتهام الذاتي: تراكمت ميتوكوندريا زائدة ذات فرق جهد غشائي مرتفع غير طبيعي، وهذه الهياكل المعيبة أطلقت كميات كبيرة من أنواع الأكسجين التفاعلية (ROS) — جزيئات غير مستقرة يمكن أن تتلف البروتينات والدهون والحمض النووي. وعلى الرغم من محاولات خلايا NK الخالية من Lkb1 التعويض بالانقسام بمعدل أعلى، فقد ماتت بمعدلات أكبر، مما كشف أن البقاء، وليس النمو، كان المشكلة الأساسية.
حمولة الحديد ومزدوجة الموت الخلوية
لم تتوقف المشكلة عند ROS. وجد الباحثون أن الخلايا القاتلة الطبيعية الخالية من Lkb1 فقدت أيضاً السيطرة على توازن الحديد. فقد جمعت هذه الخلايا الحديد وزادت من تعبير مستقبل استيراد الحديد الرئيسي، مما غذّى بدوره تكوّن «الـROS الدهنية» السامة التي تهاجم أغشية الخلايا. هذا النمط يميّز موت الخلايا بالحديد (ferroptosis)، وهو شكل من أشكال الموت الخلوي المعتمد على الحديد. بمعالجة الخلايا بعقار رابط للحديد أو بمانع للفروبتوزيس، استطاع الفريق إنقاذ جزء كبير من عيب البقاء. في الوقت نفسه، كانت مسارات الموت المبرمجة التقليدية مفرطة التفعيل أيضاً: انخفضت البروتينات الوقائية، وارتفعت الإنزيمات المنفذة، وتحسين الحيوية بفضل حجب الكاسبازات (الإنزيمات المسؤولة عن الاستماتة). إن الجمع بين إزالة الحديد وتثبيط الكاسبازات أعطى فائدة تزايدية، مما يشير إلى أن الخلايا القاتلة الطبيعية الخالية من Lkb1 تتعرض لضربتين مستقلتين لكن متقاربتين من مسارات الموت — تلف الأغشية المحرك بالحديد واستماتة مدفوعة بالميتوكندريا.
جنود منهكون ودورية أضعف ضد الأورام
إلى جانب البقاء على قيد الحياة، يجب أن تعمل الخلايا القاتلة الطبيعية بفاعلية. أنتجت خلايا NK الخالية من Lkb1 كميات أقل من جزيء الدفاع الرئيسي إنترفيرون-γ وأظهرت مستويات أعلى من «المكابح» المثبطة على سطحها، مثل PD‑1 وTIGIT — سمات مرتبطة بالخلايا المناعية المنهكة التي تُرى في العدوى المزمنة والسرطان. خفضت العلاجات المضادة للأكسدة التي قللت ROS أو حجبت الفيروبتوزيس هذه علامات الإجهاد واستعادت جزئياً نشاط الخلايا القاتلة الطبيعية. وفي الفئران الحية، كانت العواقب واضحة: الحيوانات التي افتقرت إلى Lkb1 في خلايا NK كانت أسوأ بكثير في رفض الخلايا التي تفتقر إلى إشارات «الذاتي» العادية وكانت أقل قدرة على إزالة الخلايا الورمية الحساسة لـNK أو منع انتشار الميلانوما إلى الرئتين. وأدى إزالة Lkb1 في مراحل أبكر من تطور خلايا NK إلى إخفاقات أشد، مما يبرز أهميته منذ المراحل الأولى فصاعداً.
ما مغزى ذلك للعلاجات المستقبلية
يعرف الكثيرون Lkb1 بشكل أساسي كبروتين مثبط للأورام في الخلايا السرطانية، لكن هذا العمل يبرز دوره الحاسم داخل الخلايا المناعية أيضاً. يحافظ Lkb1 على توازن الخلايا القاتلة الطبيعية من الناحية الأيضية، ويضمن أنظمة التنظيف الداخلية لديها، ويمنع حمولة الحديد وROS المفرطة، ويحميها من مساري موت مزدوجين ومن الإجهاد. ومن المثير للاهتمام أن الطرق الشائعة لاستشعار الطاقة المرتبطة بـLkb1 في خلايا أخرى — تفعيل AMPK وتثبيط mTORC1 — لم تستطع إصلاح الضرر عند تعديلها دوائياً، مما يوحي بأن خلايا NK تعتمد على دوائر سفلية مختلفة. للمختصر للقارئ العام: تحتاج خلايا NK نفسها إلى حماية من الإجهاد التأكسدي والمرتكز على الحديد لتظل حراساً فعالين ضد السرطان. وبدلاً من تعديل Lkb1 مباشرة، الأمر الذي قد يحمل مخاطر سرطانية في أماكن أخرى، قد تساعد العلاجات التي تضبط التوازن الاختزالي-الأكسدي والحد من الحديد داخل خلايا NK يوماً ما على تعزيز نظام الإنذار المبكر الطبيعي للجسم ضد الأورام.
الاستشهاد: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
الكلمات المفتاحية: الخلايا القاتلة الطبيعية, LKB1, الإجهاد التأكسدي, توازن الحديد, المراقبة المناعية للسرطان