Clear Sky Science · de
Leberkinase B1 erhält das Überleben natürlicher Killerzellen durch Regulierung der Redox‑Homöostase
Warum auch unsere immunologischen „Ersthelfer“ Schutz brauchen
Natürliche Killerzellen (NK‑Zellen) sind die Schnellreaktionssoldaten des Körpers und durchsuchen Gewebe nach virusinfizierten und krebsverdächtigen Zellen, noch bevor andere Immunkräfte eingreifen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Was hält diese kraftvollen Zellen gesund und ruhig, bis sie gebraucht werden, und was passiert, wenn dieses innere Schutzsystem versagt? Indem sie zeigen, wie ein einzelnes Protein, die Leberkinase B1 (Lkb1), NK‑Zellen vor inneren chemischen Schäden schützt, weist die Arbeit auf neue Ansätze hin, wie man die frühe Krebsüberwachung stärken kann, ohne diese wichtigen Verteidiger zu überlasten.
Ein Wächter‑Schalter innerhalb der Immunzellen
NK‑Zellen müssen ein feines Gleichgewicht halten. Sie brauchen genügend Energie, um schnell aktiv zu werden, aber nicht so viel, dass sie überaktiv, erschöpft oder zugrunde gehen. Die Autorinnen und Autoren zeigen, dass Lkb1 als zentraler innerer „Wächter‑Schalter“ fungiert, der NK‑Zellen in einem ruhigen, einsatzbereiten Zustand hält. Mithilfe verschiedener gentechnischer Mausmodelle entfernten sie Lkb1 selektiv aus NK‑Zellen in unterschiedlichen Entwicklungsstadien. Unabhängig vom Ansatz war das Ergebnis eindrücklich: NK‑Zellen wurden in vielen Organen rar, blieben in unreifen Stadien stecken und verloren die Oberflächenmarker, die normalerweise volle Einsatzbereitschaft anzeigen. Diese Effekte waren zellintrinsisch, das heißt, sie entstanden durch Probleme innerhalb der NK‑Zellen selbst und nicht durch deren Umfeld.
Wenn die zelluläre Hausordnung zusammenbricht
Bei näherer Untersuchung identifizierte das Team Tausende von Genen, deren Expression sich bei fehlendem Lkb1 veränderte – vor allem Gene, die mit Energiehaushalt, Zellteilung, Recycling und Zelltod verknüpft sind. Besonders auffällig war ein Versagen der Autophagie, des zellulären Hausputzsystems, das verschlissene Komponenten wie beschädigte Mitochondrien entfernt. Unter normalen Bedingungen verhindert dieses Aufräumen die Anhäufung schädlicher Nebenprodukte. Ohne Lkb1 stockte die Autophagie: Zellen häuften zusätzliche Mitochondrien mit ungewöhnlich hohem Membranpotenzial an, und diese fehlerhaften Strukturen setzten große Mengen reaktiver Sauerstoffspezies (ROS) frei – instabile Moleküle, die Proteine, Fette und DNA schädigen können. Obwohl Lkb1‑defiziente NK‑Zellen versuchten, dies durch vermehrte Teilung auszugleichen, starben sie häufiger, sodass sich zeigte, dass Überleben, nicht Wachstum, das Kernproblem war.
Eisenüberladung und ein doppelter Schlag des Zelltods
Das Problem beschränkte sich nicht auf ROS. Die Forschenden stellten fest, dass NK‑Zellen ohne Lkb1 auch die Eisenbalance verloren. Diese Zellen horteten Eisen und erhöhten den Ausdruck eines wichtigen Eisenimportrezeptors, was wiederum die Bildung toxischer „lipidärer ROS“ anheizte, die Zellmembranen angreifen. Dieses Muster ist typisch für die Ferroptose, eine eisenabhängige Form des Zelltods. Durch Behandlung der Zellen mit einem eisenbindenden Wirkstoff oder einem Ferroptose‑Blocker ließ sich ein Großteil des Überlebensdefekts beheben. Zugleich waren klassische Wege des programmierten Zelltods überaktiv: schützende Proteine sanken, effektorische Enzyme stiegen, und die Blockade von Caspasen (den Enzymen, die die Apoptose vorantreiben) verbesserte die Lebensfähigkeit. Die Kombination aus Eisenentfernung und Caspasenhemmung brachte zusätzlichen Nutzen, was darauf hindeutet, dass NK‑Zellen ohne Lkb1 von zwei unabhängigen, aber konvergierenden Todeswegen getroffen werden – eisengetriebene Membranschäden und mitochondrial vermittelte Apoptose.
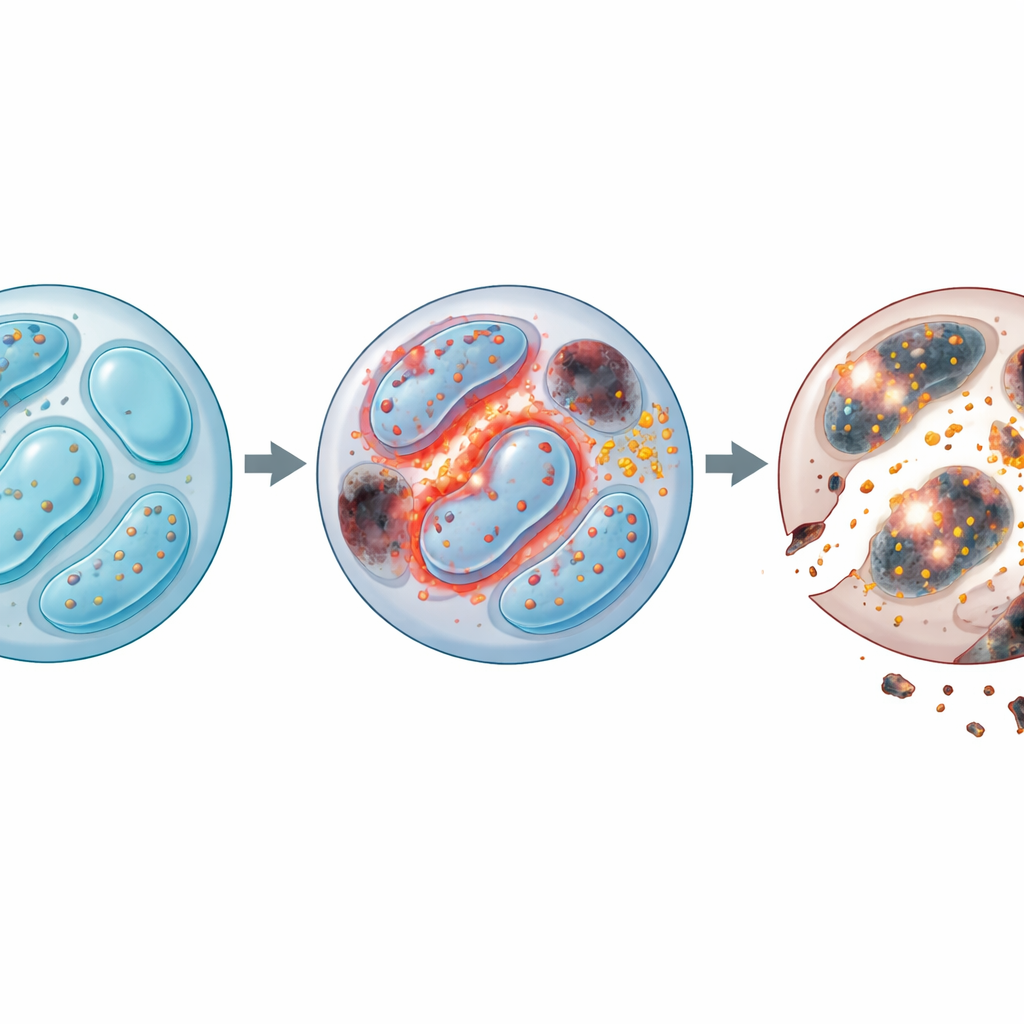
Erschöpfte Soldaten und geschwächtes Tumorpatrouillieren
Über das bloße Überleben hinaus müssen NK‑Zellen auch funktionsfähig bleiben. Lkb1‑defiziente NK‑Zellen produzierten weniger des wichtigen Abwehrmoleküls Interferon‑γ und zeigten höhere Spiegel an inhibitorischen „Bremsen“ auf ihrer Oberfläche, wie PD‑1 und TIGIT – Merkmale, die mit erschöpften Immunzellen bei chronischen Infektionen und Krebs assoziiert sind. Antioxidative Behandlungen, die ROS reduzierten oder Ferroptose blockierten, senkten diese Erschöpfungsmarker und stellten die NK‑Zell‑Aktivität teilweise wieder her. In lebenden Mäusen waren die Folgen deutlich: Tiere ohne Lkb1 in NK‑Zellen waren wesentlich schlechter darin, Zellen ohne normale „Selbst“‑Signale abzuwehren, konnten NK‑sensitive Tumorzellen schlechter eliminieren und die Ausbreitung von Melanomen in die Lungen weniger effektiv verhindern. Die frühe Entfernung von Lkb1 während der NK‑Zell‑Entwicklung führte zu noch schwereren Ausfällen und unterstreicht seine Bedeutung bereits in den frühesten Stadien.
Was das für künftige Therapien bedeutet
Für viele ist Lkb1 vor allem als Tumorsuppressor in Krebszellen bekannt, doch diese Arbeit hebt seine ebenso wichtige Rolle innerhalb von Immunzellen hervor. Lkb1 hält NK‑Zellen metabolisch im Gleichgewicht, erhält ihre internen Reinigungsmechanismen, verhindert Eisen‑ und ROS‑Überlastung und schützt sie vor doppelten Todeswegen und Erschöpfung. Interessanterweise konnten die bekannten energiesensiblen Signalwege, die in anderen Zellen mit Lkb1 verknüpft sind – AMPK‑Aktivierung und mTORC1‑Hemmung – durch pharmakologische Modulation den Schaden nicht beheben, was darauf hindeutet, dass NK‑Zellen auf eigene, unterschiedliche nachgeschaltete Schaltkreise angewiesen sind. Für Laien lautet die wesentliche Schlussfolgerung: Auch NK‑Zellen selbst brauchen Schutz vor oxidativem und eisengetriebenem Stress, um als effektive Tumorwächter zu funktionieren. Anstatt Lkb1 direkt zu verändern, was anderswo Krebsrisiken bergen könnte, könnten Therapien, die Redox‑ und Eisenhaushalt in NK‑Zellen feinjustieren, eines Tages helfen, das körpereigene Frühwarnsystem gegen Tumore zu stärken.
Zitation: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Schlüsselwörter: natürliche Killerzellen, LKB1, oxidativer Stress, Eisenhomöostase, Immunüberwachung von Krebs