Clear Sky Science · sv
Liver kinase B1 upprätthåller naturliga mördarcellers överlevnad genom att reglera redox‑homeostas
Varför våra immunsystems ”förstainsatser” också behöver skydd
Naturliga mördarceller (NK‑celler) är kroppens snabbinsatsstyrkor som patrullerar efter virusinfekterade och cancerösa celler innan andra immunceller hinner dit. Denna studie ställer en till synes enkel men betydelsefull fråga: vad håller dessa kraftfulla celler friska och lugna tills de behövs, och vad händer när det inre säkerhetssystemet sviktar? Genom att avslöja hur ett enda protein, kallat liver kinase B1 (Lkb1), skyddar NK‑celler från inre kemiska skador, pekar arbetet på nya sätt att stärka tidig cancerövervakning utan att utarma dessa viktiga försvarare.
En skyddsbrytare inne i immuncellerna
NK‑celler måste gå en balansakt. De behöver tillräckligt med energi för att snabbt sätta in ett svar, men inte så mycket att de blir överaktiva, utmattade eller dör. Författarna visar att Lkb1 fungerar som en viktig inre ”skyddsbrytare” som hjälper NK‑celler att förbli i ett tyst, berett tillstånd. Med flera genetiskt manipulerade musmodeller tog de selektivt bort Lkb1 ur NK‑celler i olika utvecklingsstadier. Oavsett strategi blev resultatet tydligt: NK‑celler blev ovanligt få i många organ, fastnade i omogna stadier och förlorade de ytmarkörer som normalt signalerar full stridsberedskap. Dessa effekter var cellintrinsiska, vilket betyder att problemen uppstod inom NK‑cellerna själva snarare än från deras omgivning.
När cellens städning kollapsar
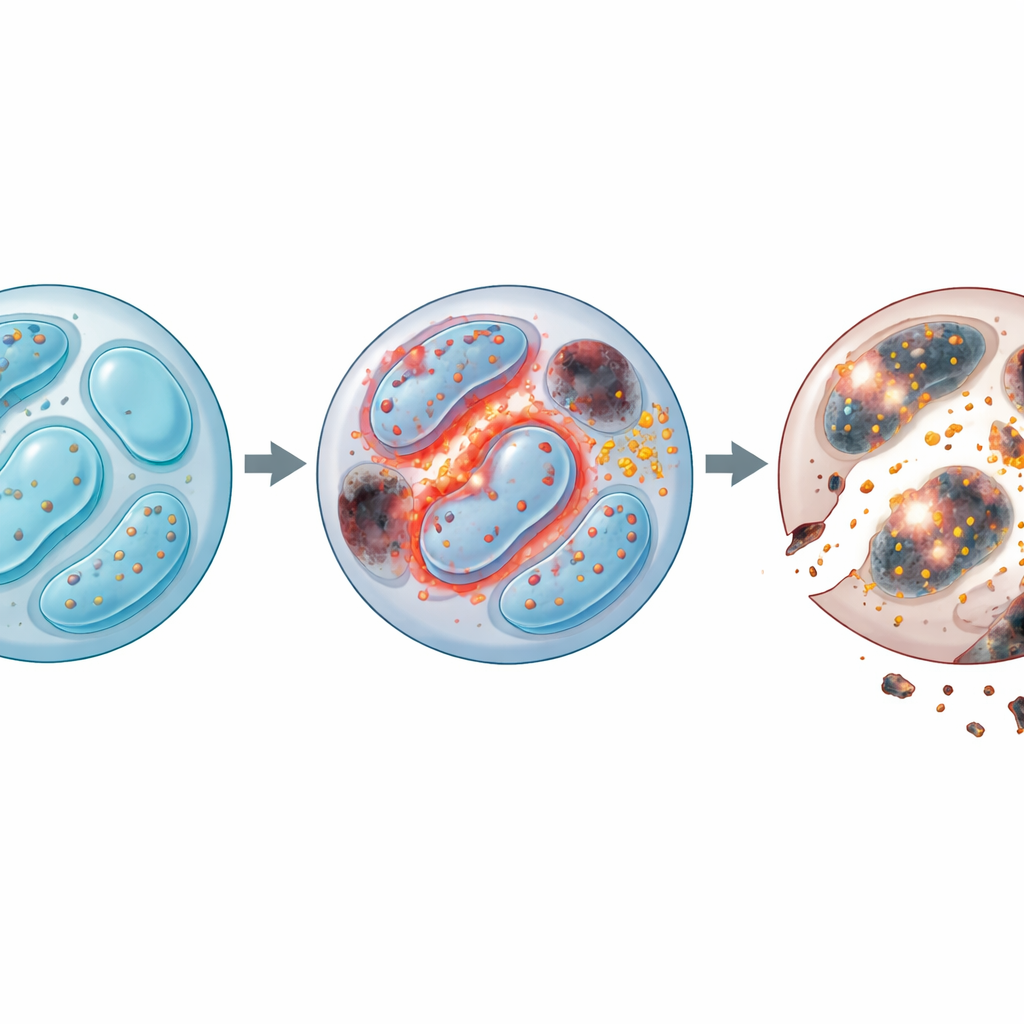
Vid en djupare analys undersökte teamet vilka gener som förändrades när Lkb1 saknades. Tusentals gener kopplade till energiomsättning, celldelning, återvinning och celldöd påverkades. Särskilt visade NK‑celler utan Lkb1 en nedbrytning av autofagi, cellens städsystem som rensar ut slitna delar som skadade mitokondrier. Under normala förhållanden förhindrar denna städning att skadliga biprodukter byggs upp. Utan Lkb1 stannade autofagin av: cellerna ackumulerade extra mitokondrier med abnormt hög membranpotential, och dessa defekta strukturer spydde ut stora mängder reaktiva syrearter (ROS) – instabila molekyler som kan skada proteiner, fetter och DNA. Trots att Lkb1‑defekta NK‑celler försökte kompensera genom att dela sig mer, dog de i högre takt, vilket visar att överlevnad, inte tillväxt, var det grundläggande problemet.
Järnöverskott och en dubbelattack av celldöd
Problemen slutade inte vid ROS. Forskarna fann att NK‑celler utan Lkb1 också förlorade kontrollen över järnbalansen. Dessa celler lagrade järn och uppreglerade en viktig järnimportreceptor, vilket i sin tur främjade bildningen av toxiska ”lipid‑ROS” som angriper cellmembran. Detta mönster är karakteristiskt för ferroptos, en järnberoende form av celldöd. Genom att behandla cellerna med ett järnbindande läkemedel eller en ferroptoshämmare kunde teamet rädda stora delar av överlevnadsdefekten. Samtidigt var klassiska programmerade celldödsvägar också överaktiva: skyddande proteiner minskade, verkställarenzymer ökade, och blockering av kaspaser (enzymerna som driver apoptos) förbättrade cellviabiliteten. Kombinationen av järnavlägsnande och kaspasinhibering gav en additiv nytta, vilket indikerar att NK‑celler utan Lkb1 drabbas av två oberoende men konvergerande dödsvägar – järn‑driven membranskada och mitokondrie‑driven apoptos.
Utmattade soldater och försvagad tumörpatrull
Utöver att överleva måste NK‑celler fungera effektivt. Lkb1‑defekta NK‑celler producerade mindre av det viktiga försvarsmolekylet interferon‑γ och visade högre nivåer av hämmande ”bromsar” på ytan, såsom PD‑1 och TIGIT – egenskaper som förknippas med utmattade immunceller vid kroniska infektioner och cancer. Antioxidantbehandlingar som minskade ROS eller blockerade ferroptos sänkte dessa utmattningsmarkörer och återställde delvis NK‑cellernas aktivitet. I levande möss var konsekvenserna tydliga: djur som saknade Lkb1 i NK‑celler hade svårare att avvisa celler utan normala ”själv”‑signaler och var mindre kapabla att rensa NK‑känsliga tumörceller eller förhindra spridning av melanom till lungorna. Att ta bort Lkb1 tidigare i NK‑cellernas utveckling ledde till ännu allvarligare fel, vilket understryker dess betydelse från de tidigaste stadierna.
Vad detta betyder för framtida terapier
För många är Lkb1 mest känd som ett tumörsuppressorprotein i cancerceller, men detta arbete lyfter fram dess lika kritiska roll inne i immunceller. Lkb1 håller NK‑cellerna metabolt balanserade, upprätthåller deras interna städsystem, förhindrar järn‑ och ROS‑överbelastning och skyddar dem från dubbla dödsvägar och utmattning. Intressant nog kunde vanliga energikänsliga vägar kopplade till Lkb1 i andra celler – AMPK‑aktivering och mTORC1‑hämning – inte reparera skadorna när de farmakologiskt modifierades, vilket antyder att NK‑celler förlitar sig på distinkta nedströmskretsar. För en lekmannaläsare är slutsatsen att NK‑celler själva behöver skydd mot oxidativt och järndrivet stress för att förbli effektiva tumörvakter. Istället för att direkt förändra Lkb1, vilket kan medföra cancerrelaterade risker på andra håll, kan terapier som finjusterar redox‑ och järnbalansen i NK‑celler en dag hjälpa till att stärka kroppens eget tidiga varningssystem mot tumörer.
Citering: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Nyckelord: naturliga mördarceller, LKB1, oxidativ stress, järnhomeostas, cancerimmunövervakning