Clear Sky Science · nl
Liver kinase B1 behoudt de overleving van natural killer‑cellen door regulatie van redox‑homeostase
Waarom onze immuun “eerstehulpverleners” ook bescherming nodig hebben
Natural killer (NK)‑cellen zijn de snelle responseenheden van het lichaam, die patrouilleren op virus‑infecties en kankercellen nog voordat andere immuundefensen arriveren. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties: wat houdt deze krachtige cellen gezond en rustig totdat ze nodig zijn, en wat gebeurt er als dat interne beveiligingssysteem faalt? Door te onthullen hoe één eiwit, liver kinase B1 (Lkb1), NK‑cellen beschermt tegen interne chemische schade, wijst het werk op nieuwe manieren om vroege kankerdetectie te versterken zonder deze cruciale verdedigers uit te putten.
Een waak‑schakelaar binnen immuuncellen
NK‑cellen moeten een fijn evenwicht bewaren. Ze hebben genoeg energie nodig om in actie te komen, maar niet zoveel dat ze overactief, uitgeput of afstervend worden. De auteurs laten zien dat Lkb1 fungeert als een belangrijke interne “waak‑schakelaar” die NK‑cellen helpt in een rustige, paraat‑toestand te blijven. Met meerdere genetisch gemodificeerde muismodellen verwijderden ze Lkb1 selectief uit NK‑cellen in verschillende ontwikkelingsstadia. Hoe ze het ook deden, het resultaat was opvallend: NK‑cellen raakten schaars in veel organen, bleven hangen in onrijpe stadia en verloren de oppervlakte‑kenmerken die normaal gesproken gereedheid signaleren. Deze effecten waren cell‑intrinsiek, wat betekent dat ze voortkwamen uit problemen binnen de NK‑cellen zelf en niet uit hun omgeving.
Wanneer cellair onderhoud faalt
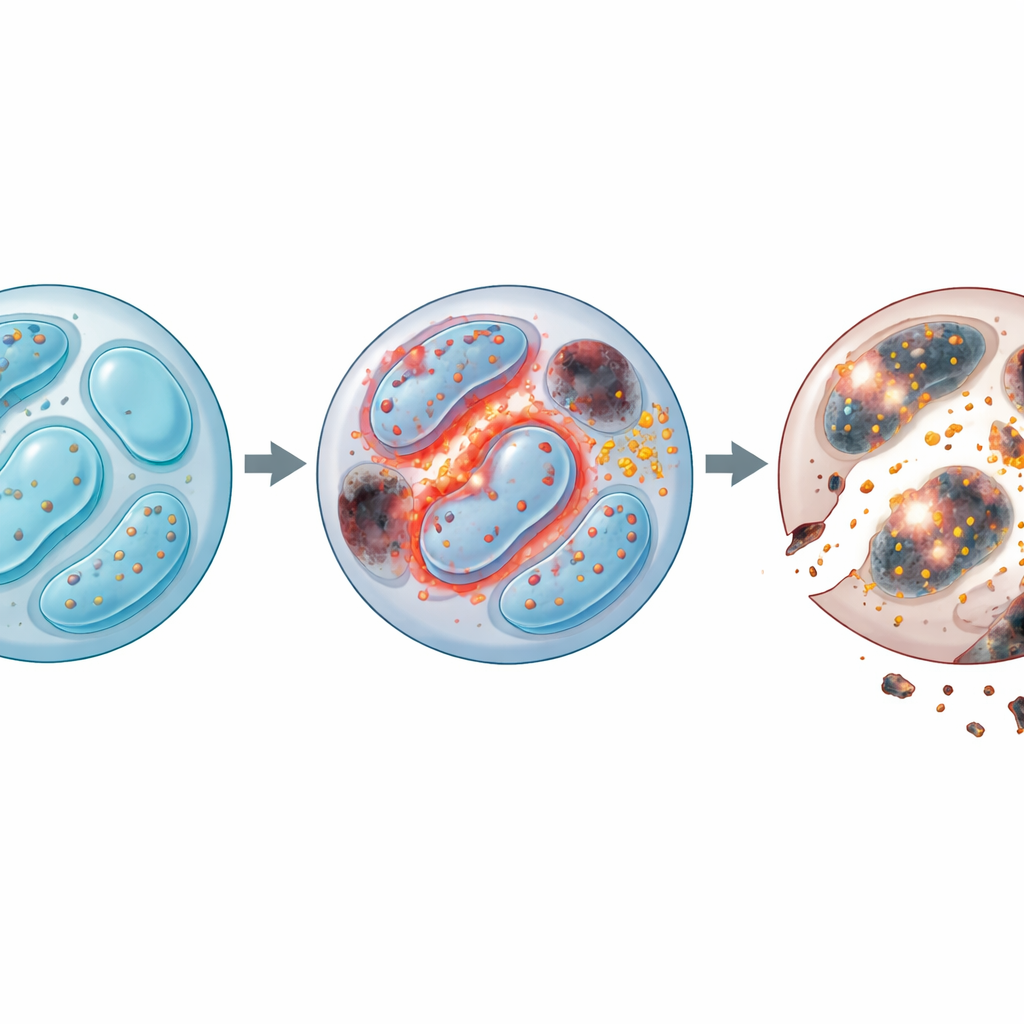
Dieper gravend onderzochten de onderzoekers welke genen veranderden wanneer Lkb1 ontbrak. Duizenden genen die betrokken zijn bij energiegebruik, celdeling, afvalrecycling en celdood werden gewijzigd. Vooral lieten NK‑cellen zonder Lkb1 een falende autofagie zien, het cellulaire huishoudsysteem dat versleten onderdelen zoals beschadigde mitochondriën opruimt. Onder normale omstandigheden voorkomt deze schoonmaakdat potentieel schadelijke bijproducten zich ophopen. Zonder Lkb1 stokte de autofagie: cellen bouwden extra mitochondriën op met abnormaal hoge membraanpotentiaal, en deze defecte structuren spuugden grote hoeveelheden reactieve zuurstofsoorten (ROS) uit — onstabiele moleculen die eiwitten, vetten en DNA kunnen beschadigen. Zelfs hoewel Lkb1‑deficiënte NK‑cellen probeerden te compenseren door meer te delen, stierven ze vaker, wat onthult dat overleving, niet groei, het kernprobleem was.
IJzerstapeling en een dubbele klap van celdood
De problemen hielden niet op bij ROS. De onderzoekers vonden dat NK‑cellen zonder Lkb1 ook de controle over ijzerbalans verloren. Deze cellen hamsterden ijzer en verhoogden een belangrijk ijzer‑importreceptor, wat op zijn beurt de vorming van toxische “lipide‑ROS” aanwakkerde die celmembranen aanvallen. Dit patroon is kenmerkend voor ferroptose, een ijzerafhankelijke vorm van celdood. Door cellen te behandelen met een ijzerbindend middel of een ferroptose‑remmer konden de onderzoekers veel van het overlevingsdefect herstellen. Tegelijkertijd waren klassieke geprogrammeerde celdoodroutes ook overactief: beschermende eiwitten daalden, uitvoerende enzymen stegen, en het blokkeren van caspases (de enzymen die apoptose aandrijven) verbeterde de levensvatbaarheid. Het combineren van ijzerverwijdering en caspase‑inhibitie gaf een additief effect, wat aangeeft dat NK‑cellen zonder Lkb1 door twee onafhankelijke maar convergerende doodsroutes worden getroffen—ijzergedreven membraanschade en mitochondria‑gedreven apoptose.
Uitgeputte strijders en verzwakte tumorpatrouille
Buiten overleving moeten NK‑cellen effectief functioneren. Lkb1‑deficiënte NK‑cellen produceerden minder van het sleutelafweermolecuul interferon‑γ en vertoonden hogere niveaus van remmende “handremmen” aan hun oppervlak, zoals PD‑1 en TIGIT — kenmerken die geassocieerd zijn met uitgeputte immuuncellen die gezien worden bij chronische infecties en kanker. Antioxidantbehandelingen die ROS verminderden of ferroptose blokkeerden verlaagden deze uitputtingsmarkers en herstelden gedeeltelijk de NK‑celactiviteit. In levende muizen waren de gevolgen duidelijk: dieren zonder Lkb1 in NK‑cellen waren veel slechter in het afstoten van cellen die normale “zelf”‑signalen misten en minder goed in het opruimen van NK‑gevoelige tumoren of het voorkomen van uitzaaiing van melanoom naar de longen. Het verwijderen van Lkb1 eerder in de NK‑celontwikkeling veroorzaakte nog ernstiger uitval, wat het belang ervan vanaf de vroegste stadia benadrukt.
Wat dit betekent voor toekomstige therapieën
Voor velen is Lkb1 vooral bekend als een tumorsuppressor in kankercellen, maar dit werk benadrukt zijn even cruciale rol binnen immuuncellen. Lkb1 houdt NK‑cellen metabolisch in balans, onderhoudt hun interne schoonmaaksystemen, voorkomt ijzer‑ en ROS‑overbelasting en beschermt ze tegen dubbele doodspaden en uitputting. Interessant is dat gebruikelijke energie‑sensorroutes die in andere cellen aan Lkb1 gekoppeld zijn — AMPK‑activatie en mTORC1‑remming — het defect niet konden herstellen wanneer farmacologisch aangepast, wat suggereert dat NK‑cellen op specifieke downstream‑circuits vertrouwen. Voor de niet‑specialist is de conclusie dat NK‑cellen zelf bescherming nodig hebben tegen oxidatieve en ijzer‑gedreven stress om effectieve kankewachters te blijven. In plaats van Lkb1 direct te veranderen, wat elders kankergerelateerde risico’s kan meebrengen, zouden therapieën die de redox‑ en ijzerbalans in NK‑cellen fijner afstemmen mogelijk het eigen alarmeringssysteem van het lichaam tegen tumoren kunnen versterken.
Bronvermelding: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Trefwoorden: natural killer‑cellen, LKB1, oxidatieve stress, ijzerhomeostase, kanker‑immunosurveillance