Clear Sky Science · fr
La kinase hépatique B1 préserve la survie des cellules NK en régulant l’homéostasie redox
Pourquoi nos « premiers intervenants » immunitaires ont aussi besoin de protection
Les cellules tueuses naturelles (NK) sont les forces d’intervention rapide de l’organisme, à l’affût des cellules infectées par des virus et des cellules cancéreuses avant l’arrivée des autres défenses immunitaires. Cette étude pose une question apparemment simple mais aux grandes implications : qu’est‑ce qui maintient ces cellules puissantes en bonne santé et en veille jusqu’à ce qu’elles soient nécessaires, et que se passe‑t‑il lorsque ce système de sécurité interne fait défaut ? En révélant comment une seule protéine, la kinase hépatique B1 (Lkb1), protège les cellules NK des dommages chimiques internes, le travail ouvre des pistes pour renforcer la surveillance précoce du cancer sans épuiser ces défenseurs cruciaux.
Un commutateur gardien à l’intérieur des cellules immunitaires
Les cellules NK doivent trouver un juste équilibre. Elles ont besoin d’assez d’énergie pour intervenir, mais pas au point de devenir hyperactives, épuisées ou de mourir. Les auteurs montrent que Lkb1 joue le rôle d’un « commutateur gardien » interne clé qui aide les cellules NK à rester dans un état calme et prêt. En utilisant plusieurs modèles murins génétiquement modifiés, ils ont supprimé sélectivement Lkb1 des cellules NK à différents stades de leur développement. Quel que soit le modèle, le résultat fut net : les cellules NK se raréfiaient dans de nombreux organes, restaient bloquées à des stades immatures et perdaient les marqueurs de surface qui signalent normalement leur pleine capacité à combattre. Ces effets étaient intrinsèques aux cellules, c’est‑à‑dire qu’ils provenaient de dysfonctionnements à l’intérieur des NK elles‑mêmes plutôt que de leur environnement.
Quand le ménage cellulaire se dérègle
En approfondissant, l’équipe a examiné les gènes dont l’expression changeait en l’absence de Lkb1. Des milliers de gènes liés à l’utilisation de l’énergie, à la division cellulaire, au recyclage des déchets et à la mort cellulaire étaient altérés. En particulier, les cellules NK dépourvues de Lkb1 présentaient une défaillance de l’autophagie, le système de ménage cellulaire qui élimine les composants usés comme les mitochondries endommagées. Dans des conditions normales, ce nettoyage empêche l’accumulation de sous‑produits nocifs. Sans Lkb1, l’autophagie s’arrêtait : les cellules accumulaient des mitochondries en excès avec un potentiel de membrane anormalement élevé, et ces structures défectueuses produisaient de grandes quantités d’espèces réactives de l’oxygène (ROS) — des molécules instables susceptibles d’endommager protéines, lipides et ADN. Même si les NK déficientes en Lkb1 tentaient de compenser en se divisant davantage, elles mouraient à des taux plus élevés, révélant que le problème principal était la survie, et non la prolifération.
Surcharge en fer et double mécanisme de mort cellulaire
Le problème ne s’arrêtait pas aux ROS. Les chercheurs ont constaté que les cellules NK sans Lkb1 perdaient aussi le contrôle de l’équilibre du fer. Ces cellules accumulaient du fer et surexprimaient un récepteur clé d’importation du fer, ce qui favorisait la formation de « ROS lipidiques » toxiques qui attaquent les membranes cellulaires. Ce profil est caractéristique de la ferroptose, une forme de mort cellulaire dépendante du fer. En traitant les cellules avec un principe actif chélateur de fer ou un inhibiteur de la ferroptose, l’équipe a pu corriger une grande partie du défaut de survie. Parallèlement, les voies classiques de mort cellulaire programmée étaient également hyperactives : les protéines protectrices diminuaient, les enzymes exécutrices augmentaient, et le blocage des caspases (les enzymes qui pilotent l’apoptose) améliorait la viabilité. L’association d’un enlèvement du fer et d’une inhibition des caspases apportait un bénéfice additif, indiquant que les cellules NK privées de Lkb1 subissent deux voies de mort indépendantes mais convergentes — des dommages membranaires induits par le fer et une apoptose d’origine mitochondriale.
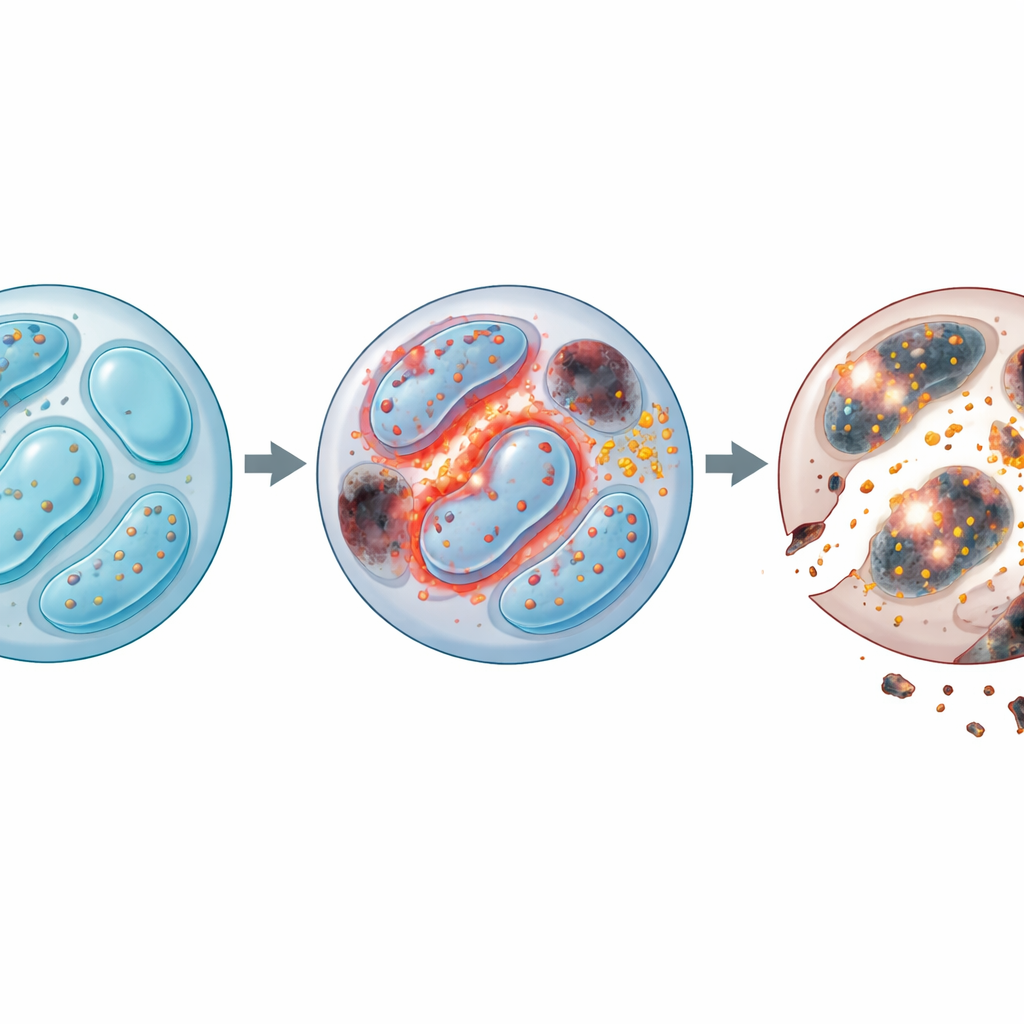
Soldats épuisés et patrouille tumorale affaiblie
Au‑delà de leur survie, les cellules NK doivent rester fonctionnelles. Les NK déficientes en Lkb1 produisaient moins de la molécule clé de défense interféron‑γ et affichaient des niveaux plus élevés de « freins » inhibiteurs à leur surface, tels que PD‑1 et TIGIT — des caractéristiques associées à des cellules immunitaires épuisées observées lors d’infections chroniques et de cancers. Des traitements antioxydants réduisant les ROS ou bloquant la ferroptose diminuaient ces marqueurs d’épuisement et restaurait partiellement l’activité des NK. In vivo, les conséquences furent nettes : les souris dépourvues de Lkb1 dans leurs NK étaient beaucoup moins aptes à rejeter des cellules dépourvues de signaux normaux de « soi » et peinaient à éliminer des tumeurs sensibles aux NK ou à empêcher la dissémination de mélanomes vers les poumons. La suppression précoce de Lkb1 durant le développement des NK entraînait des défaillances encore plus sévères, soulignant son importance dès les stades initiaux.
Que cela signifie pour les thérapies futures
Pour beaucoup, Lkb1 est surtout connu comme une protéine suppresseur de tumeur dans les cellules cancéreuses, mais ce travail souligne son rôle tout aussi critique à l’intérieur des cellules immunitaires. Lkb1 maintient l’équilibre métabolique des NK, préserve leurs systèmes de nettoyage internes, empêche la surcharge en fer et en ROS, et les protège de voies de mort et d’épuisement doubles. Il est intéressant de noter que les voies classiques de détection énergétique associées à Lkb1 dans d’autres cellules — activation d’AMPK et inhibition de mTORC1 — n’ont pas permis de réparer les dommages lorsqu’elles ont été modulées pharmacologiquement, laissant entendre que les NK s’appuient sur des circuits en aval distincts. Pour le lecteur non spécialiste, la conclusion est que les NK ont elles‑mêmes besoin d’être protégées contre le stress oxydatif et induit par le fer pour rester des sentinelles efficaces contre le cancer. Plutôt que de modifier directement Lkb1, ce qui pourrait comporter des risques oncogéniques ailleurs, des thérapies visant à ajuster finement l’équilibre redox et du fer dans les NK pourraient un jour renforcer le système d’alerte précoce de l’organisme contre les tumeurs.
Citation: Meng, W., Luo, L., Xiao, Z. et al. Liver kinase B1 maintains natural killer cell survival by regulating redox homeostasis. Cell Death Dis 17, 413 (2026). https://doi.org/10.1038/s41419-026-08629-w
Mots-clés: cellules tueuses naturelles, LKB1, stress oxydatif, homéostasie du fer, immunosurveillance du cancer