Clear Sky Science · tr
ACAD9’un sitozolik ikincil işlevi: TRAF6 aracılı osteoklastogenezin baskılanması ve osteoporozdan korunma
Kemikler Neden Yaşla Zayıflar
Kırık kalçalar ve kırılgan omurlar, yaşlanmanın en korkulan sorunları arasındadır; ancak bu kırıkların arkasındaki gizli hücresel biyoloji laboratuvar dışındayken nadiren konuşulur. Bu çalışma, kemiklerimizi güçlü tutmada mitokondriyal bir protein olan ACAD9’un şaşırtıcı bir rolünü ortaya koyuyor. Hem hücrenin enerji merkezlerinde hem de hücresel sinyal mekanizmalarında görev yaparak ACAD9, kemik yiyen hücreleri dizginlemeye yardımcı oluyor ve osteoporozu önlemeye yönelik yeni bir yol açabilir.
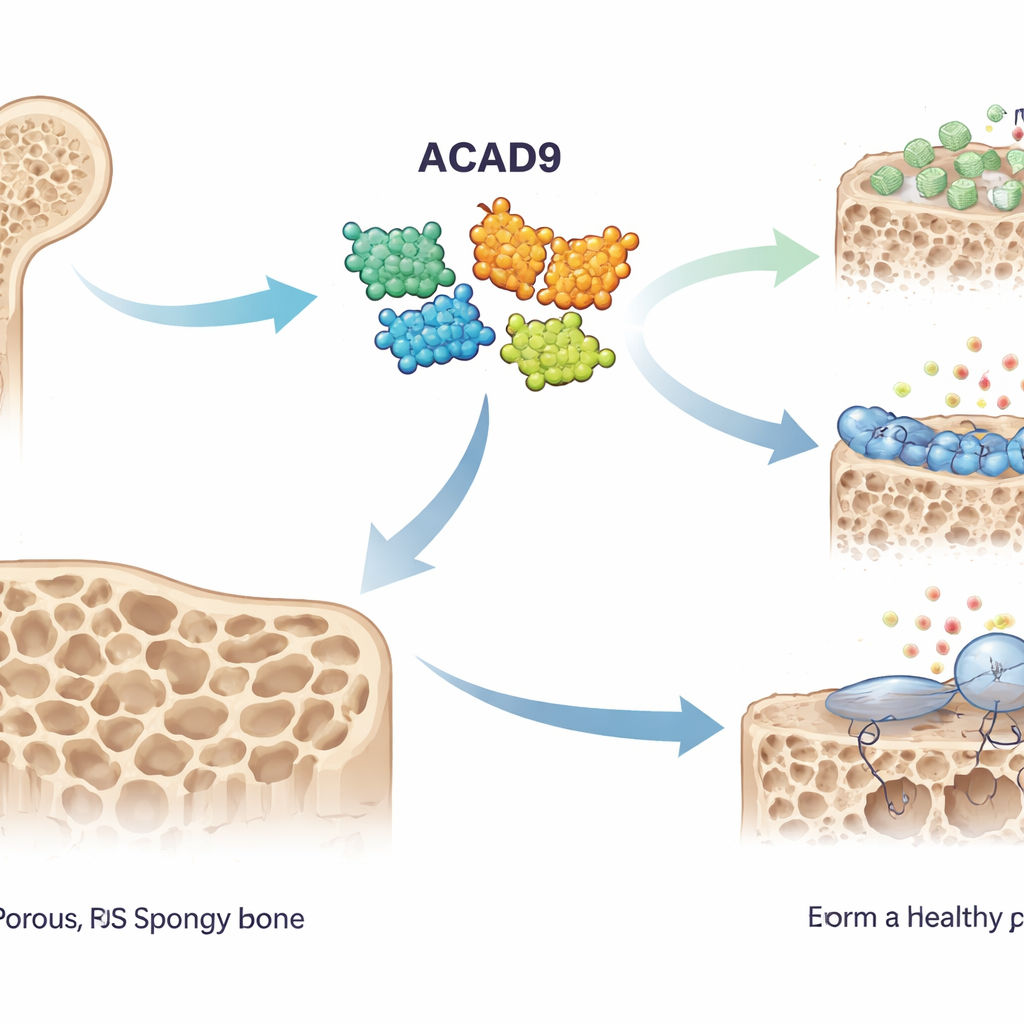
Kemik İnşa Edenler ve Kemik Yiyenler
Sağlıklı kemik, birbirine zıt iki hücre takımı tarafından sürekli yeniden düzenlenir: kemiği inşa eden osteoblastlar ve onu çözen osteoklastlar. Osteoporozda denge kemik yiyenler lehine kayar ve iskeleti ince, kırılgan bırakır. Osteoklastlar, RANKL adı verilen bir sinyalin öncül hücrelerdeki reseptörüne bağlanmasıyla aktive olur; bu da TRAF6 adlı bir proteini devreye sokar. Bu sıralama kimyasal kaskadlar ve reaktif oksijen türlerinde (genellikle ROS olarak anılan yüksek reaktif moleküller) bir patlama tetikler; bunlar öncüllerin birleşip büyük, kemik rezorbe eden hücrelere dönüşmesini sağlar. Yazarlar, mitokondrial enerji üretimindeki rolüyle tanınan ACAD9’un bu süreci etkileyebileceğini düşündüler.
Strese Karşı Bir Mitokondriyal Koruyucu
Mitokondride ACAD9, kompleks I adı verilen büyük bir protein makinesinin montajına yardımcı olur ve birkaç solunum zinciri kompleksinin düzenli gruplanması olan “süperkompleks”lerin oluşumunu destekler. Bu yapılar enerji üretimini daha verimli hale getirir ve istenmeyen ROS’u sınırlar. Hücre deneylerinde araştırmacılar, osteoklast öncülleri RANKL’ye maruz kalıp olgunlaşmaya başladığında ACAD9 seviyelerinin düştüğünü, kompleks I ve süperkomplekslerin azaldığını ve ROS’un keskin biçimde yükseldiğini buldular. ACAD9’un azaltılması ROS’u daha da artırdı ve osteoklast oluşumunu hızlandırdı; ACAD9’un artırılması ise kompleks I’i geri getirdi, hücresel enerjiyi (ATP) yükseltti, ROS’u azalttı ve osteoklast farklılaşmasını baskıladı. Bir antioksidan ilaçla ROS’un temizlenmesi, ACAD9 kaybının etkilerini yalnızca kısmen geri çevirdi; bu da ACAD9’un başka, mitokondri dışı bir yol üzerinden de etki etmesi gerektiğine işaret ediyor.
Kemik Yiyenlere Karşı Moleküler Bir Fren: ACAD9
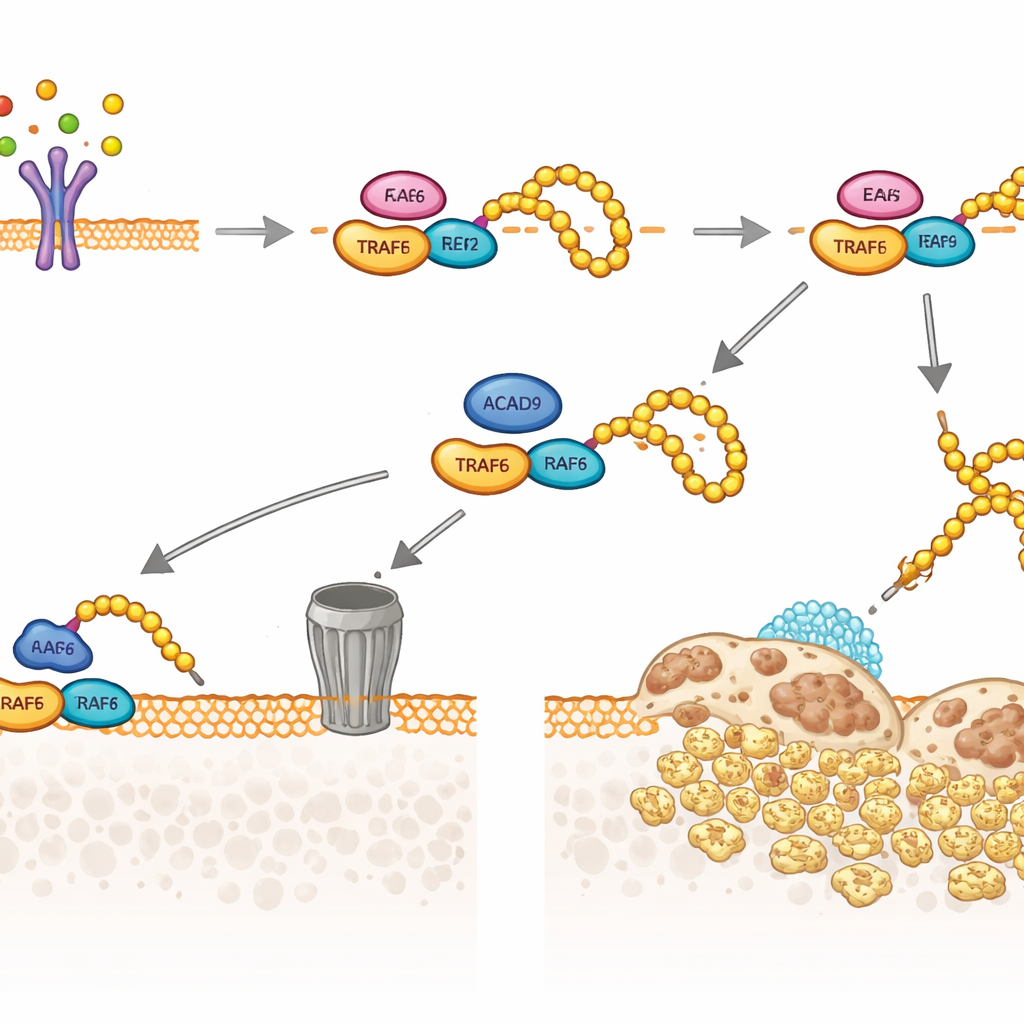
Araştırma ekibi bir sonraki adımda osteoklast genlerini açan RANKL’in ana rölesi olan TRAF6’ya baktı. ACAD9 proteininin bir kısmının mitokondrilerde değil hücre sıvısında yer aldığını ve burada fiziksel olarak TRAF6’ya bağlanabildiğini keşfettiler. Bu bağlanma, TRAF6’nın küçük “ubikitin” etiketlerini takan ortak enzimleriyle olan etkileşimini değiştiriyor. ACAD9 yoksa TRAF6, aşağı akış sinyallerini (osteoklast büyümesini ve kemik rezorpsiyonunu yönlendiren MAPK ve NF‑κB yolları dahil) aktive eden bir iskelet görevi gören bir ubikitin zinciri türüyle (K63 bağlantılı) yoğun şekilde süsleniyor. ACAD9 mevcut olduğunda bu K63 zincirleri azaltılıyor, bunun yerine farklı bir ubikitin zinciri türü (K48‑bağlantılı) tercih ediliyor ve TRAF6 hücrenin protein öğütme mekanizmasında yıkılmak üzere hedefleniyor. Özetle ACAD9 hem TRAF6’nın sinyal verme yeteneğini törpülüyor hem de onun parçalanmasını hızlandırıyor.
Fare Kemiklerinden İnsan Kırıklarına
Bunun canlı bir organizmada nasıl sonuçlandığını görmek için araştırmacılar, osteoklast öncüllerinde özel olarak ACAD9 eksikliği olan fareler ürettiler. Bu hayvanlar yaşlandıkça taramalarda trabeküler kemiğin giderek inceldiği, kemik kirişleri arasındaki boşlukların arttığı ve kemik mimarisinin bozulduğu—osteoporozun tüm belirteçleri—gözlendi. Kemiklerinde daha fazla osteoklast ve daha yüksek düzeyde kemik rezorpsiyon belirteçleri vardı; mitokondriyal kompleks I, süperkompleksler ve ATP azalmıştı. TRAF6 sonrası sinyalleşme molekülleri aşırı aktive olmuş ve ROS üreten enzimler yükselmişti. Önemli olarak, kemik oluşturma aktivitesi büyük ölçüde normal kaldı; bu da aşırı kemik kaybının esas olarak aşırı etkin osteoklastlardan kaynaklandığını gösteriyor. Fare çalışmalarını tamamlayıcı olarak, büyük insan biyobankası verilerinin analizi ACAD9 geninde nadir, zararlı varyantlarla omurga kırık riskinin artışı arasında ilişki buldu; bu da klinik önemi düşündürüyor.
Gelecekteki Tedaviler İçin Ne Anlama Geliyor
Bu bulgular birlikte ACAD9’u osteoporoza karşı iki yönlü bir savunucu olarak sunuyor. Mitokondrilerde verimli enerji üretimini sürdürür ve oksidatif stresi kontrol altında tutar; sitozolde ise osteoklast aktivasyonunun ana anahtarı olan TRAF6’yı ubikitin etiketlerini yeniden şekillendirerek ve yıkımını teşvik ederek bastırır. ACAD9 eksik veya azaldığında kemik yiyen hücreler çoğalır ve kemikler zayıflar. ACAD9’un aktivitesini artıran veya TRAF6 ile etkileşimini taklit eden ilaçlar bu nedenle yaşlanan kemikleri korumak için hücresel metabolizmayı iyileştirme ve aşırı kemik rezorpsiyonunu yatıştırma olmak üzere iki yönlü yeni bir strateji sunabilir.
Atıf: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
Anahtar kelimeler: osteoporoz, osteoklastlar, mitokondri, ubikitinasyon, kemik yenilenmesi