Clear Sky Science · pt
Função citosólica multitarefa da ACAD9: supressão da osteoclastogênese mediada por TRAF6 e proteção contra a osteoporose
Por que os ossos enfraquecem com a idade
Quadris quebrados e colunas frágeis estão entre os problemas mais temidos do envelhecimento, mas a biologia celular por trás dessas fraturas raramente é discutida fora do laboratório. Este estudo revela um papel surpreendente de uma proteína mitocondrial chamada ACAD9 na manutenção da resistência óssea. Atuando tanto nas usinas de energia da célula quanto na maquinaria de sinalização, a ACAD9 ajuda a conter as células que “comem” osso e pode abrir um novo caminho para prevenir a osteoporose.
Construtores e comedores de osso
O osso saudável é remodelado constantemente por duas equipes celulares opostas: os osteoblastos, que constroem osso, e os osteoclastos, que o dissolvem. Na osteoporose, o equilíbrio desloca‑se em favor dos comedores de osso, deixando o esqueleto fino e frágil. Os osteoclastos são ativados quando um sinal chamado RANKL se liga ao seu receptor em células precursoras, ativando uma proteína nomeada TRAF6. Isso, por sua vez, desencadeia cascatas químicas e uma explosão de espécies reativas de oxigênio — moléculas altamente reativas frequentemente chamadas de ROS — que empurram esses precursores a fundir‑se em grandes células capazes de reabsorver osso. Os autores suspeitaram que a ACAD9, conhecida por seu papel na produção de energia mitocondrial, também poderia influenciar esse processo.
Uma guardiã mitocondrial do estresse
No interior das mitocôndrias, a ACAD9 ajuda a montar uma grande máquina proteica chamada complexo I e promove a formação de “supercomplexos”, agrupamentos ordenados de vários complexos da cadeia respiratória. Essas estruturas tornam a produção de energia mais eficiente e limitam ROS indesejadas. Em experimentos celulares, os pesquisadores observaram que quando precursores de osteoclastos foram expostos a RANKL e começaram a amadurecer, os níveis de ACAD9 caíram, o complexo I e os supercomplexos diminuíram, e as ROS aumentaram fortemente. A redução da ACAD9 amplificou ainda mais as ROS e acelerou a formação de osteoclastos, enquanto aumentar a ACAD9 restaurou o complexo I, elevou a energia celular (ATP), reduziu as ROS e atenuou a diferenciação osteoclástica. Eliminar as ROS com um antioxidante reverteu apenas parcialmente os efeitos da perda de ACAD9, sugerindo que a ACAD9 age também por outra via não mitocondrial.
ACAD9 como um freio molecular sobre os comedores de osso
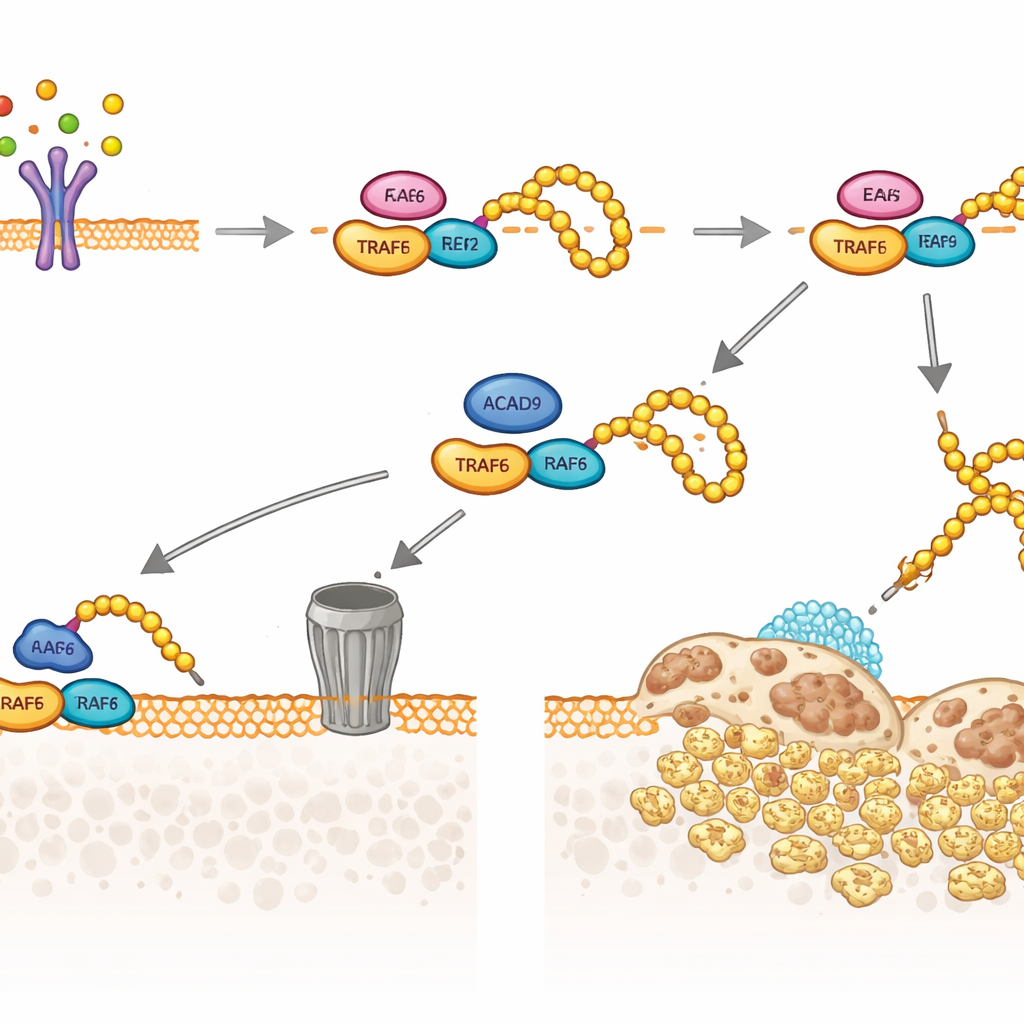
A equipe investigou então o TRAF6, o elo chave que o RANKL usa para ligar os genes osteoclásticos. Eles descobriram que parte da proteína ACAD9 está presente no citosol, em vez de ficar apenas nas mitocôndrias, onde pode se ligar fisicamente ao TRAF6. Essa interação altera como o TRAF6 se relaciona com suas enzimas parceiras que adicionam pequenas etiquetas de “ubiquitina”. Sem ACAD9, o TRAF6 torna‑se fortemente decorado com um tipo de cadeia de ubiquitina (ligada via K63), que atua como um andaime para ativar sinais a jusante, incluindo as vias MAPK e NF‑κB que impulsionam o crescimento dos osteoclastos e a reabsorção óssea. Com ACAD9 presente, essas cadeias K63 são contidas, enquanto outro tipo de cadeia de ubiquitina (ligada via K48) é favorecido, direcionando o TRAF6 para destruição na maquinaria de degradação proteica da célula. Em essência, a ACAD9 tanto enfraquece a capacidade de sinalização do TRAF6 quanto acelera sua remoção.
Dos ossos de camundongo às fraturas humanas
Para avaliar como isso se manifesta em um organismo vivo, os pesquisadores geraram camundongos que carecem de ACAD9 especificamente nos precursores de osteoclastos. À medida que esses animais envelheceram, exames revelaram um afinamento progressivo do osso trabecular, maior espaçamento entre as traves ósseas e arquitetura óssea prejudicada — todos sinais de osteoporose. Seus ossos continham mais osteoclastos e níveis mais altos de marcadores de reabsorção óssea, enquanto o complexo I mitocondrial, os supercomplexos e o ATP foram reduzidos. Moléculas de sinalização a jusante do TRAF6 estavam hiperativadas, e enzimas produtoras de ROS estavam elevadas. Importante, a atividade formadora de osso permaneceu em grande parte normal, mostrando que a perda óssea excessiva decorreu principalmente de osteoclastos hiperativos. Complementando o trabalho em camundongos, a análise de grandes bancos de dados humanos associou variantes raras e deletérias no gene ACAD9 a um risco maior de fraturas vertebrais, sugerindo relevância clínica.
O que isso significa para terapias futuras
Em conjunto, os achados apresentam a ACAD9 como uma defensora dupla contra a osteoporose. Nas mitocôndrias, ela mantém a produção eficiente de energia e controla o estresse oxidativo; no citosol, reprime o TRAF6, o interruptor mestre da ativação osteoclástica, remodelando suas marcas de ubiquitina e promovendo sua degradação. Quando a ACAD9 está ausente ou reduzida, os comedores de osso se multiplicam e os ossos enfraquecem. Fármacos que aumentem a atividade da ACAD9 ou imitem sua interação com o TRAF6 podem, portanto, oferecer uma nova estratégia dupla para proteger os ossos envelhecidos — simultaneamente melhorando o metabolismo celular e silenciosamente reduzindo a reabsorção óssea excessiva.
Citação: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
Palavras-chave: osteoporose, osteoclastos, mitocôndrias, ubiquitinação, remodelação óssea