Clear Sky Science · ru
Цитозольная функция ACAD9 как вторая роль: подавление TRAF6‑опосредованного образования остеокластов и защита от остеопороза
Почему кости слабеют с возрастом
Переломы шейки бедра и ломкая позвоночная кость — одни из самых пугающих последствий старения, но скрытая клеточная биология, лежащая в основе этих переломов, редко обсуждается вне лабораторий. В этом исследовании обнаружена неожиданная роль митохондриального белка ACAD9 в поддержании прочности костей. Действуя как внутри клеточных «электростанций», так и в сигнальной системе клетки, ACAD9 сдерживает клетки, разрушающие кость, и может открыть новый путь для предотвращения остеопороза.
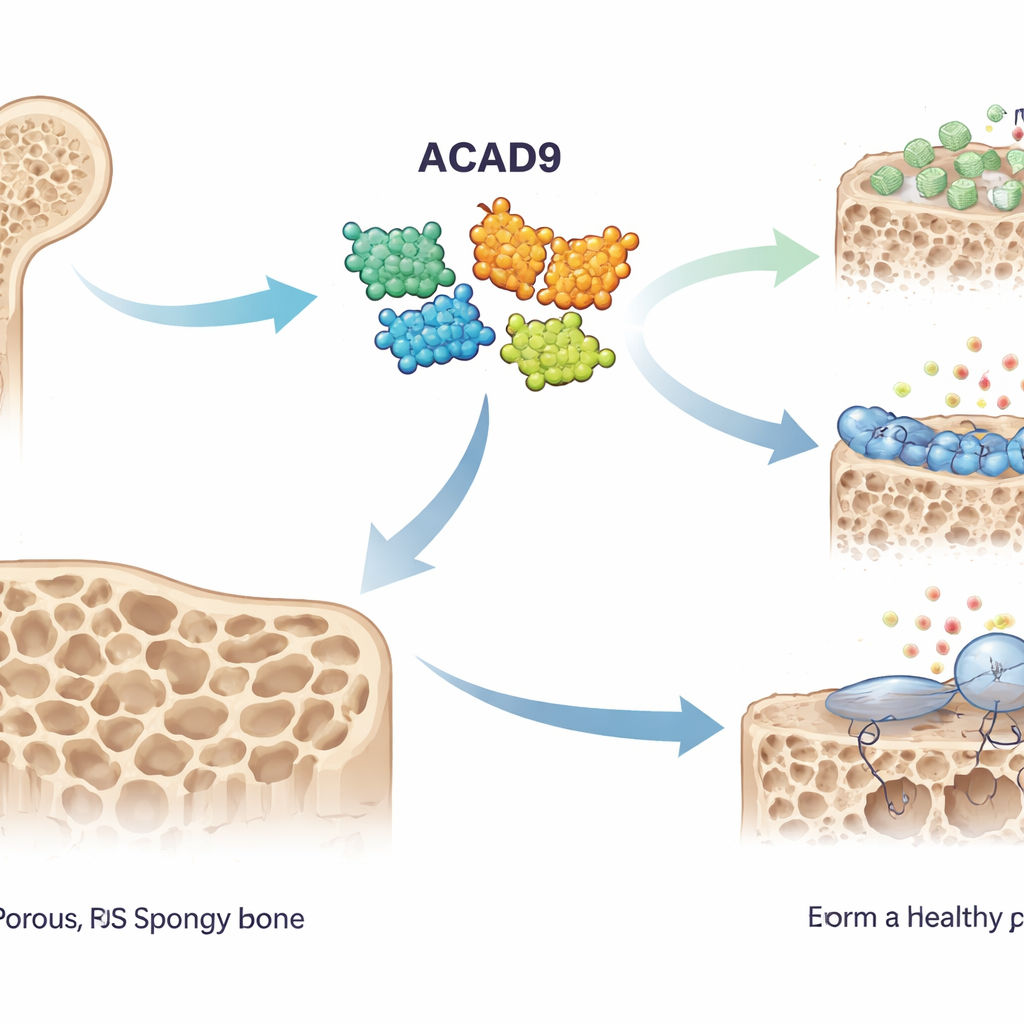
Костеобразователи и костеедатели
Здоровая кость постоянно перестраивается двумя противоположными группами клеток: остеобластами, строящими кость, и остеокластами, её разрушающими. При остеопорозе равновесие смещается в сторону «костеедов», в результате скелет становится тонким и хрупким. Остеокласты активируются, когда сигнал под названием RANKL связывается с его рецептором на предшественниках, включая активацию белка TRAF6. Это, в свою очередь, запускает химические каскады и всплеск реактивных форм кислорода (ROS) — высокореактивных молекул, которые стимулируют слияние предшественников в крупные клетки, разрушающие кость. Авторы предположили, что ACAD9, известный своей ролью в митохондриальном энергообеспечении, может также влиять на этот процесс.
Митохондриальный страж стресса
В митохондриях ACAD9 помогает собирать большой белковый комплекс I и способствует формированию «суперкомплексов» — упорядоченных групп нескольких комплексов дыхательной цепи. Эти структуры повышают эффективность выработки энергии и ограничивают нежелательные ROS. В клеточных экспериментах исследователи обнаружили, что при экспозиции предшественников остеокластов RANKL и их созревании уровень ACAD9 падал, комплекс I и суперкомплексы сокращались, а ROS резко возрастали. Понижение экспрессии ACAD9 ещё сильнее усиливало ROS и ускоряло образование остеокластов, тогда как повышение ACAD9 восстанавливало комплекс I, увеличивало клеточную энергию (АТФ), снижало ROS и замедляло дифференцировку остеокластов. Удаление ROS с помощью антиоксидантного препарата лишь частично обращало эффекты утраты ACAD9, что указывает на то, что ACAD9 действует и другим, немитохондриальным путём.
ACAD9 как молекулярный тормоз для «костеедов»
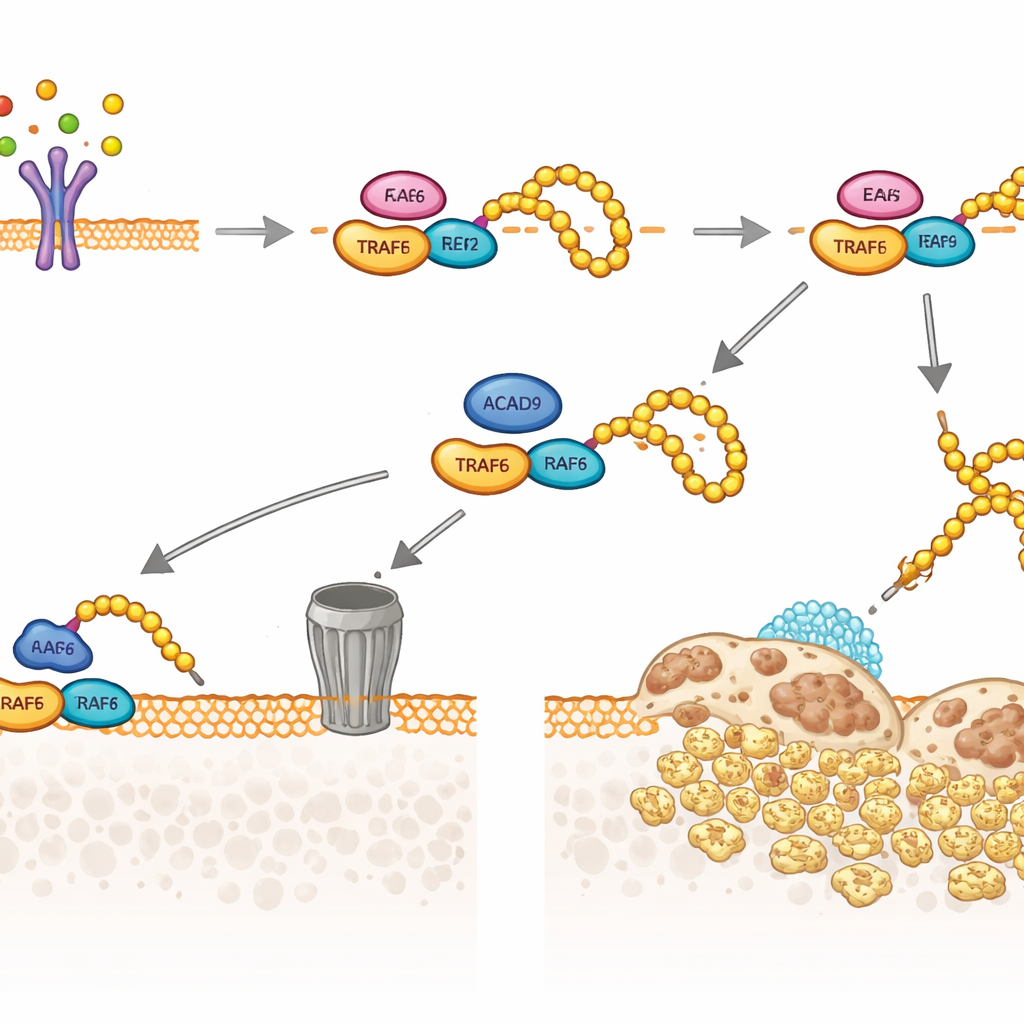
Далее исследователи обратились к TRAF6 — ключевому посреднику, через который RANKL включает гены остеокластов. Они обнаружили, что часть ACAD9 локализуется не в митохондриях, а в цитозоле, где он может физически связываться с TRAF6. Это связывание изменяет взаимодействие TRAF6 с его партнёрными ферментами, прикрепляющими небольшие «убиквитиновые» метки. При отсутствии ACAD9 TRAF6 сильно украшен одним типом убиквитиновой цепочки (связи через остаток K63), которая служит каркасом для активации последующих сигналов, включая пути MAPK и NF‑κB, стимулирующие рост остеокластов и резорбцию кости. В присутствии ACAD9 эти K63‑цепочки ограничиваются, тогда как преимущество получает другой тип цепей (K48‑связанные), нацеливающих TRAF6 на разрушение в протеолитической системе клетки. Иными словами, ACAD9 одновременно ослабляет сигнальную активность TRAF6 и ускоряет его удаление.
От костей мыши к переломам у человека
Чтобы проверить это в живом организме, учёные создали мышей с дефицитом ACAD9 специфически в предшественниках остеокластов. С возрастом у этих животных томография показала постепенное истончение губчатой кости, увеличение расстояния между костными балками и ухудшение архитектуры — всё признаки остеопороза. В их костях оказалось больше остеокластов и выше уровни маркеров резорбции кости, в то время как митохондриальный комплекс I, суперкомплексы и АТФ были снижены. Сигнальные молекулы ниже по цепочке от TRAF6 оказались гиперактивированы, а ферменты, производящие ROS, — повышены. Важно, что активность остеобластов осталась в основном нормальной, что показывает: избыточная потеря кости возникала главным образом из‑за сверхактивных остеокластов. Дополняя данные на мышах, анализ больших человеческих биобанков связал редкие повреждающие варианты гена ACAD9 с повышенным риском переломов позвонков, что указывает на клиническую значимость.
Что это значит для будущих терапий
В совокупности результаты представляют ACAD9 как двойного защитника от остеопороза. В митохондриях он поддерживает эффективное производство энергии и контролирует окислительный стресс; в цитозоле он подавляет TRAF6, главный переключатель активации остеокластов, изменяя его убиквитиновые метки и способствуя его разрушению. При нехватке ACAD9 клетки, разрушающие кость, размножаются, и кости слабеют. Лекарства, усиливающие активность ACAD9 или имитирующие его взаимодействие с TRAF6, поэтому могли бы предложить новую двухуровневую стратегию защиты стареющих костей — одновременно улучшая клеточный метаболизм и подавляя избыточную резорбцию кости.
Цитирование: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
Ключевые слова: остеопороз, остеокласты, митохондрии, убиквитинирование, ремоделирование кости