Clear Sky Science · it
Funzione citosolica moonlighting di ACAD9: soppressione dell’osteoclastogenesi mediata da TRAF6 e protezione contro l’osteoporosi
Perché le ossa si indeboliscono con l’età
Fratture del femore e colonne vertebrali fragili sono tra i problemi dell’invecchiamento più temuti, tuttavia la biologia cellulare nascosta dietro a queste fratture è raramente discussa al di fuori dei laboratori. Questo studio svela un ruolo sorprendente di una proteina mitocondriale chiamata ACAD9 nel mantenere le nostre ossa robuste. Agendo sia all’interno delle centrali energetiche della cellula sia nei meccanismi di segnalazione cellulare, ACAD9 contribuisce a contenere le cellule che mangiano l’osso e potrebbe aprire una nuova strada per prevenire l’osteoporosi.
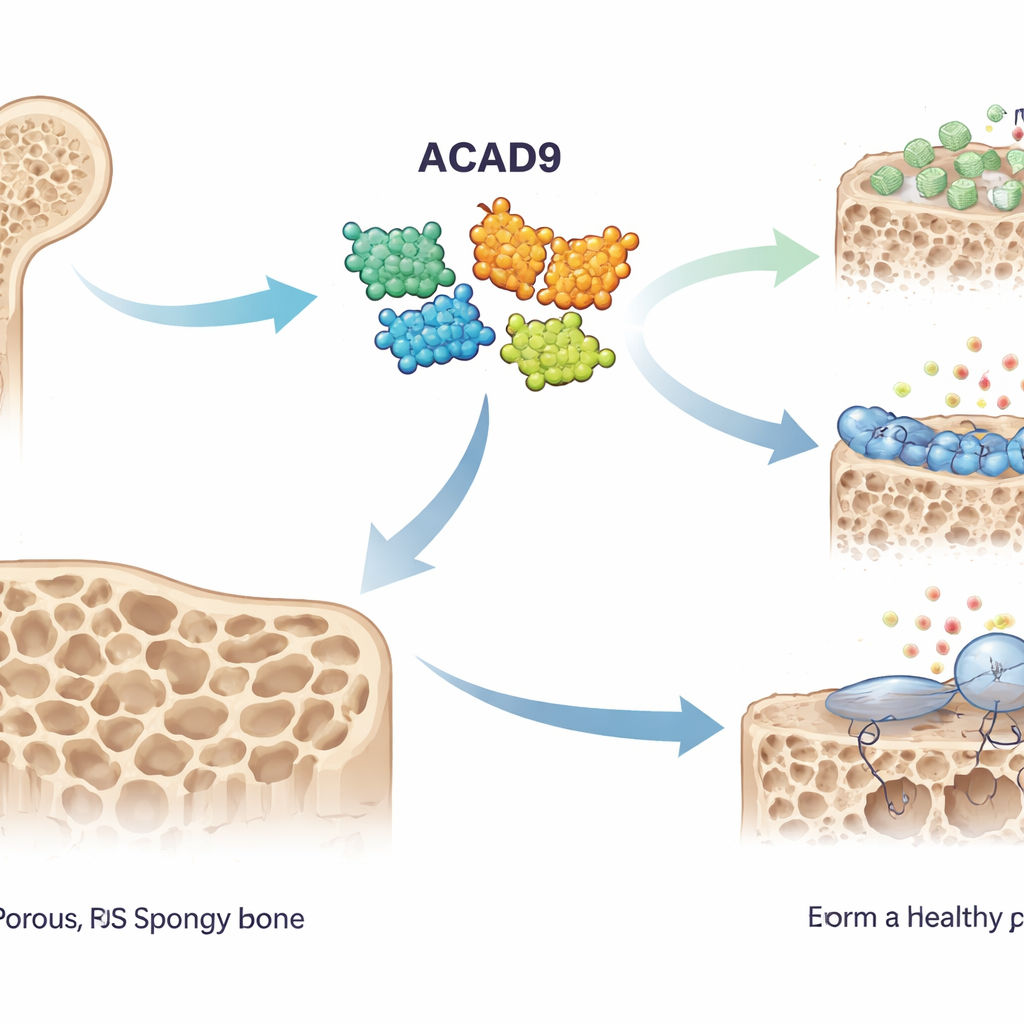
Costruttori e divoratori di osso
L’osso sano viene costantemente rimodellato da due squadre cellulari opposte: gli osteoblasti che costruiscono osso e gli osteoclasti che lo dissolvono. Nell’osteoporosi, l’equilibrio si sposta verso i divoratori d’osso, lasciando lo scheletro sottile e fragile. Gli osteoclasti si attivano quando un segnale chiamato RANKL si lega al suo recettore sulle cellule precursori, attivando una proteina chiamata TRAF6. Questa a sua volta innesca cascate chimiche e un’esplosione di specie reattive dell’ossigeno — molecole altamente reattive spesso indicate come ROS — che spingono quei precursori a fondersi in grandi cellule capaci di riassorbire l’osso. Gli autori ipotizzavano che ACAD9, nota per il suo ruolo nella produzione energetica mitocondriale, potesse influenzare anche questo processo.
Un guardiano mitocondriale dello stress
All’interno dei mitocondri, ACAD9 aiuta ad assemblare una grande macchina proteica chiamata complesso I e favorisce la formazione di “supercomplessi”, raggruppamenti ordinati di più complessi della catena respiratoria. Queste strutture rendono la produzione di energia più efficiente e limitano la generazione indesiderata di ROS. In esperimenti cellulari, i ricercatori hanno osservato che quando i precursori degli osteoclasti venivano esposti a RANKL e iniziavano a maturare, i livelli di ACAD9 diminuivano, complesso I e supercomplessi calavano e i ROS aumentavano nettamente. L’abbattimento di ACAD9 amplificava ulteriormente i ROS e accelerava la formazione degli osteoclasti, mentre aumentare ACAD9 ripristinava il complesso I, incrementava l’energia cellulare (ATP), riduceva i ROS e attenuava la differenziazione osteoclastica. La rimozione dei ROS con un farmaco antiossidante invertiva solo in parte gli effetti della perdita di ACAD9, suggerendo che ACAD9 agisca anche attraverso una via non mitocondriale.
ACAD9 come freno molecolare sugli osteoclasti
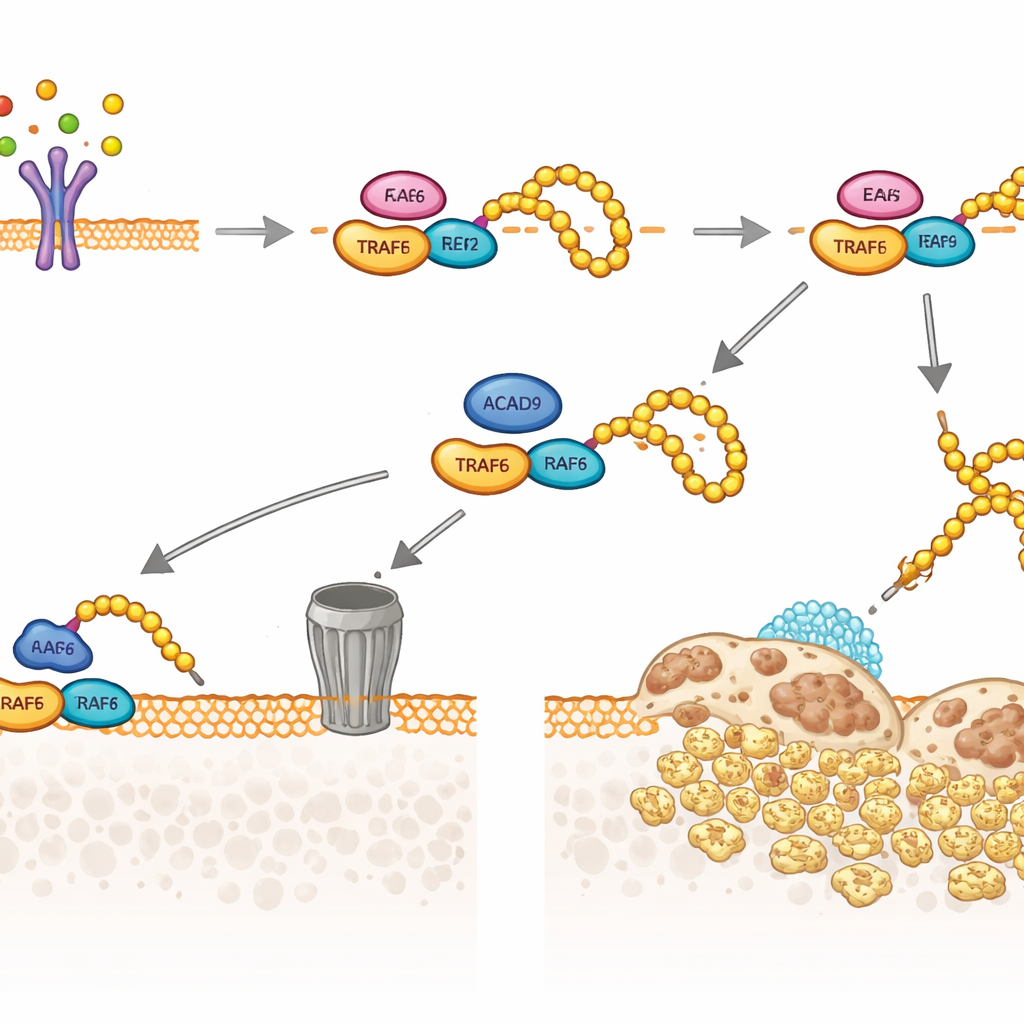
Il gruppo ha quindi esaminato TRAF6, il relè chiave che RANKL usa per attivare i geni degli osteoclasti. Hanno scoperto che una frazione di ACAD9 si trova nel citosol anziché nei mitocondri, dove può legarsi fisicamente a TRAF6. Questo legame altera il modo in cui TRAF6 interagisce con gli enzimi partner che attaccano piccole etichette di “ubiquitina”. In assenza di ACAD9, TRAF6 viene ampiamente decorato con un tipo di catena di ubiquitina (collegata tramite la posizione K63), che funge da impalcatura per attivare segnali a valle, inclusi i percorsi MAPK e NF‑κB che promuovono la crescita degli osteoclasti e il riassorbimento osseo. In presenza di ACAD9, queste catene K63 sono contenute, mentre è favorita un’altra forma di catena ubiquitina (legata via K48), che indirizza TRAF6 alla degradazione presso la macchina cellulare di demolizione delle proteine. In sostanza, ACAD9 sia attenua la capacità di segnalazione di TRAF6 sia ne accelera lo smaltimento.
Dalle ossa dei topi alle fratture umane
Per valutare l’effetto in un organismo vivente, i ricercatori hanno creato topi privi di ACAD9 specificamente nei precursori degli osteoclasti. Con l’età, le scansioni degli animali hanno rivelato un progressivo assottigliamento dell’osso trabecolare, un aumento degli spazi tra le travi ossee e una peggiore architettura ossea — tutti segni caratteristici dell’osteoporosi. Le loro ossa presentavano più osteoclasti e livelli più alti di marcatori del riassorbimento osseo, mentre il complesso I mitocondriale, i supercomplessi e l’ATP risultavano ridotti. Le molecole di segnalazione a valle di TRAF6 erano iperattivate e gli enzimi che producono ROS erano aumentati. È importante che l’attività di formazione ossea fosse in larga parte normale, indicando che la perdita ossea eccessiva derivava principalmente dall’iperattività degli osteoclasti. A complemento dei dati murini, l’analisi di grandi biobanche umane ha collegato varianti rare e dannose nel gene ACAD9 a un rischio maggiore di fratture vertebrali, suggerendo rilevanza clinica.
Cosa significa per le terapie future
Globalmente, i risultati presentano ACAD9 come un doppio difensore contro l’osteoporosi. Nei mitocondri mantiene una produzione energetica efficiente e controlla lo stress ossidativo; nel citosol frena TRAF6, l’interruttore maestro per l’attivazione degli osteoclasti, rimodellandone le etichette di ubiquitina e promuovendone la degradazione. Quando ACAD9 manca o è ridotto, le cellule che mangiano l’osso si moltiplicano e le ossa si indeboliscono. Farmaci che aumentino l’attività di ACAD9 o ne imitino l’interazione con TRAF6 potrebbero dunque offrire una nuova strategia a doppio binario per proteggere le ossa invecchianti — migliorando contemporaneamente il metabolismo cellulare e attenuando il riassorbimento osseo eccessivo.
Citazione: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
Parole chiave: osteoporosi, osteoclasti, mitocondri, ubiquitinazione, rimodellamento osseo