Clear Sky Science · fr
Fonction cytosolique « moonlighting » de l'ACAD9 : suppression de l'ostéoclastogenèse médiée par TRAF6 et protection contre l'ostéoporose
Pourquoi les os s’affaiblissent avec l’âge
Les fractures de la hanche et l’effondrement des vertèbres figurent parmi les problèmes les plus redoutés du vieillissement, pourtant la biologie cellulaire qui sous‑tend ces lésions est rarement expliquée en dehors des laboratoires. Cette étude révèle un rôle surprenant d’une protéine mitochondriale appelée ACAD9 dans le maintien de la solidité osseuse. En agissant à la fois à l’intérieur des « centrales » cellulaires et au sein de la machinerie de signalisation, l’ACAD9 aide à contenir les cellules qui « mangent » l’os et pourrait ouvrir une nouvelle voie pour prévenir l’ostéoporose.
Bâtisseurs d’os et « mangeurs » d’os
L’os sain est continuellement remodelé par deux équipes cellulaires opposées : les ostéoblastes qui forment l’os et les ostéoclastes qui le dissolvent. Dans l’ostéoporose, l’équilibre bascule en faveur des « mangeurs » d’os, laissant le squelette fin et fragile. Les ostéoclastes sont activés lorsqu’un signal appelé RANKL se lie à son récepteur sur les cellules précurseurs, déclenchant l’activation d’une protéine nommée TRAF6. Cela entraîne des cascades chimiques et une vague d’espèces réactives de l’oxygène — des molécules hautement réactives souvent appelées ROS — qui poussent ces précurseurs à fusionner en grandes cellules résorbantes. Les auteurs ont émis l’hypothèse que l’ACAD9, connue pour son rôle dans la production d’énergie mitochondriale, pourrait aussi influencer ce processus.
Un gardien mitochondrial du stress
À l’intérieur des mitochondries, l’ACAD9 aide à assembler une grande machinerie protéique appelée complexe I et favorise la formation de « supercomplexes », des regroupements ordonnés de plusieurs complexes de la chaîne respiratoire. Ces structures rendent la production d’énergie plus efficace et limitent la production indésirable de ROS. Dans des expériences cellulaires, les chercheurs ont constaté que, lorsque les précurseurs d’ostéoclastes étaient exposés au RANKL et commençaient à mûrir, les niveaux d’ACAD9 diminuaient, le complexe I et les supercomplexes déclinaient, et les ROS augmentaient fortement. L’inhibition de l’ACAD9 amplifiait encore les ROS et accélèrait la formation d’ostéoclastes, tandis que l’augmentation de l’ACAD9 restaurant le complexe I, augmentait l’énergie cellulaire (ATP), réduisait les ROS et atténuait la différenciation ostéoclastique. L’élimination des ROS par un antioxydant n’inversait que partiellement les effets de la perte d’ACAD9, suggérant que l’ACAD9 agit aussi par une voie non mitochondriale.
ACAD9, frein moléculaire des « mangeurs » d’os
L’équipe s’est ensuite intéressée à TRAF6, le relais clé que le RANKL utilise pour activer les gènes ostéoclastiques. Ils ont découvert qu’une fraction d’ACAD9 se trouvait dans le cytosol plutôt que dans les mitochondries, où elle peut se lier physiquement à TRAF6. Cette liaison modifie la manière dont TRAF6 interagit avec ses enzymes partenaires chargées d’ajouter de petites étiquettes « ubiquitine ». En l’absence d’ACAD9, TRAF6 devient fortement décoré d’un type de chaîne ubiquitine (liée via une position appelée K63), qui sert de plateforme pour activer des signaux en aval, notamment les voies MAPK et NF‑κB qui stimulent la croissance des ostéoclastes et la résorption osseuse. En présence d’ACAD9, ces chaînes K63 sont limitées, tandis qu’un autre type de chaîne ubiquitine (liée en K48) est favorisé, ciblant TRAF6 pour destruction par le système de dégradation protéique de la cellule. En somme, l’ACAD9 atténue la capacité de signalisation de TRAF6 et accélère son élimination.
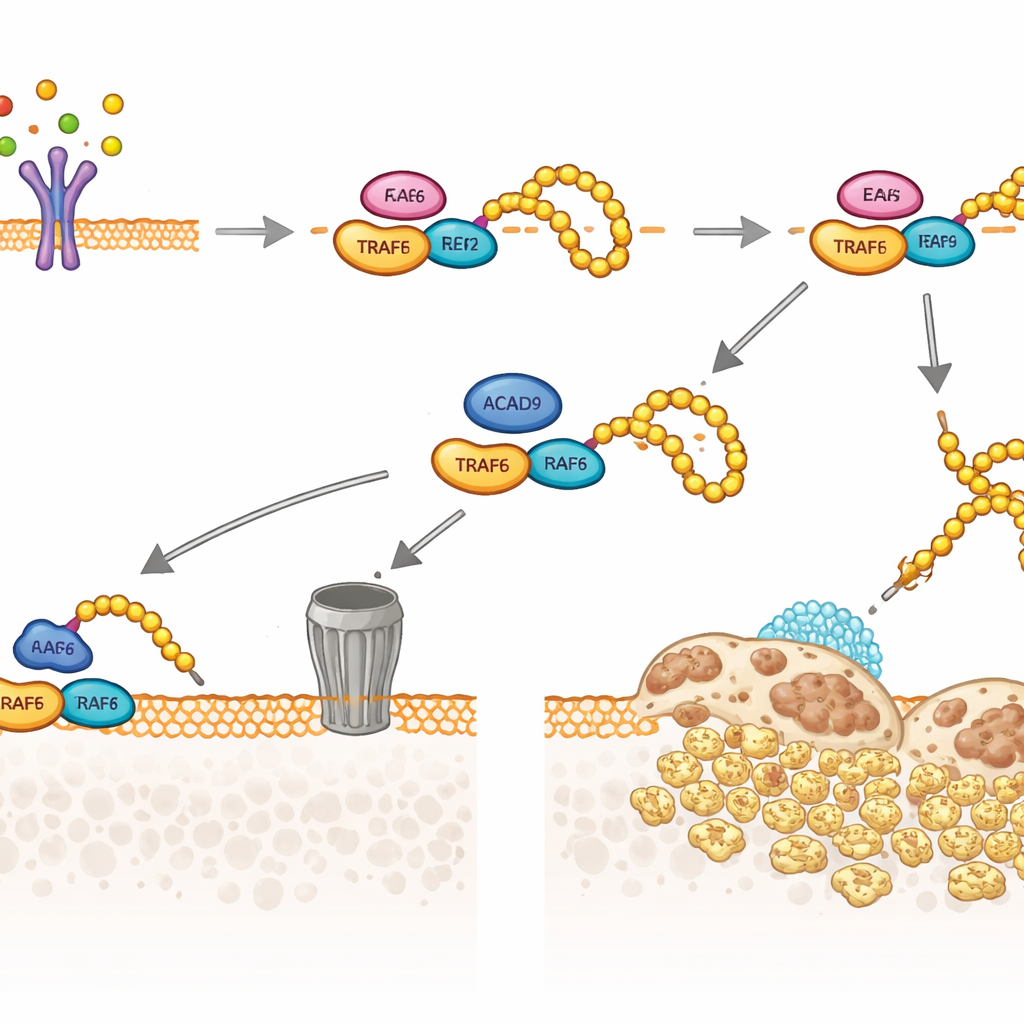
Des os de souris aux fractures humaines
Pour évaluer l’effet in vivo, les chercheurs ont généré des souris dépourvues d’ACAD9 spécifiquement dans les précurseurs d’ostéoclastes. À mesure que ces animaux vieillissaient, les scans montraient un affinement progressif de l’os trabéculaire, un espacement accru entre les trabécules et une architecture osseuse détériorée — autant de signes d’ostéoporose. Leurs os contenaient plus d’ostéoclastes et des niveaux plus élevés de marqueurs de résorption osseuse, tandis que le complexe I mitochondrial, les supercomplexes et l’ATP diminuaient. Les molécules de signalisation en aval de TRAF6 étaient hyper‑activées et les enzymes productrices de ROS augmentées. Fait important, l’activité de formation osseuse restait globalement normale, montrant que la perte osseuse excessive résultait principalement d’une activation excessive des ostéoclastes. En complément des expériences murines, l’analyse de larges cohortes humaines a associé des variants rares délétères du gène ACAD9 à un risque accru de fractures vertébrales, suggérant une pertinence clinique.
Ce que cela signifie pour les thérapies futures
Pris ensemble, les résultats présentent l’ACAD9 comme un double défenseur contre l’ostéoporose. À l’intérieur des mitochondries, il maintient une production d’énergie efficace et limite le stress oxydatif ; dans le cytosol, il bride TRAF6, l’interrupteur maître de l’activation ostéoclastique, en remodelant ses marquages ubiquitine et en favorisant sa dégradation. Lorsque l’ACAD9 est absent ou réduit, les cellules qui résorbent l’os se multiplient et les os s’affaiblissent. Des médicaments qui renforcent l’activité d’ACAD9 ou miment son interaction avec TRAF6 pourraient donc offrir une stratégie nouvelle en deux volets pour protéger les os vieillissants — en améliorant simultanément le métabolisme cellulaire et en calmant une résorption osseuse excessive.
Citation: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
Mots-clés: ostéoporose, ostéoclastes, mitochondries, ubiquitination, remodelage osseux