Clear Sky Science · ar
دور ACAD9 السيتوسولي الثانوي: قمع تكون الخلايا الماصة للعظم بوساطة TRAF6 والحماية من هشاشة العظام
لماذا تضعف العظام مع التقدم في السن
كسور الورك والهياكل الشوكية الهشة من بين أكثر مشاكل الشيخوخة رهبة، ومع ذلك نادراً ما تُناقش بيولوجيا الخلايا الخفية وراء هذه الكسور خارج المختبر. تكشف هذه الدراسة عن دور مفاجئ لبروتين ميتوكوندري يُدعى ACAD9 في الحفاظ على قوة عظامنا. من خلال العمل داخل محطات الطاقة الخلوية وفي آليات الإشارة الخلوية، يساعد ACAD9 على كبح الخلايا التي تآكل العظم وقد يفتح طريقاً جديداً لمنع هشاشة العظام.
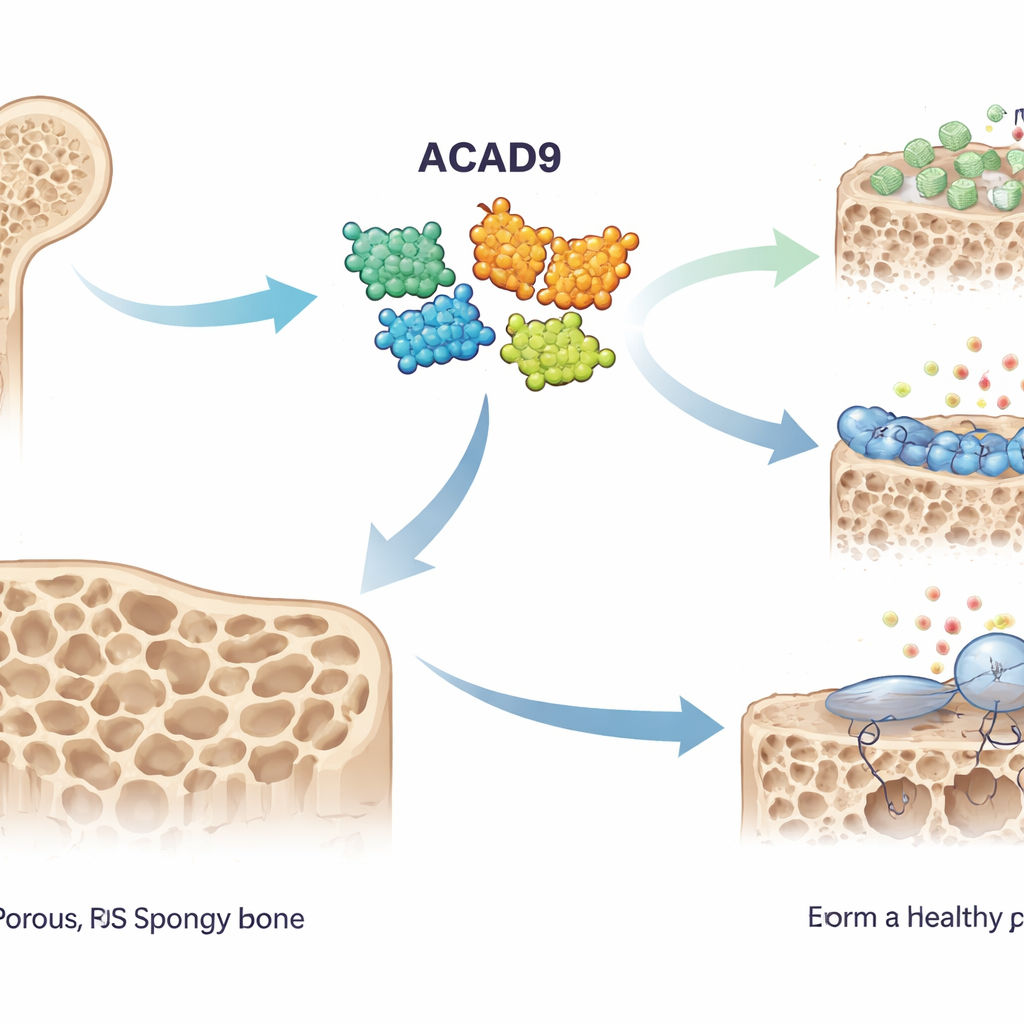
بناة العظم وآكله
العظم السليم يخضع باستمرار لإعادة تشكيل بواسطة فريقين متقابلين من الخلايا: البانيات العظمية التي تبني العظم، والمماسحات العظمية (الخلايا الماصة) التي تذيب العظم. في هشاشة العظام، يميل التوازن لصالح آكلي العظم، ما يترك الهيكل العظمي رقيقاً وهشاً. تُفعَّل الخلايا الماصة عندما يرتبط إشارة تُسمى RANKL بمستقبلها على الخلايا السلفية، فتُشغّل بروتيناً اسمه TRAF6. هذا بدوره يطلق تسلسلات كيميائية وتفجّراً في أنواع الأكسجين التفاعلية — جزيئات شديدة التفاعل غالباً ما تُختصر ROS — والتي تدفع هذه الخلايا السلفية للاندماج وتكوين خلايا كبيرة قادرة على امتصاص العظم. اشتبه الباحثون أن ACAD9، المعروف بدوره في إنتاج الطاقة الميتوكوندرية، قد يؤثر أيضاً في هذه العملية.
حارس ميتوكوندري للإجهاد
داخل الميتوكوندريا، يساعد ACAD9 على تجميع آلة بروتينية كبيرة تُسمى المجمع I ويعزز تكوين «التيارات الفائقة» (supercomplexes)، وهي مجموعات منظمة من عدة مركبات في سلسلة التنفس. تجعل هذه التراكيب إنتاج الطاقة أكثر كفاءة وتحدّ من ROS غير المرغوب فيه. في تجارب خلوية، وجد الباحثون أنه عندما تعرضت الخلايا السلفية للمماصين للعظم لـ RANKL وبدأت في النضج، انخفضت مستويات ACAD9، وتراجع المجمع I والتيارات الفائقة، وارتفعت ROS بشكل حاد. زيادة إخماد ACAD9 ضاعفت ROS وسرّعت تكون الخلايا الماصة، بينما أدّت زيادة ACAD9 إلى استعادة المجمع I، ورفع طاقة الخلية (ATP)، وخفض ROS، وكبح تمايز الخلايا الماصة. تنظيف ROS بعقار مضاد للأكسدة لم يعكس بالكامل آثار فقدان ACAD9، مما يشير إلى أن ACAD9 يعمل أيضاً عبر مسار آخر خارج الميتوكوندريا.
ACAD9 كفرامل جزيئية لآكلي العظم
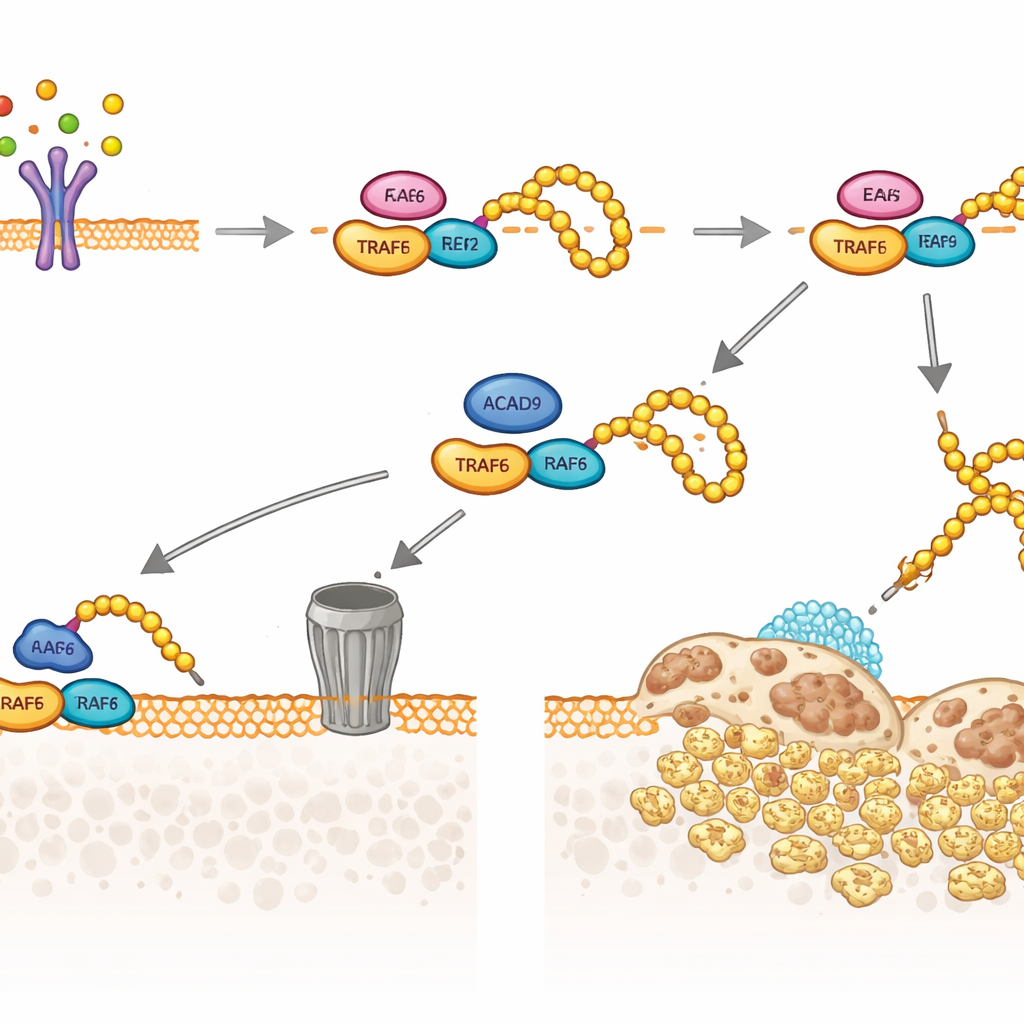
نظر الفريق بعد ذلك إلى TRAF6، المرحّل الرئيسي الذي يستخدمه RANKL لتشغيل جينات الخلايا الماصة. اكتشفوا أن جزءاً من بروتين ACAD9 يتواجد في سيتوسول الخلية بدلاً من الميتوكوندريا، حيث يمكنه الارتباط ماديّاً بـ TRAF6. يغير هذا الارتباط كيفية تفاعل TRAF6 مع إنزيماته الشريكة التي تُلصق وسمات صغيرة تسمى «اليوبكويتين». بدون ACAD9، يصبح TRAF6 مزخرفاً بشكل كبير بسلسلة من نوع واحد من اليوبكويتين (مرتبطة عند موضع يُسمى K63)، والتي تعمل كهيكل لتفعيل الإشارات اللاحقة، بما في ذلك مسارات MAPK وNF‑κB التي تدفع نمو الخلايا الماصة وامتصاص العظم. بوجود ACAD9، تُقَلّ هذه سلاسل K63، بينما يُفضّل نوع مختلف من سلاسل اليوبكويتين (مرتبطة بـK48)، ما يوجّه TRAF6 نحو التحلل في آلية تكسير البروتين داخل الخلية. باختصار، يخفف ACAD9 من قدرة TRAF6 على الإشارة ويسرّع في نفس الوقت إزالته.
من عظام الفئران إلى كسور البشر
لرؤية كيف يتجلى هذا داخل كائن حي، هندس الباحثون فئراناً تفتقر إلى ACAD9 بشكل مخصص في الخلايا السلفية المماصة للعظم. مع تقدم عمر هذه الحيوانات، أظهرت الفحوصات ترققاً تدريجياً في العظم الشبكي، وتزايد المسافات بين أعمدة العظم، وتدهور هندسة العظم — وكلها علامات مميزة لهشاشة العظام. احتوت عظامهم على عدد أكبر من الخلايا الماصة ومستويات أعلى من علامات امتصاص العظم، بينما كان المجمع I والتيارات الفائقة وATP منخفضة. كانت جزيئات الإشارة أسفل TRAF6 مفعّلة مفرطة، وزادت إنزيمات مولدة لـ ROS. والأهم أن نشاط بناء العظم ظلّ سليماً إلى حد كبير، مما يدل على أن الفقدان المفرط للعظم ناتج أساساً عن فرط نشاط الخلايا الماصة. مكملاً لعمل الفئران، ربط تحليل بيانات صناديق حيوية بشرية كبيرة طفرات نادرة ومدمرة في جين ACAD9 بزيادة خطر كسور الفقرات، ما يشير إلى صلة سريرية.
ماذا يعني هذا للعلاجات المستقبلية
تقدم النتائج معاً ACAD9 كمدافع مزدوج ضد هشاشة العظام. داخل الميتوكوندريا، يُحافظ على إنتاج طاقة فعال ويقلل الإجهاد التأكسدي؛ وفي السيتوسول، يقمع TRAF6، المفتاح الرئيسي لتنشيط الخلايا الماصة، عبر إعادة تشكيل علامات اليوبكويتين وتعزيز تحلله. عندما ينقص ACAD9 أو يقل، تتكاثر الخلايا الماصة وتضعف العظام. لذلك قد توفر الأدوية التي تعزز نشاط ACAD9 أو تحاكي تَفاعله مع TRAF6 استراتيجية جديدة ذات شقّين لحماية عظام المسنين — بتحسين الأيض الخلوي وتهدئة امتصاص العظم المفرط في الوقت نفسه.
الاستشهاد: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
الكلمات المفتاحية: هشاشة العظام, الخلايا الماصة للعظم, الميتوكوندريا, اليوبيكويتينيشن, إعادة تشكيل العظم