Clear Sky Science · es
Función citosólica alternativa de ACAD9: supresión de la osteoclastogénesis mediada por TRAF6 y protección frente a la osteoporosis
Por qué los huesos se debilitan con la edad
Las fracturas de cadera y las vértebras frágiles están entre los problemas de envejecimiento más temidos, pero la biología celular que hay detrás de estas fracturas rara vez se discute fuera del laboratorio. Este estudio revela un papel sorprendente de una proteína mitocondrial llamada ACAD9 en el mantenimiento de la resistencia ósea. Al actuar tanto dentro de las centrales energéticas de la célula como en la maquinaria de señalización celular, ACAD9 ayuda a contener a las células que devoran hueso y podría abrir una vía nueva para prevenir la osteoporosis.
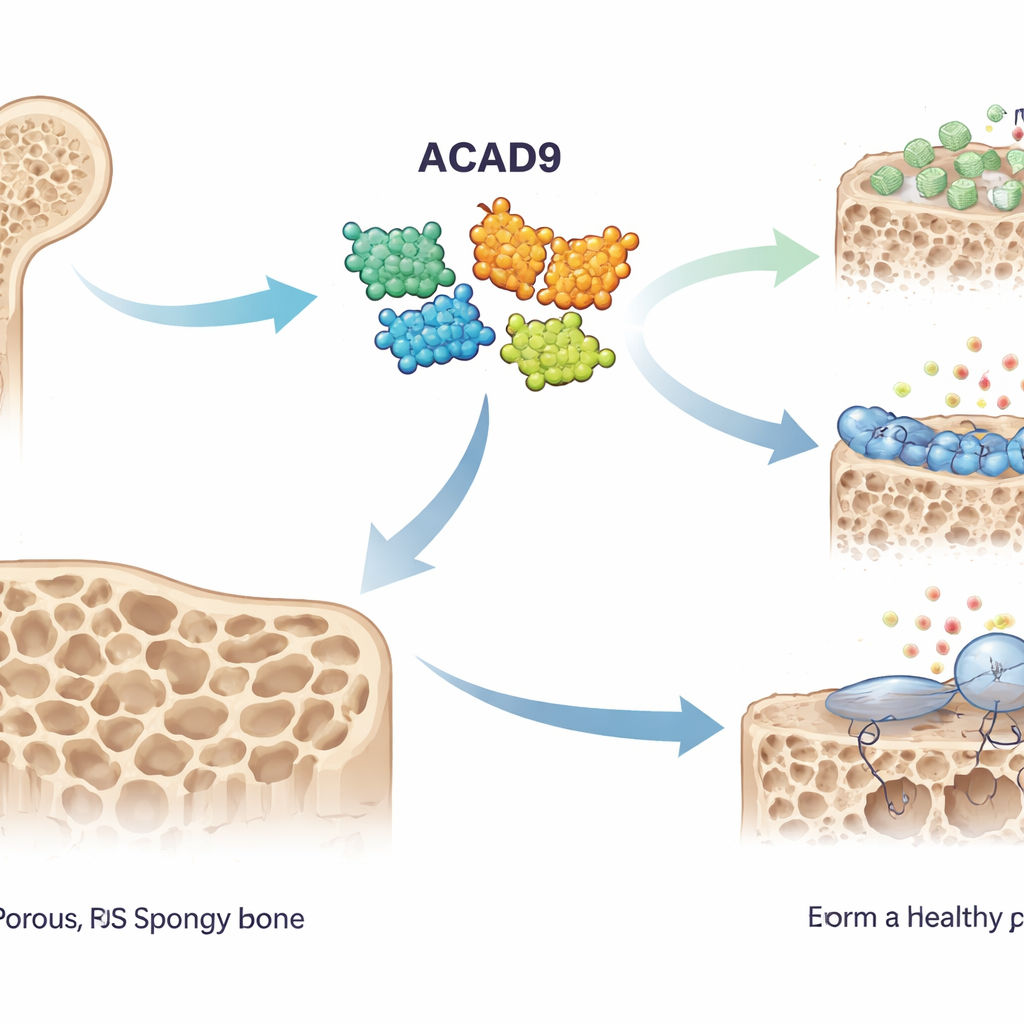
Constructores y devoradores del hueso
El hueso sano se remodela constantemente por dos equipos celulares opuestos: los osteoblastos, que forman hueso, y los osteoclastos, que lo disuelven. En la osteoporosis, el equilibrio se inclina hacia los devoradores de hueso, dejando el esqueleto delgado y frágil. Los osteoclastos se activan cuando una señal llamada RANKL se une a su receptor en las células precursoras, activando una proteína denominada TRAF6. Esto a su vez desencadena cascadas químicas y una ráfaga de especies reactivas de oxígeno —moléculas altamente reactivas a menudo llamadas ROS— que empujan a estos precursores a fusionarse en grandes células que reabsorben hueso. Los autores sospechaban que ACAD9, conocido por su papel en la producción de energía mitocondrial, podría influir también en este proceso.
Un guardián mitocondrial frente al estrés
Dentro de las mitocondrias, ACAD9 ayuda a ensamblar una gran máquina proteica llamada complejo I y favorece la formación de “supercomplejos”, agrupaciones ordenadas de varios complejos de la cadena respiratoria. Estas estructuras hacen la producción de energía más eficiente y limitan las ROS indeseadas. En experimentos celulares, los investigadores observaron que cuando los precursores de osteoclastos se exponían a RANKL y comenzaban a madurar, los niveles de ACAD9 disminuían, el complejo I y los supercomplejos se redujeron y las ROS aumentaron bruscamente. La supresión de ACAD9 amplificó aún más las ROS y aceleró la formación de osteoclastos, mientras que aumentar ACAD9 restauró el complejo I, incrementó la energía celular (ATP), redujo las ROS y frenó la diferenciación osteoclástica. El aclarado de ROS con un fármaco antioxidante sólo revirtió parcialmente los efectos de la pérdida de ACAD9, lo que sugiere que ACAD9 debe actuar también por otra vía no mitocondrial.
ACAD9 como freno molecular de los devoradores del hueso
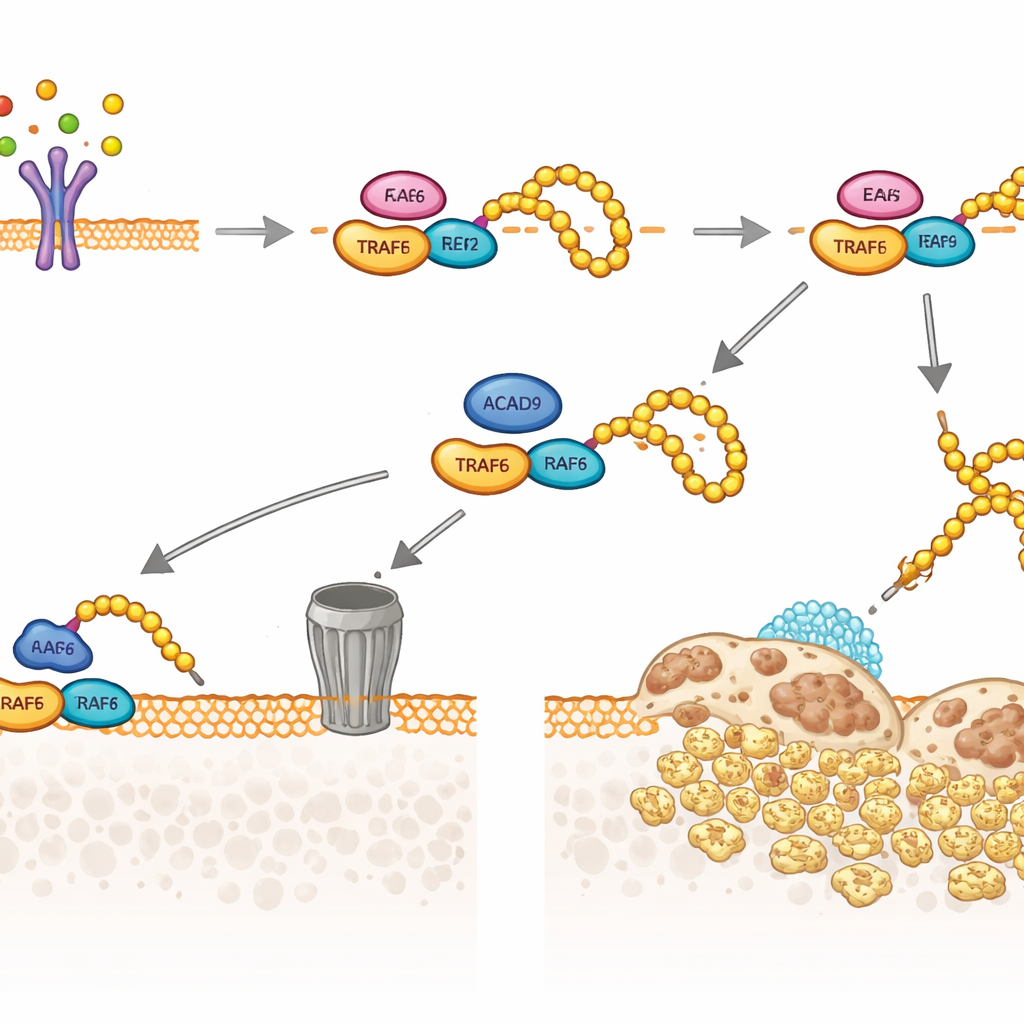
El equipo examinó a continuación a TRAF6, el relevo clave que RANKL utiliza para activar los genes osteoclásticos. Descubrieron que parte de la proteína ACAD9 reside en el citoplasma en lugar de en las mitocondrias, donde puede unirse físicamente a TRAF6. Esta interacción cambia cómo TRAF6 se relaciona con sus enzimas asociadas que añaden pequeñas etiquetas de “ubiquitina”. Sin ACAD9, TRAF6 se ve fuertemente decorado con un tipo de cadena de ubiquitina (enlazada a través de una posición llamada K63), que actúa como andamiaje para activar señales aguas abajo, incluidas las vías MAPK y NF-κB que impulsan el crecimiento de los osteoclastos y la resorción ósea. Con ACAD9 presente, estas cadenas K63 se limitan, mientras que se favorece otro tipo de cadena de ubiquitina (enlazada por K48), que marca a TRAF6 para su destrucción en la maquinaria celular de degradación de proteínas. En esencia, ACAD9 tanto atenúa la capacidad señalizadora de TRAF6 como acelera su eliminación.
De los huesos de ratón a las fracturas humanas
Para ver cómo se manifiesta esto en un organismo vivo, los investigadores diseñaron ratones que carecen de ACAD9 específicamente en los precursores de osteoclastos. A medida que estos animales envejecían, las exploraciones revelaron un adelgazamiento progresivo del hueso trabecular, mayor separación entre las trabéculas y una arquitectura ósea peor —todos rasgos distintivos de la osteoporosis. Sus huesos contenían más osteoclastos y niveles más altos de marcadores de resorción ósea, mientras que el complejo I mitocondrial, los supercomplejos y el ATP estaban reducidos. Las moléculas de señalización aguas abajo de TRAF6 estaban hiperactivadas y las enzimas productoras de ROS aumentaron. Es importante que la actividad formadora de hueso permaneció en gran medida normal, lo que muestra que la pérdida ósea en exceso surgió principalmente por osteoclastos hiperactivos. Complementando el trabajo en ratones, el análisis de grandes bases de datos humanas vinculó variantes raras y dañinas en el gen ACAD9 con un mayor riesgo de fracturas vertebrales, lo que sugiere relevancia clínica.
Qué significa esto para futuras terapias
En conjunto, los hallazgos presentan a ACAD9 como un defensor dual contra la osteoporosis. Dentro de las mitocondrias, mantiene una producción de energía eficiente y controla el estrés oxidativo; en el citosol, reprime a TRAF6, el interruptor maestro de la activación osteoclástica, al remodelar sus etiquetas de ubiquitina y promover su degradación. Cuando ACAD9 falta o se reduce, las células que devoran hueso se multiplican y los huesos se debilitan. Los fármacos que aumenten la actividad de ACAD9 o imiten su interacción con TRAF6 podrían, por tanto, ofrecer una estrategia nueva y de doble acción para proteger los huesos envejecidos —mejorando simultáneamente el metabolismo celular y atenuando la resorción ósea excesiva.
Cita: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
Palabras clave: osteoporosis, osteoclastos, mitocondrias, ubiquitinación, remodelado óseo