Clear Sky Science · he
תפקוד ציטוסולי נוסף של ACAD9: עיכוב אוסטאוקלסטוגנזה בתיווך TRAF6 והגנה מפני אוסטאופורוזיס
מדוע העצמות נחלשות עם הגיל
שברים במותן ועמוד שדרה שביר הם מהחששות הבולטים בגיל המבוגר, אך הביולוגיה התאית שמאחורי שברים אלה נדירה בדיון מחוץ למעבדה. המחקר חושף תפקיד מפתיע לחלבון מיטוכונדריאלי בשם ACAD9 בשמירה על חוזק העצמות. על ידי פעולה הן בתחנות הכוח של התא והן במערכות הסיגנול התאית, ACAD9 מסייע לשלוט בתאים ש"אוכלים" עצם ועשוי לפתוח נתיב חדש למניעת אוסטאופורוזיס.
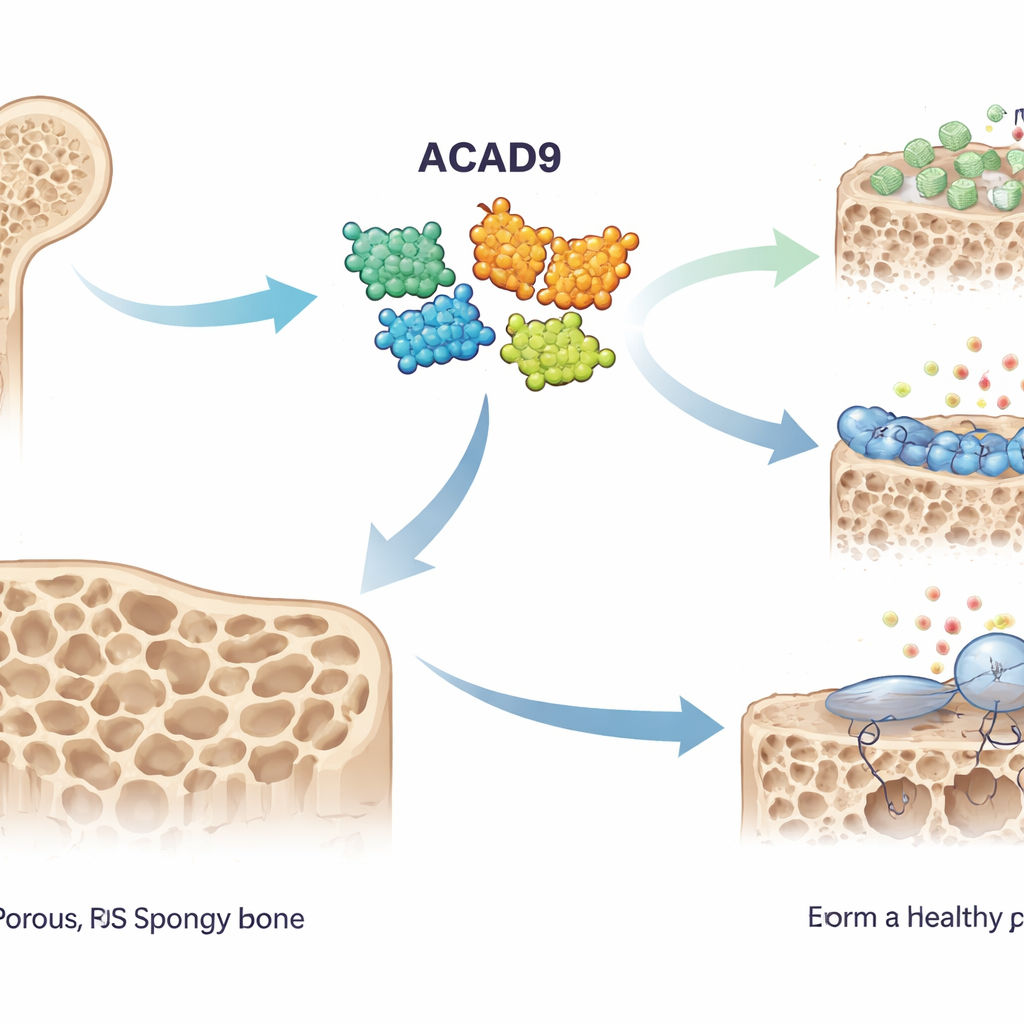
בוני עצם ואוכלי עצם
עצם בריאה מתחדשת כל הזמן על ידי שתי קבוצות תחרותיות של תאים: אוסטאובלאסטים שבונים עצם ואוסטאוקלסטים שממיסים אותה. באוסטאופורוזיס האיזון נוטה לטובת אוכלי העצם, מה שמותיר שלד דק ושביר. אוסטאוקלסטים מופעלים כאשר אות שנקרא RANKL נקשר לקולטן שלו בתאי העתודה, ומפעיל חלבון בשם TRAF6. זה מעורר מפל של שפע של מרכיבים כימיים והתפרצות של סוגי חמצון תגובתי — מולקולות פעילות מאוד שמוכרות כ‑ROS — שמניעות את תאי העתודה להיתוך לתאים גדולים שפוררים עצם. החוקרים חשדו כי ACAD9, המוכר מתפקידו בייצור אנרגיה מיטוכונדריאלי, עשוי להשפיע גם על תהליך זה.
שומר מיטוכונדריאלי של מתח
בתוך המיטוכונדריה, ACAD9 מסייע בהרכבת מכונת חלבונים גדולה הנקראת קומפלקס I ומקדם יצירת "סופרקומפלקסים", קבוצות מסודרות של כמה קומפלקסים בשרשרת הנשימה. מבנים אלה משפרים את יעילות ייצור האנרגיה ומגבילים ROS לא רצויים. בניסויים תאיתיים מצאו החוקרים כי כאשר תאי עתודת אוסטאוקלסט נחשפו ל‑RANKL והחלו להתבגר, רמות ACAD9 ירדו, קומפלקס I והסופרקומפלקסים פחתו ו‑ROS עלו בחדות. הדחקת ACAD9 הגבירה עוד יותר את ה‑ROS והאיצה את היווצרות האוסטאוקלסטים, בעוד שחיזוק ACAD9 שחזר את קומפלקס I, העלה את אנרגיית התא (ATP), הוריד את ה‑ROS ובלם את ההבחנה לאוסטאוקלסטים. סילוק ה‑ROS באמצעות תרופה אנטי‑אוקסידנטית השיב רק חלקית את ההשפעות של אובדן ACAD9, מה שמרמז ש־ACAD9 פועל גם דרך מסלול נוסף שאינו מיטוכונדריאלי.
ACAD9 כבלם מולקולרי על אוכלי העצם
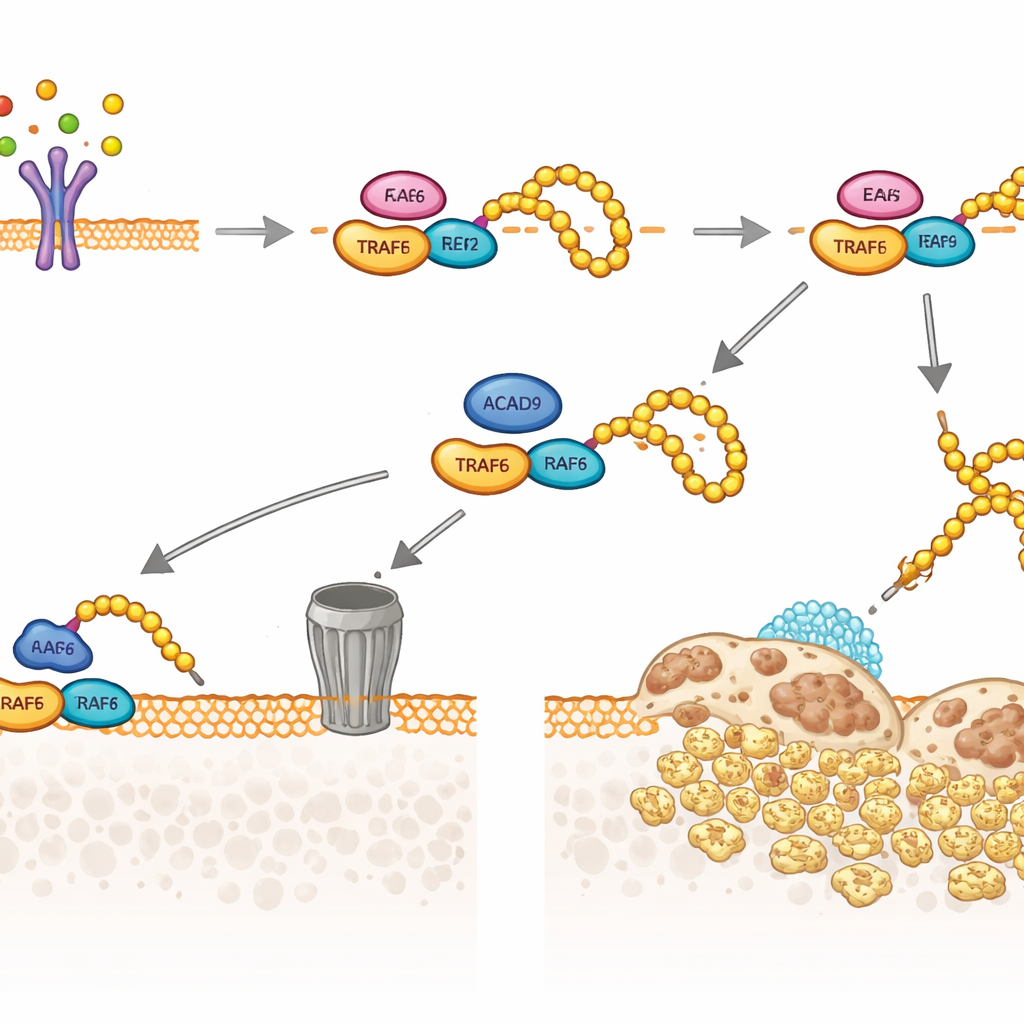
הצוות חקר בהמשך את TRAF6, הממסר המרכזי שבו משתמש RANKL כדי להפעיל גנים של אוסטאוקלסטים. הם גילו שחלק מחלבון ACAD9 נמצא בנוזל התאי (ציטוזול) ולא רק במיטוכונדריה, שם הוא יכול להיקשר פיזית ל‑TRAF6. קשר זה משנה את האופן שבו TRAF6 מתקשר עם האנזימים השותפים שמחברים תגיות יוביקוויטין קטנות. בהיעדר ACAD9, TRAF6 מקבל עיטור כבד מסוג שרשרת יוביקוויטין אחת (קישור דרך המיקום שנקרא K63), המשמשת כשלד להפעלת איתותים מטה, כולל מסלולי MAPK ו‑NF‑κB שמניעים צמיחה של אוסטאוקלסטים ופעילות פירור עצם. בנוכחות ACAD9, שרשרות K63 מצומצמות, בעוד שסוג אחר של שרשרת יוביקוויטין (קישור מסוג K48) מועדף, וכך מכוון את TRAF6 להרס במכונת מחזור החלבונים של התא. בעצם, ACAD9 גם מחליש את יכולת האיתות של TRAF6 וגם מהרה את הסרתו.
מעצמות עכבר לשברי אדם
כדי לבחון כיצד הדבר מתבטא באורגניזם חי, החוקרים הנדסו עכברים חסרי ACAD9 באופן ספציפי בתאי עתודת האוסטאוקלסט. עם התבגרות בעלי החיים נצפו סריקות שהראו דילול מתמשך של העצם הטרבקולרית, רווח גדול יותר בין רצועות העצם וארכיטקטורת עצם גרועה — כל אלה סימנים אופייניים לאוסטאופורוזיס. בעצמותיהם היו יותר אוסטאוקלסטים ורמות גבוהות יותר של סמני פירור עצם, בעוד שקומפלקס I המיטוכונדריאלי, סופרקומפלקסים ו‑ATP פחתו. מולקולות איתות מטה מ‑TRAF6 היו בהיפראקטיבציה, ואנזימים מייצרי ROS היו מוגברים. חשוב להדגיש כי פעילות בניית העצם נותרה ברובה נורמלית, מה שמראה שאובדן עצם מופרז נבע בעיקר מאוסטאוקלסטים פעילים מדי. כמשלים לעבודה בעכבר, ניתוח של מאגרי נתונים אנושיים גדולים קישר וריאנטים נדירים ומזיקים בגן ACAD9 לסיכון גבוה יותר לשברי חוליות, מה שמרמז על רלוונטיות קלינית.
מה משמעות הדבר עבור טיפולים עתידיים
במאמצע כל הממצאים מציגים את ACAD9 כמגן כפול מפני אוסטאופורוזיס. בתוך המיטוכונדריה הוא שומר על ייצור אנרגיה יעיל ושומר על מתח חמצוני תחת שליטה; בציטוזול הוא מדכא את TRAF6, המתג הראשי להפעלת אוסטאוקלסטים, על‑ידי עיצוב מחדש של תגיות היוביקוויטין שלו וקידום פירוקו. כאשר ACAD9 חסר או מופחת, תאי אוכלי העצם מתרבים והעצמות נחלשות. תרופות שמגבירות את פעולת ACAD9 או מחקות את הקשר שלו עם TRAF6 עלולות לכן להציע אסטרטגיה חדשה רב‑ממדית להגנת עצמות המתבגרים — הן על ידי שיפור המטבוליזם התאי והן על ידי הרחקת פעילות פירור העצם המוגזמת.
ציטוט: Wang, M., Yuan, C., Zhang, Y. et al. Moonlighting cytosolic function of ACAD9: suppression of TRAF6-mediated osteoclastogenesis and protection against osteoporosis. Cell Death Dis 17, 362 (2026). https://doi.org/10.1038/s41419-026-08626-z
מילות מפתח: אוסטאופורוזיס, אוסטאוקלסטים, מיטוכונדריה, יוביקוויטינציה, שחזור עצם