Clear Sky Science · tr
Azalmış YTHDF2, kolorektal kanserde m6A içeren SPOP mRNA’sını stabilize ederek PD-L1 ifadesini baskılar
Bu araştırma neden önemli
Kolorektal kanser, dünya genelinde en yaygın ve ölümcül kanserlerden biridir. Birçok modern tedavi, PD-1/PD-L1 adlı fren mekanizmasını engelleyerek vücudun kendi bağışıklık sisteminin tümörlere saldırmasını sağlamayı amaçlar. Yine de çoğu kolorektal kanser hastası bu ilaçlardan yarar görmemektedir. Bu çalışma, kanser hücreleri içinde bu bağışıklık “frenini” kapalı tutmalarına yardımcı olan gizli bir moleküler zincirleme reaksiyonu ortaya koymaktadır. Bu zincirin anlaşılması, immünoterapinin çok daha fazla hasta için işe yaramasını sağlayacak yeni bir yol sunar.
Tümör RNA’sında gizli bir işaret
Hücrelerimiz sürekli olarak RNA iplikçiklerini okur ve parçalar; bu kısa ömürlü mesajlar hangi proteinlerin üretilmesini söyleyen talimatlardır. Son yıllarda, birçok RNA mesajının m6A adlı bir işaret dahil olmak üzere küçük kimyasal etiketler taşıdığı keşfedildi; bu etiketler bir yazıdaki düzenleme işaretleri gibi davranarak bir mesajın ne kadar süre kaldığını ve ne kadar etkin okunduğunu belirler. YTHDF2 adlı bir protein, bu m6A etiketlerini tanımada uzmanlaşmıştır ve genellikle etiketli RNA’yı yıkıma yönlendirerek bir hücrenin hangi proteinleri ürettiğini ince ayarlar. Hastalardan alınan kolorektal kanser örneklerinde ve geniş kamu veritabanlarında yazarlar, YTHDF2 seviyelerinin tümör dokusunda normal kolon dokusuna göre belirgin biçimde daha yüksek olduğunu ve yüksek YTHDF2’ye sahip hastaların genellikle daha kötü sağkalıma sahip olduğunu buldular; bu da bu RNA “okuyucusunun” kanser yanlısı bir rolü olabileceğini gösterir.
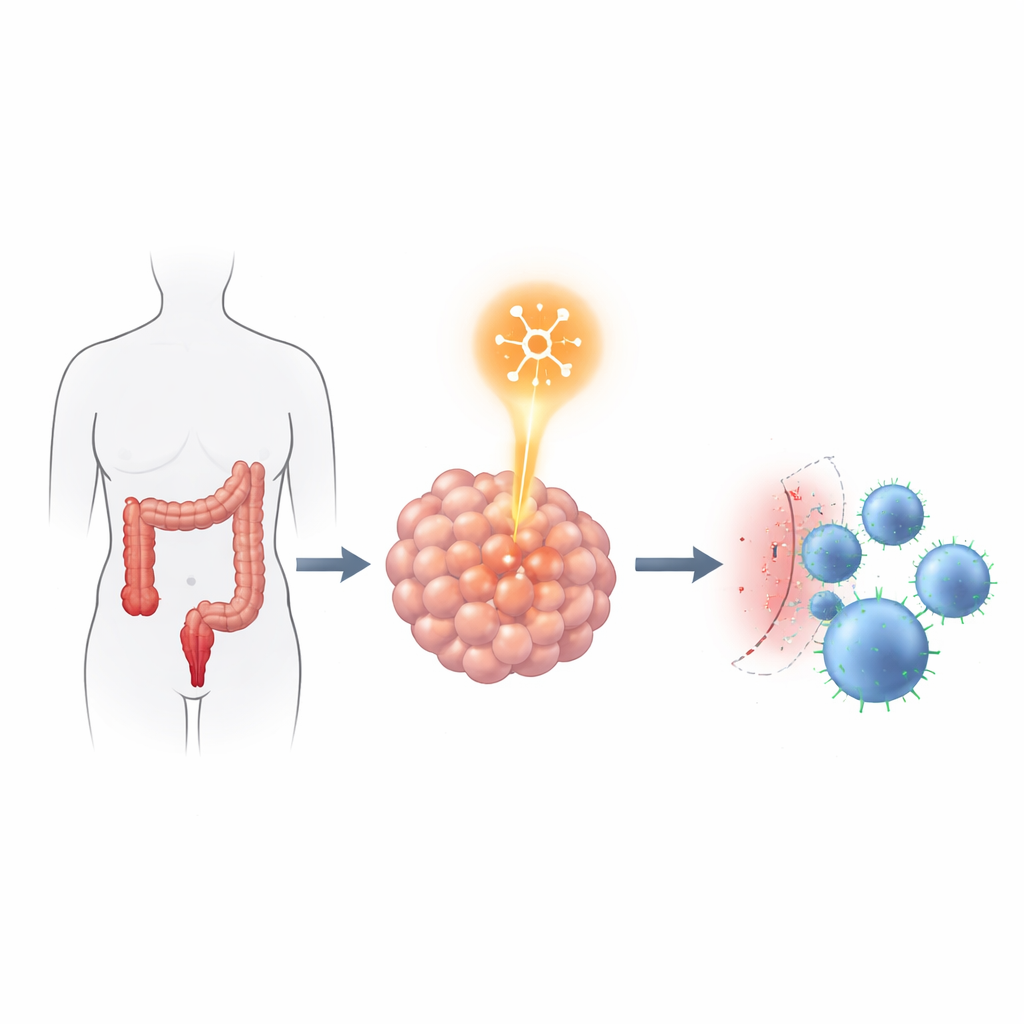
RNA okuyucuyu bağışıklık frenine bağlamak
Araştırma ekibi, YTHDF2’nin tümörlerin bağışıklık hücrelerinin saldırılarına nasıl direnmesine yardımcı olabileceğini sorguladı. İnsana ait kolorektal kanser hücrelerini, YTHDF2 olan veya olmayan biçimleriyle, insan bağışıklık hücreleri de alacak şekilde özel farelere nakletti. Normal YTHDF2’ye sahip tümörler daha hızlı büyüdü ve içinde daha az kanser öldürücü T hücresi görüldü. YTHDF2 azaltıldığında tümörler küçüldü ve kanser içine daha fazla CD4 ve CD8 T hücresi girdi. Çarpıcı biçimde, YTHDF2’nin düşürülmesi laboratuvar ortamında kanser hücrelerinin büyüme, hareket veya invazyon hızını değiştirmedi; bu da etkisinin daha çok tümörün bağışıklık sistemiyle etkileşiminde olduğunu, ham tümör agresifliğinde olmadığını düşündürür.
Kanser hücreleri PD-L1’i nasıl yüksek tutar
PD-L1, tümör hücresi yüzeyinde bulunan, T hücrelerindeki PD-1 ile etkileşip onların inhibe olmasını sağlayan bir proteindir. Araştırmacılar, YTHDF2 baskılanınca kanser hücrelerinde ve onların salgıladığı veziküllerde (ekzosomlar) PD-L1 protein miktarının keskin biçimde düştüğünü, oysa PD-L1 RNA seviyelerinin yaklaşık olarak aynı kaldığını gözlemlediler. Bu, YTHDF2’nin PD-L1’i RNA aşamasından sonra dolaylı olarak etkilediğine işaret etti. Ayrıntılı testler, YTHDF2 kaybının PD-L1 proteinini daha az stabil hale getirdiğini ve hücrenin protein parçalama mekanizması tarafından daha kolay yok edildiğini, ayrıca PD-1 ile PD-L1 arasındaki bağlanmayı zayıflattığını gösterdi. Sonuç olarak, eşkültürde yapılan deneylerde YTHDF2 düzeyi düşük olduğunda T hücreleri daha fazla kanser hücresi öldürdü; bu da bağışıklık saldırısında işlevsel bir artış olduğunu gösterdi.
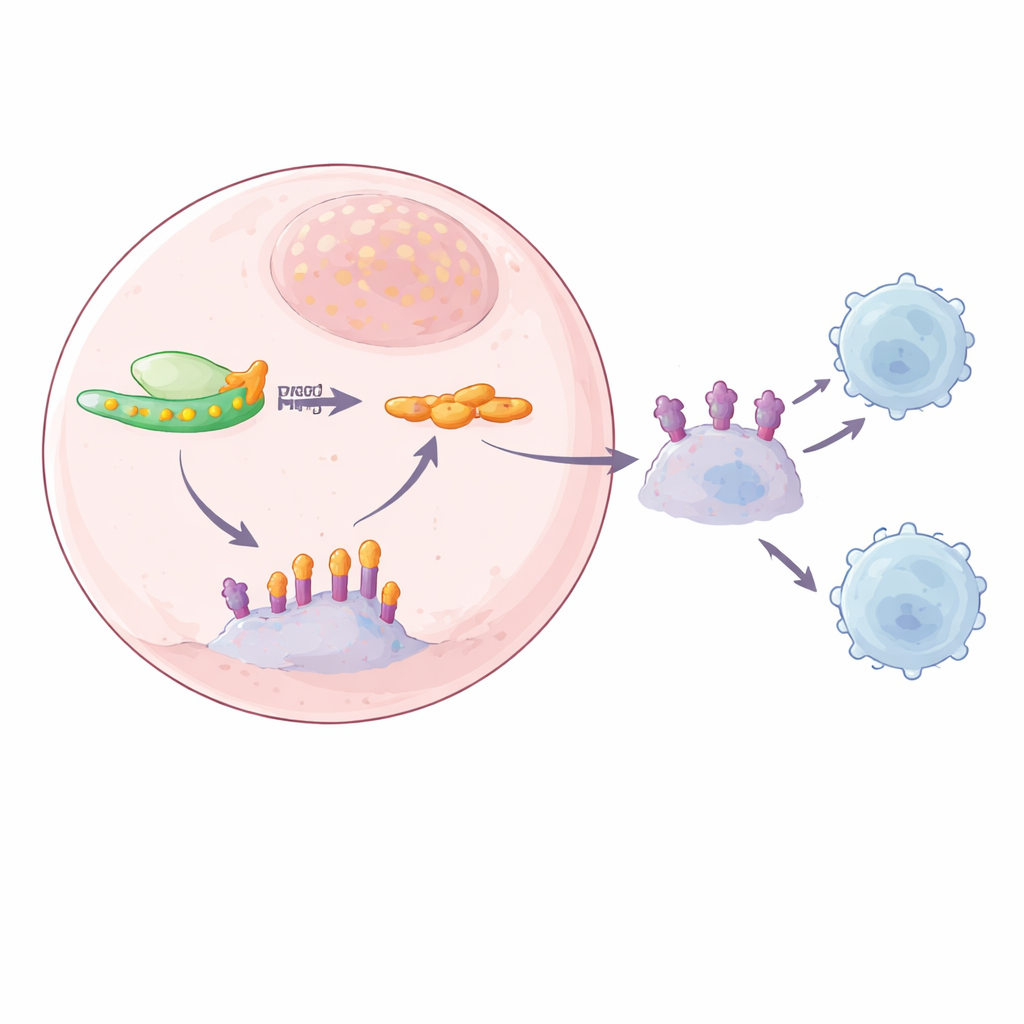
SPOP bağlantısı: bozulmuş bir temizlik ekibi
YTHDF2 ile PD-L1 arasındaki eksik halkayı izlemek için ekip, hem m6A ile işaretlenmiş hem de YTHDF2 tarafından bağlanan RNA mesajlarını aramak üzere birden çok sıralama yaklaşımını birleştirdi. Güçlü adaylardan biri, normalde PD-L1’i yok edilmek üzere etiketleyen bir protein kompleksinin parçası olan SPOP’tu; bu kompleks PD-L1’in birikmesini önleyen bir temizlik ekibi gibi görev yapar. Yazarlar SPOP RNA’sının kuyruk bölgesinde m6A işaretleri buldular ve YTHDF2’nin tam olarak oraya bağlandığını gösterdiler. YTHDF2 yüksek olduğunda SPOP RNA’sı daha hızlı parçalanıyor, bunun sonucunda SPOP proteini azalıyor ve PD-L1 temizliği zayıflıyordu. YTHDF2 azaldığında SPOP RNA daha stabil hale geliyor, SPOP proteini artıyor ve hem hücre yüzeyinde hem de ekzosomlarda PD-L1 protein seviyeleri düşüyordu. SPOP RNA’sındaki m6A bölgelerinin mutasyona uğratılması veya SPOP’un kendisinin ortadan kaldırılması bu zinciri bozdu; bu da m6A’ya bağımlı YTHDF2–SPOP yolunun PD-L1 bolluğunu kontrol ettiğini doğruladı.
Gelecekteki tedaviler için ne anlama geliyor
Basitçe ifade etmek gerekirse, bu çalışma kolorektal kanser hücreleri içinde üç adımlı bir röleyi ortaya koyuyor: RNA etiketi m6A, YTHDF2’nin SPOP seviyelerini azaltmasına izin veriyor; zayıflamış SPOP PD-L1’i düzgün biçimde temizleyemiyor; bunun sonucu artan PD-L1 tümörü T hücrelerinden koruyor. Bu röleyi kesintiye uğratarak—ya YTHDF2’yi engelleyerek ya da SPOP’u güçlendirerek—tümörlerde PD-L1’i düşürmek ve mevcut PD-1/PD-L1 ilaçlarını özellikle şu anda az fayda gören hastalar için daha etkili kılmak mümkün olabilir. Böylelikle YTHDF2–SPOP–PD-L1 ekseni, bağışıklık sisteminin kolorektal kanseri daha iyi tanımasına ve yok etmesine yardımcı olacak umut verici yeni bir hedef olarak öne çıkıyor.
Atıf: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Anahtar kelimeler: kolorektal kanser, immünoterapi, PD-L1, RNA modifikasyonu, tümör bağışıklık kaçışı