Clear Sky Science · pl
Obniżony poziom YTHDF2 hamuje ekspresję PD-L1 przez stabilizację m6A-zawierającego mRNA SPOP w raku jelita grubego
Dlaczego to badanie ma znaczenie
Rak jelita grubego jest jednym z najczęstszych i najbardziej śmiertelnych nowotworów na świecie. Wiele współczesnych terapii stara się uwolnić własny układ odpornościowy pacjenta do ataku na guzy, blokując hamulec znany jako PD-1/PD-L1. Mimo to większość chorych na raka jelita grubego nadal nie odnosi korzyści z tych leków. W tej pracy odkryto ukrytą molekularną reakcję łańcuchową w komórkach nowotworowych, która pomaga im utrzymywać ten immunologiczny „hamulec” w pozycji włączonej. Poznanie tego łańcucha otwiera nową drogę do zwiększenia skuteczności immunoterapii u znacznie większej liczby osób.
Ukryta etykieta w RNA guza
Nasze komórki nieustannie odczytują i niszczą nici RNA — krótkotrwałe komunikaty, które mówią, jakie białka należy wytworzyć. W ostatnich latach naukowcy odkryli, że wiele wiadomości RNA niesie drobne chemiczne znaczniki, w tym m6A, które działają jak znaki edycyjne w manuskrypcie: decydują, jak długo komunikat przetrwa i jak intensywnie będzie odczytywany. Białko o nazwie YTHDF2 wyspecjalizowane jest w rozpoznawaniu tych znaczników m6A i zwykle pomaga w rozkładzie oznakowanego RNA, dopracowując profil produkowanych białek. W próbkach raka jelita grubego od pacjentów oraz w dużych publicznych bazach danych autorzy stwierdzili wyraźnie wyższe poziomy YTHDF2 w guzach niż w prawidłowej tkance jelita i zauważyli, że pacjenci z wyższym YTHDF2 mieli gorsze przeżycie, co sugeruje pronowotworową rolę tego „czytnika” RNA.
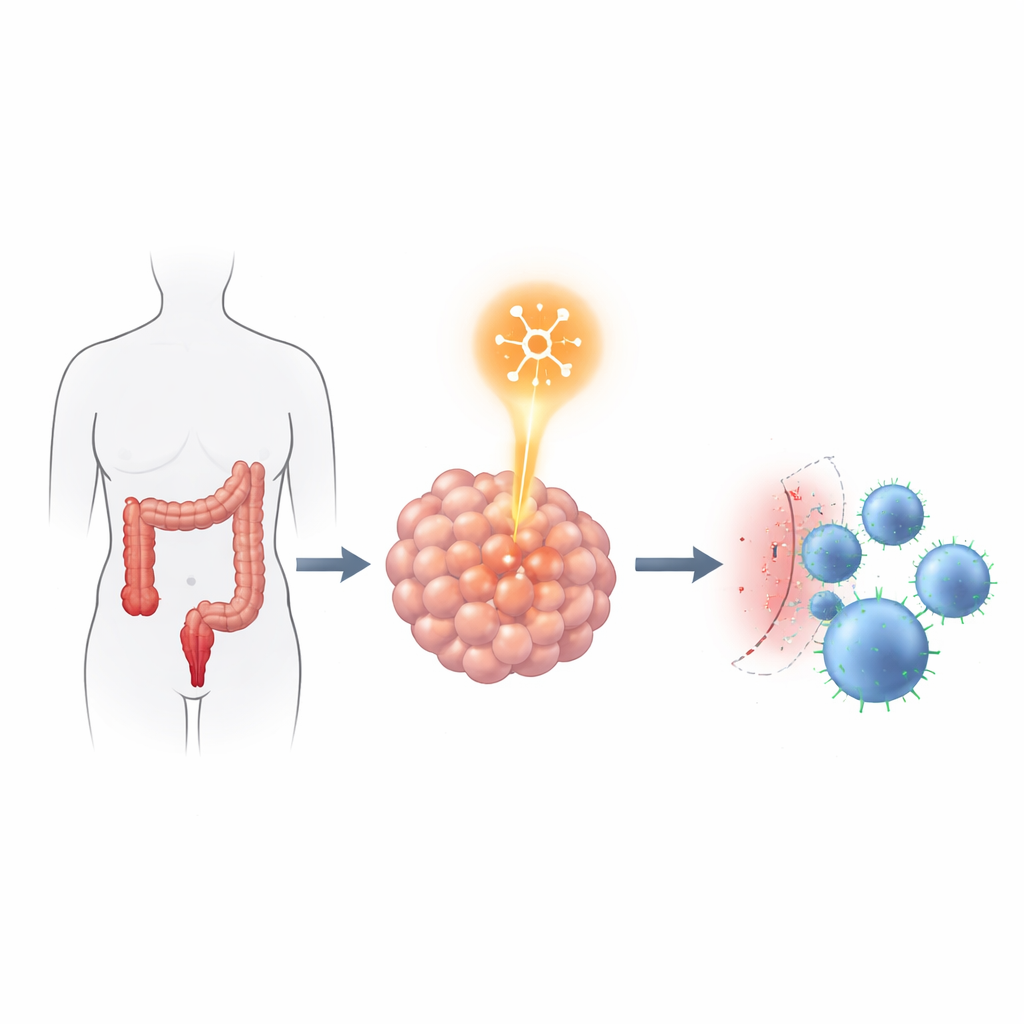
Powiązanie czytnika RNA z immunologicznym hamulcem
Zespół zapytał następnie, w jaki sposób YTHDF2 może pomagać guzom przetrwać ataki komórek odpornościowych. Przeszczepili ludzkie komórki raka jelita grubego z normalnym poziomem YTHDF2 lub bez niego do specjalnych myszy, którym podawano także ludzkie komórki odpornościowe. Guzy z normalnym YTHDF2 rosły szybciej i zawierały mniej T komórek zabijających raka. Po zmniejszeniu poziomu YTHDF2 guzy zmniejszyły się, a do guza napłynęło więcej limfocytów CD4 i CD8. Co istotne, obniżenie YTHDF2 nie zmieniało tempa wzrostu, migracji ani inwazyjności komórek nowotworowych w warunkach hodowlanych, co sugeruje, że jego główny wpływ dotyczy interakcji guza z układem odpornościowym, a nie bezpośredniej agresywności guza.
Jak komórki nowotworowe utrzymują wysoki poziom PD-L1
PD-L1 to białko na powierzchni komórek nowotworowych, które łączy się z PD-1 na limfocytach T i nakazuje im wstrzymać działanie. Badacze zaobserwowali, że po stłumieniu YTHDF2 ilość białka PD-L1 na komórkach nowotworowych i w wydzielanych przez nie pęcherzykach (egzosomach) gwałtownie spadała, nawet gdy poziomy RNA PD-L1 pozostawały mniej więcej takie same. Sugerowało to, że YTHDF2 wpływa na PD-L1 po etapie RNA, czyli pośrednio. Szczegółowe testy wykazały, że utrata YTHDF2 zmniejsza stabilność białka PD-L1 i ułatwia jego degradację przez komórkowe mechanizmy rozkładu białek oraz osłabia wiązanie między PD-1 a PD-L1. W rezultacie w doświadczeniach wspólnej hodowli limfocyty T zabijały więcej komórek nowotworowych przy niskim YTHDF2, co dowodzi funkcjonalnego wzmocnienia ataku immunologicznego.
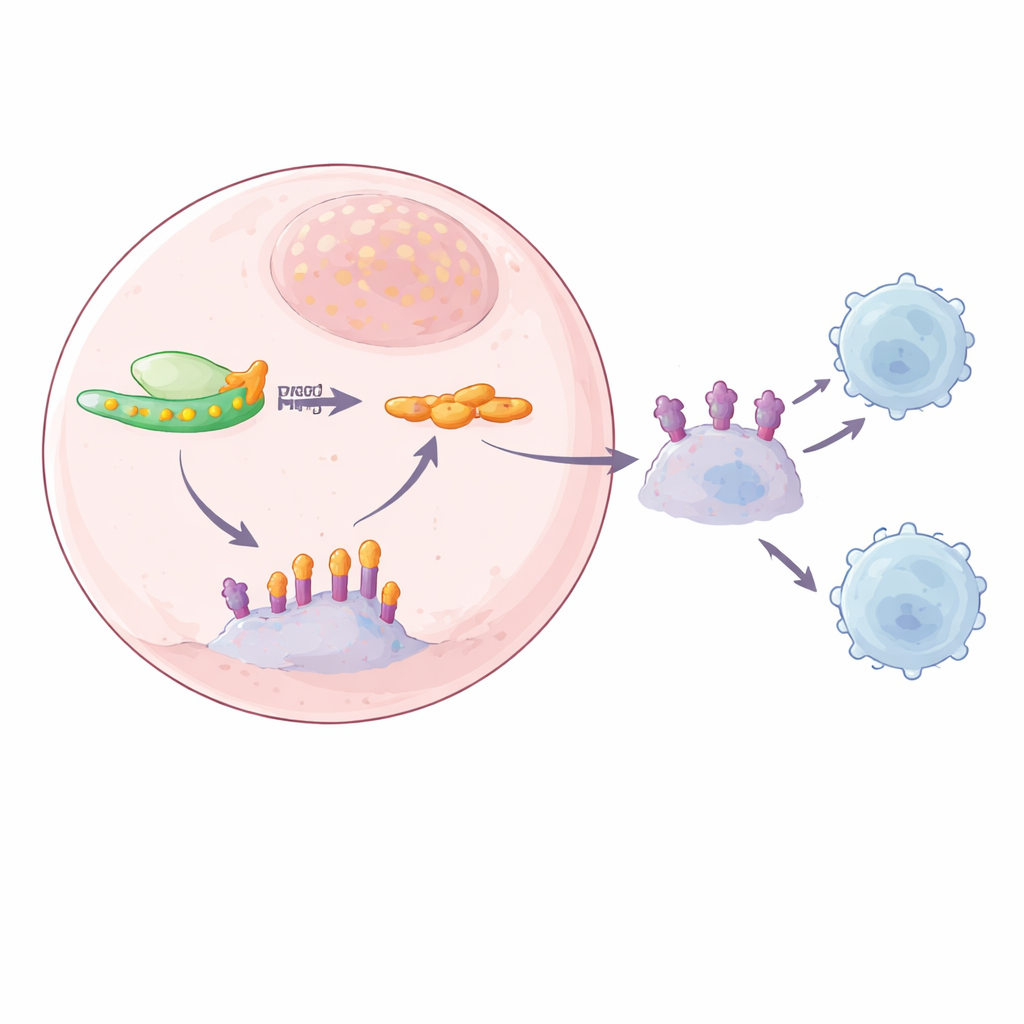
Powiązanie z SPOP: uszkodzony zespół sprzątający
Aby odnaleźć brakujące ogniwo między YTHDF2 a PD-L1, zespół połączył kilka podejść sekwencjonujących, by wyszukać RNA oznakowane m6A i wiążące się z YTHDF2. Jednym z silnych kandydatów okazał się SPOP, komponent kompleksu białkowego, który normalnie oznacza PD-L1 do degradacji, działając jak zespół sprzątający zapobiegający nagromadzeniu PD-L1. Autorzy wykryli znaczniki m6A w ogonie mRNA SPOP i pokazali, że YTHDF2 wiąże się dokładnie w tym miejscu. Gdy YTHDF2 występował w wysokich poziomach, mRNA SPOP było szybciej degradowane, co prowadziło do mniejszych ilości białka SPOP i mniejszego usuwania PD-L1. Po zmniejszeniu YTHDF2 mRNA SPOP stawało się bardziej stabilne, poziom białka SPOP rósł, a poziomy PD-L1 malały, zarówno na powierzchni komórkowej, jak i w egzosomach. Mutacje miejsc m6A na mRNA SPOP lub usunięcie samego SPOP przerywały ten łańcuch, potwierdzając, że zależna od m6A ścieżka YTHDF2–SPOP kontroluje obfitość PD-L1.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, praca ta ujawnia trzystopniowy przekaźnik w komórkach raka jelita grubego: znacznik m6A na RNA pozwala YTHDF2 obniżać poziomy SPOP; osłabiony SPOP nie jest w stanie prawidłowo usuwać PD-L1; w efekcie nadmiar PD-L1 chroni guz przed limfocytami T. Przerywając ten łańcuch — poprzez blokowanie YTHDF2 lub wzmacnianie SPOP — możliwe może być obniżenie PD-L1 na guzach i zwiększenie skuteczności istniejących leków przeciw PD-1/PD-L1, szczególnie u pacjentów, którzy obecnie odnoszą niewielką korzyść. Oś YTHDF2–SPOP–PD-L1 wyłania się zatem jako obiecujący nowy cel pomagający układowi odpornościowemu lepiej rozpoznawać i niszczyć raka jelita grubego.
Cytowanie: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Słowa kluczowe: rak jelita grubego, immunoterapia, PD-L1, modyfikacja RNA, ucieczka przed układem odpornościowym guza