Clear Sky Science · he
ירידה ב‑YTHDF2 מדכאת את ביטוי PD‑L1 על ידי ייצוב mRNA של SPOP שמכיל m6A בסרטן המעי הגס
מדוע מחקר זה חשוב
סרטן המעי הגס הוא אחד הסרטנים השכיחים והקטלניים ביותר ברחבי העולם. טיפולים מודרניים רבים מנסים לשחרר את מערכת החיסון של הגוף כדי לתקוף גידולים על‑ידי חסימת ה"בלם" שנקרא PD‑1/PD‑L1. יחד עם זאת, רוב חולי סרטן המעי הגס עדיין אינם נהנים מטיפול זה. המחקר חושף שרשרת מולקולרית נסתרת בתוך תאי הגידול שמסייעת להם לשמור על ה"בלם" החיסוני לחוץ. הבנת השרשרת הזו מציעה דרך חדשה להפוך את האימונותרפיה ליעילה עבור הרבה יותר מטופלים.
תג מסר נסתר על RNA של הגידול
התאים שלנו קוראים ומשמידים ללא הרף רצועות RNA, ההודעות קצרות‑החיים שאומרות אילו חלבונים לייצר. בשנים האחרונות מדענים גילו שרבים מההודעות הללו נושאות תגי כימיה זעירים, כולל תג שנקרא m6A, הפועל כמו סימוני עריכה במסמך: הם קובעים כמה זמן ההודעה תחזיק מעמד וכמה ביעילות תוקרא. חלבון בשם YTHDF2 מתמחה בזיהוי תגי m6A ובתנאים רגילים מסייע בפירוק ה‑RNA המסומן, וכך מכוונן אילו חלבונים התא מייצר. בדגימות סרטן המעי הגס של מטופלים ובמאגרי נתונים ציבוריים גדולים מצאו החוקרים שרמות YTHDF2 היו גבוהות משמעותית בגידולים בהשוואה לרקמת המעי הרגילה, ומטופלים עם כמות גבוהה יותר של YTHDF2 נטו להישרדות גרועה יותר, מה שמרמז על תפקיד תומך־סרטן ל"קורא" ה‑RNA הזה.
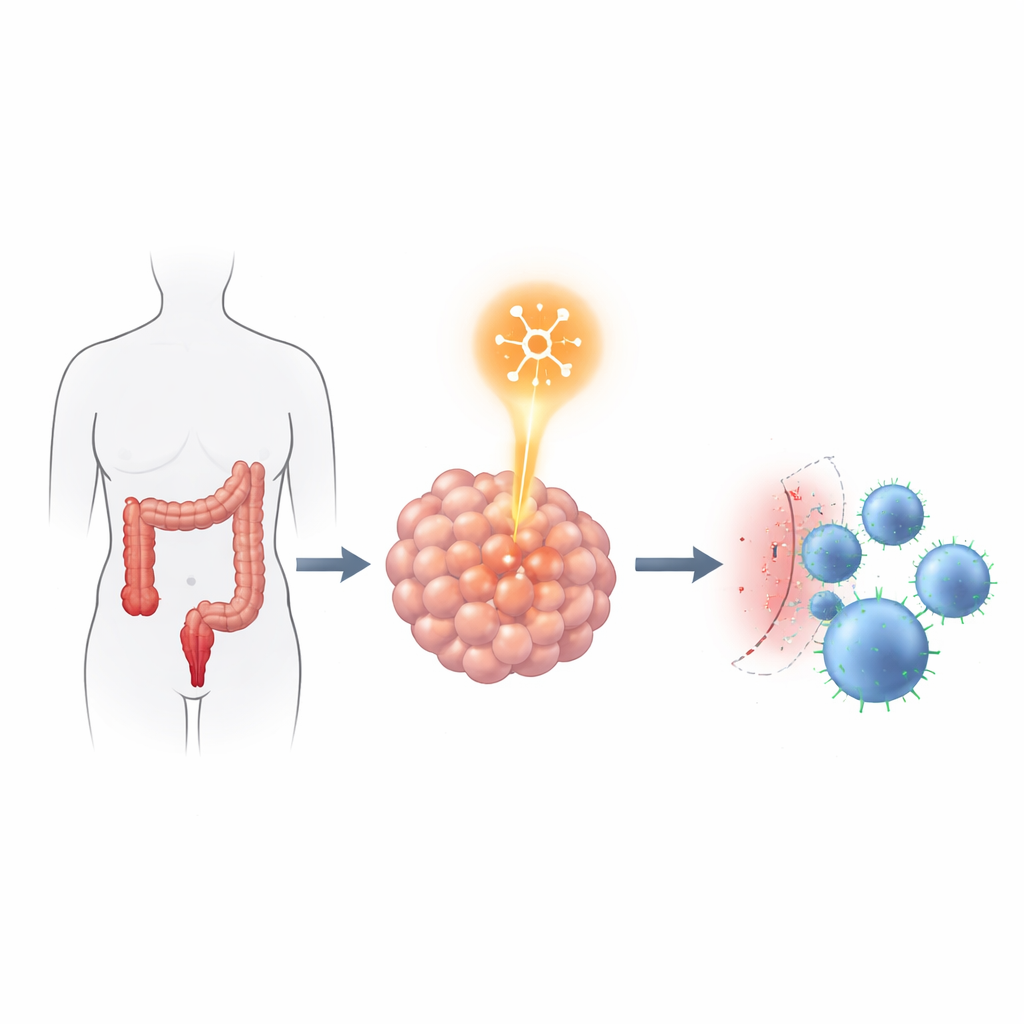
קישור ה"קורא" של ה‑RNA לבלם החיסוני
הצוות שאל בהמשך כיצד YTHDF2 עשוי לעזור לגידולים לעמוד בהתקפות של תאי חיסון. הם נטעו תאי סרטן מעיים אנושיים עם או בלי YTHDF2 בעכברים מיוחדים שקיבלו גם תאי חיסון אנושיים. גידולים עם YTHDF2 רגיל גדלו מהר יותר והראו פחות תאי T ההורגים סרטן במרכזם. כאשר YTHDF2 פחת, הגידולים כווצו ויותר תאי CD4 ו‑CD8 חדרו אל תוך הגידול. באופן מפתיע, הקטנת YTHDF2 לא שינתה את קצב הגידול, התנועה או היכולת להסתננות של התאים במבחנה, מה שמרמז שההשפעה העיקרית היא על האינטראקציה בין הגידול למערכת החיסון ולא על אגרסיביות הגידול עצמה.
כיצד תאי הגידול משמרים רמות גבוהות של PD‑L1
PD‑L1 הוא חלבון על פני תאי הגידול שמקשר ל‑PD‑1 על תאי T ומורה להם להירגע. החוקרים שמו לב שכאשר YTHDF2 דוכא, כמות חלבון PD‑L1 על התאים ובואקסוסומים שהם מפרישים ירדה משמעותית, אף על פי שרמות ה‑RNA של PD‑L1 נותרו דומות. הדבר רמז ש‑YTHDF2 משפיע על PD‑L1 בעקיפין, אחרי שלב ה‑RNA. בדיקות מפורטות הראו שאיבוד YTHDF2 עשה את חלבון PD‑L1 פחות יציב וקל יותר לפירוק על‑ידי מכונת הפירוק של החלבונים בתא, ופגם בקשירה בין PD‑1 ל‑PD‑L1. כתוצאה מכך, בניסויי תרביות משולבות תאי T הרגו יותר תאים סרטניים כאשר YTHDF2 היה נמוך, מה שמצביע על חיזוק פונקציונלי של ההתקפה החיסונית.
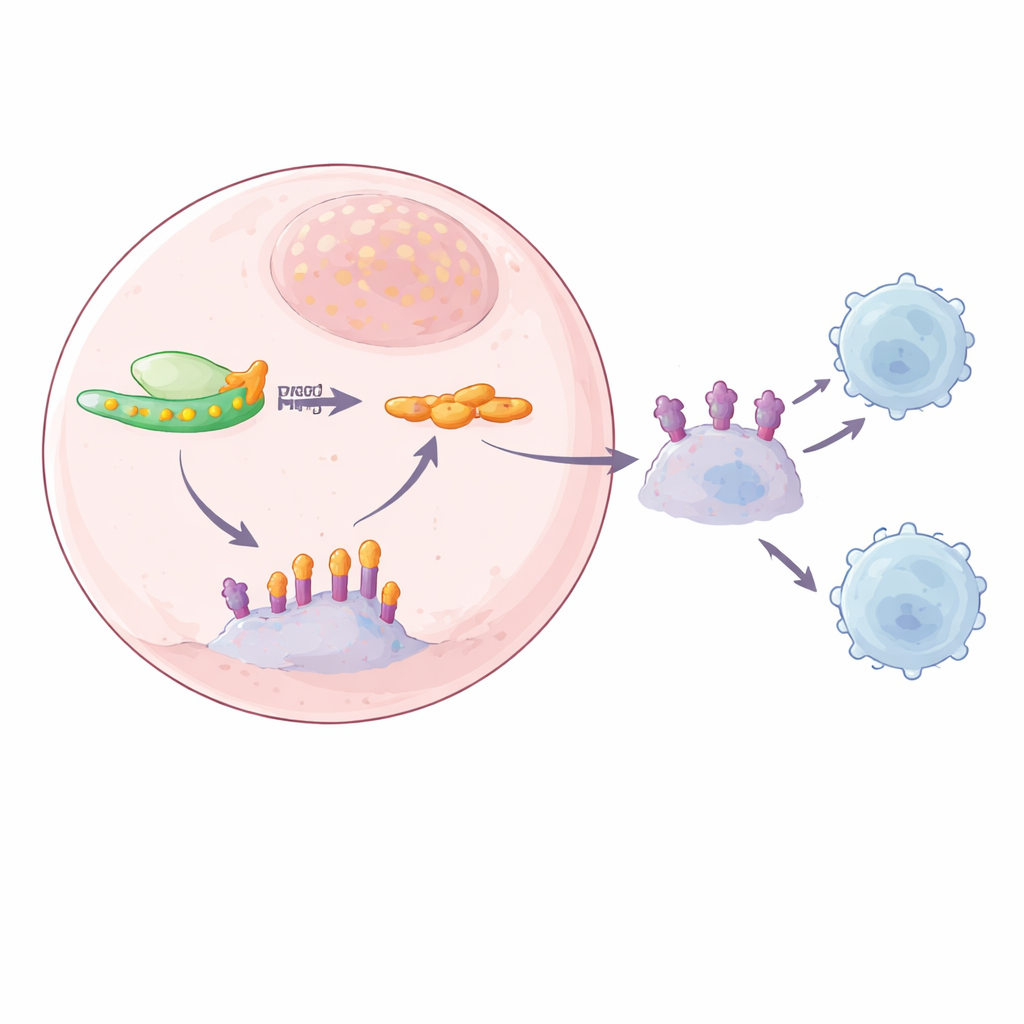
הקשר ל‑SPOP: צוות ניקיון שבור
כדי לעקוב אחרי הקישור החסר בין YTHDF2 ל‑PD‑L1, הצוות שילב כמה גישות ריצוף כדי לצוד הודעות RNA שנשאו m6A ושקושרו ל‑YTHDF2. מועמד חזק שנמצא היה SPOP, חלק מקומפלקס חלבוני שלרוב מתייג את PD‑L1 לפירוק, פועל כצוות ניקיון שמונע הצטברות PD‑L1. המחברים מצאו סימני m6A באזור הזנב של ה‑mRNA של SPOP והראו ש‑YTHDF2 נקשר בדיוק שם. כאשר YTHDF2 היה ברמות גבוהות, mRNA של SPOP נשבר מהר יותר, מה שהוביל לירידה בחלבון SPOP ופחות הסרה של PD‑L1. כשה‑YTHDF2 פחת, mRNA של SPOP נעשה יציב יותר, חלבון SPOP עלה ורמות PD‑L1 ירדו, הן על פני התא והן באקסוסומים. שינוי אתרי m6A ב‑mRNA של SPOP או הוצאת SPOP עצמו שברה את השרשרת הזו, ואישרה כי מסלול תלוי‑m6A של YTHDF2–SPOP שולט בשפע PD‑L1.
מה משמעות זה לטיפול בעתיד
במילים פשוטות, עבודה זו חושפת מעגל תלת‑שלבי בתוך תאי סרטן המעי הגס: תג ה‑m6A על ה‑RNA מאפשר ל‑YTHDF2 להפחית רמות SPOP; SPOP מוחלש אינו מצליח להסיר כראוי את PD‑L1; והרמות העודפות של PD‑L1 מגינות על הגידול מפני תאי T. על ידי הפרעה לשרשרת הזו — בין אם על‑ידי חסימת YTHDF2 או חיזוק SPOP — ייתכן שניתן להוריד את PD‑L1 על הגידולים ולהפוך את תרופות ה‑PD‑1/PD‑L1 הקיימות ליעילות יותר, במיוחד עבור מטופלים שכרגע נהנים ממעט תועלת. ציר YTHDF2–SPOP–PD‑L1 עולה אפוא כמטרה מבטיחה כדי לאפשר למערכת החיסון לזהות ולחסל טוב יותר את סרטן המעי הגס.
ציטוט: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
מילות מפתח: סרטן המעי הגס, אימונותרפיה, PD‑L1, שינויים ב‑RNA, בריחת מערכת החיסון הגידולית