Clear Sky Science · pt
Redução de YTHDF2 inibe a expressão de PD-L1 ao estabilizar o mRNA SPOP contendo m6A no câncer colorretal
Por que esta pesquisa é importante
O câncer colorretal é um dos cânceres mais comuns e letais no mundo. Muitos tratamentos modernos buscam liberar o próprio sistema imunológico do corpo para atacar tumores bloqueando um freio chamado PD-1/PD-L1. Ainda assim, a maioria dos pacientes com câncer colorretal não se beneficia desses medicamentos. Este estudo desvenda uma cadeia molecular oculta dentro das células tumorais que as ajuda a manter esse “freio” imune acionado. Compreender essa cadeia oferece uma nova maneira de tornar a imunoterapia eficaz para muito mais pessoas.
Uma etiqueta de mensagem oculta no RNA tumoral
Nossas células leem e destroem continuamente fitas de RNA, as mensagens de curta duração que dizem quais proteínas produzir. Nos últimos anos, cientistas descobriram que muitas mensagens de RNA carregam pequenas marcas químicas, incluindo uma chamada m6A, que atuam como marcas de edição em um manuscrito: decidem quanto tempo uma mensagem dura e com que intensidade ela é lida. Uma proteína chamada YTHDF2 se especializa em reconhecer essas marcas m6A e normalmente ajuda a degradar o RNA marcado, ajustando quais proteínas a célula produz. Em amostras de câncer colorretal de pacientes e em grandes bases de dados públicas, os autores encontraram níveis de YTHDF2 visivelmente mais altos nos tumores do que no tecido normal do cólon, e pacientes com mais YTHDF2 tendiam a ter pior sobrevida, apontando para um papel pró‑tumoral desse “leitor” de RNA.
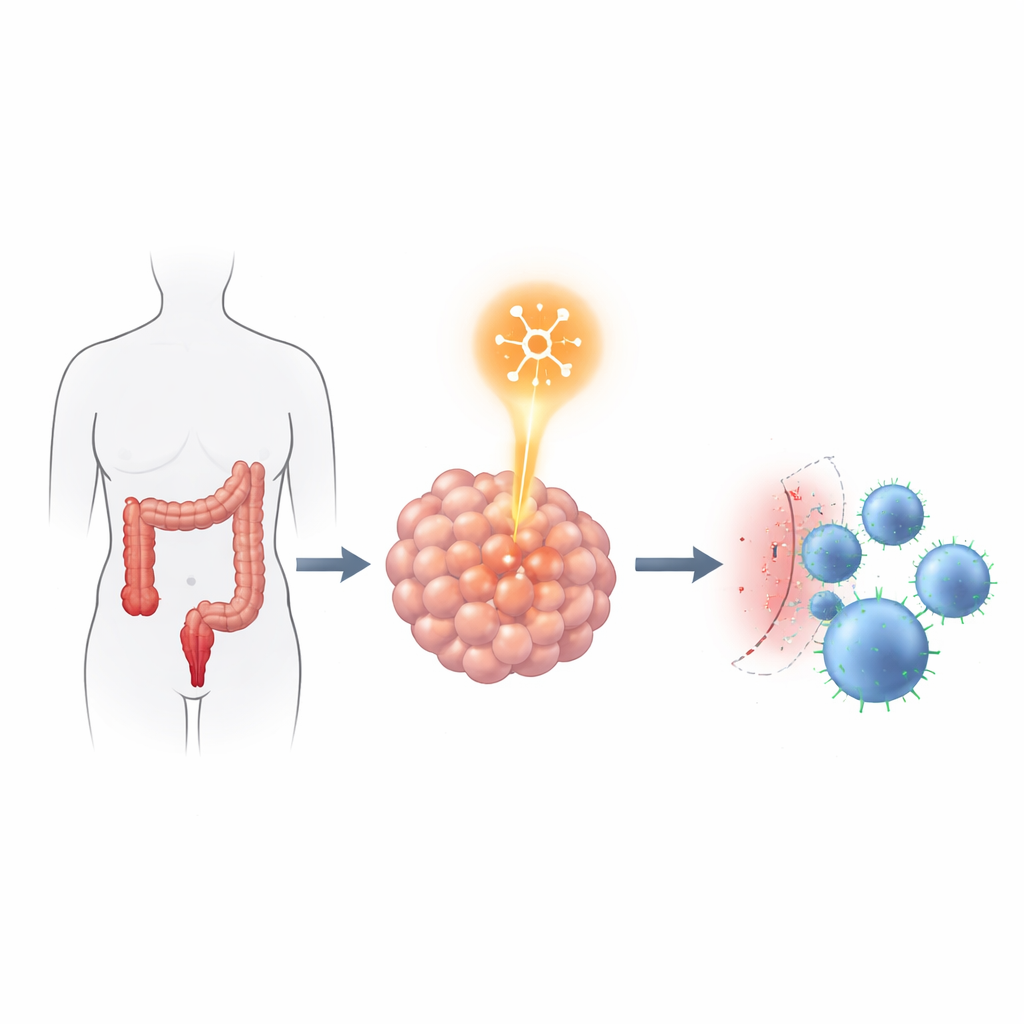
Ligando o leitor de RNA ao freio imune
A equipe investigou em seguida como YTHDF2 poderia ajudar os tumores a resistir a ataques de células imunes. Eles implantaram células humanas de câncer colorretal com ou sem YTHDF2 em camundongos especiais que também receberam células imunes humanas. Tumores com níveis normais de YTHDF2 cresceram mais rápido e mostraram menos células T citotóxicas infiltradas. Quando YTHDF2 foi reduzido, os tumores encolheram e mais células T CD4 e CD8 infiltraram o câncer. Notavelmente, a diminuição de YTHDF2 não alterou a velocidade de crescimento, migração ou invasão das células cancerosas em placas de cultura, sugerindo que seu principal impacto foi na interação do tumor com o sistema imunológico, e não na agressividade intrínseca do tumor.
Como as células tumorais mantêm PD-L1 alto
PD-L1 é uma proteína na superfície das células tumorais que se liga a PD-1 nas células T e as instrui a recuar. Os pesquisadores observaram que, quando YTHDF2 foi reduzido, a quantidade de proteína PD-L1 nas células cancerosas e em suas vesículas secretadas (exossomos) caiu acentuadamente, embora os níveis de RNA de PD-L1 permanecessem praticamente os mesmos. Isso sugeriu que YTHDF2 afeta PD-L1 de forma indireta, após a etapa do RNA. Testes detalhados mostraram que a perda de YTHDF2 tornou a proteína PD-L1 menos estável e mais suscetível à destruição pela maquinaria de degradação proteica da célula, e enfraqueceu a ligação entre PD-1 e PD-L1. Como resultado, em experimentos de co-cultura, células T mataram mais células cancerosas quando YTHDF2 estava baixo, demonstrando um aumento funcional no ataque imune.
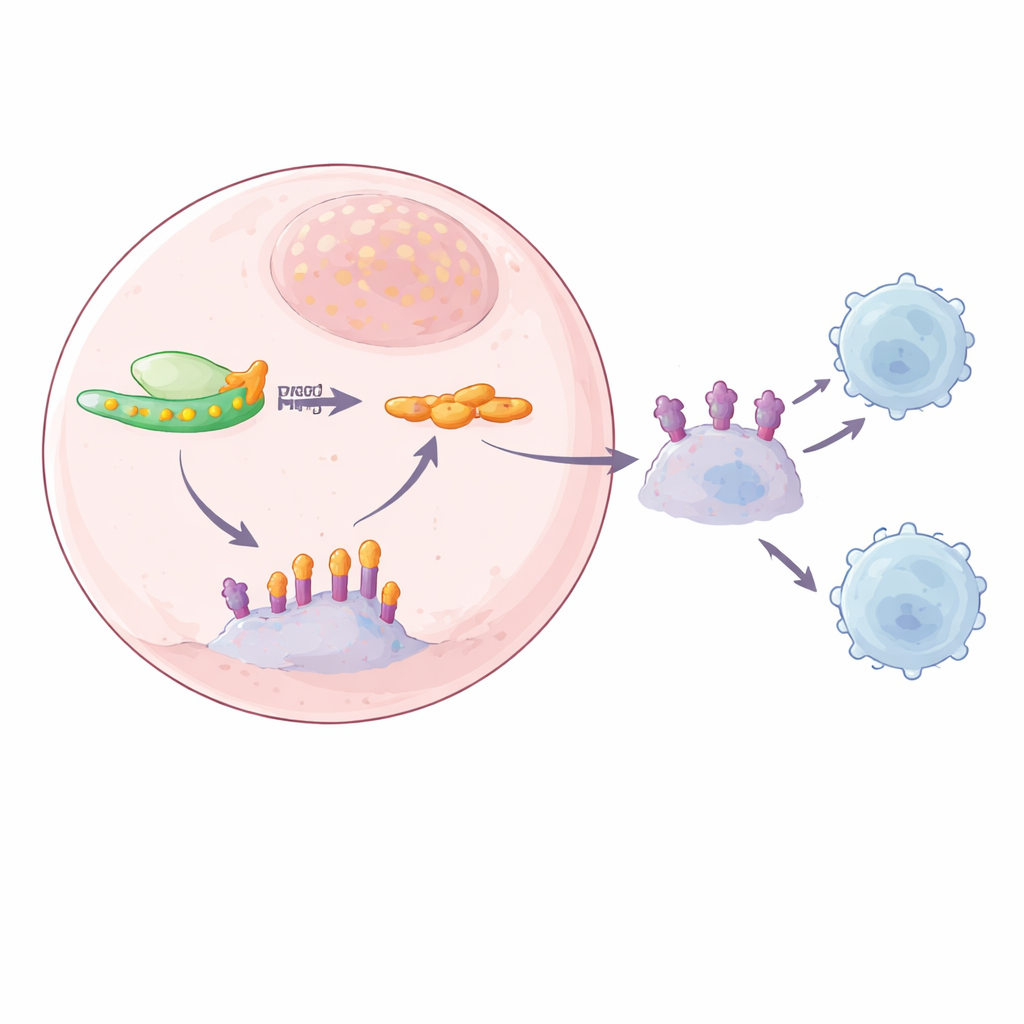
A conexão SPOP: uma equipe de limpeza comprometida
Para rastrear o elo perdido entre YTHDF2 e PD-L1, a equipe combinou várias abordagens de sequenciamento para buscar mensagens de RNA que fossem ao mesmo tempo marcadas com m6A e ligadas por YTHDF2. Um candidato forte foi SPOP, parte de um complexo proteico que normalmente marca PD-L1 para destruição, atuando como uma equipe de limpeza que impede o acúmulo de PD-L1. Os autores encontraram marcas m6A na região da cauda do RNA de SPOP e mostraram que YTHDF2 se liga exatamente ali. Quando YTHDF2 estava presente em altos níveis, o RNA de SPOP era degradado mais rapidamente, levando a níveis mais baixos de proteína SPOP e menos remoção de PD-L1. Quando YTHDF2 foi reduzido, o RNA de SPOP tornou-se mais estável, a proteína SPOP aumentou e os níveis de PD-L1 caíram, tanto na superfície celular quanto nos exossomos. Mutar os sítios de m6A no RNA de SPOP ou remover o próprio SPOP interrompeu essa cadeia, confirmando que a via dependente de m6A YTHDF2–SPOP controla a abundância de PD-L1.
O que isso significa para tratamentos futuros
Em termos simples, este trabalho revela um revezamento de três etapas dentro das células do câncer colorretal: a marca de RNA m6A permite que YTHDF2 reduza os níveis de SPOP; SPOP enfraquecido não consegue eliminar corretamente PD-L1; e o excesso resultante de PD-L1 protege o tumor das células T. Ao interromper esse revezamento — seja bloqueando YTHDF2 ou fortalecendo SPOP — pode ser possível reduzir PD-L1 nos tumores e tornar os medicamentos anti‑PD-1/PD-L1 existentes mais eficazes, especialmente para pacientes que atualmente se beneficiam pouco. O eixo YTHDF2–SPOP–PD-L1 assim surge como um novo alvo promissor para ajudar o sistema imunológico a reconhecer e destruir melhor o câncer colorretal.
Citação: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Palavras-chave: câncer colorretal, imunoterapia, PD-L1, modificação de RNA, evasão imune tumoral