Clear Sky Science · sv
Minskad YTHDF2 hämmar PD-L1-uttryck genom att stabilisera m6A‑innehållande SPOP-mRNA vid kolorektal cancer
Varför denna forskning är viktig
Kolorektal cancer är en av de vanligaste och mest dödliga cancerformerna globalt. Många moderna behandlingar försöker frigöra kroppens eget immunsystem för att angripa tumörer genom att blockera en broms som kallas PD-1/PD-L1. Trots det får fortfarande majoriteten av patienterna med kolorektal cancer inte nytta av dessa läkemedel. Denna studie avslöjar en dold molekylär kedjereaktion inuti cancerceller som hjälper dem att hålla denna immunbroms nedtryckt. Att förstå denna kedja ger en ny möjlighet att få immunterapin att fungera för betydligt fler patienter.
En dold märkning på tumörrna
Våra celler läser ständigt av och bryter ner RNA‑strängar, de kortlivade budskapen som talar om vilka proteiner som ska tillverkas. Under de senaste åren har forskare upptäckt att många RNA‑budskap bär små kemiska taggar, inklusive en som kallas m6A, som fungerar som redigeringsmärken i ett manus: de avgör hur länge ett budskap varar och hur starkt det läses. Ett protein som heter YTHDF2 är specialiserat på att känna igen dessa m6A‑taggar och hjälper vanligtvis till att bryta ner taggat RNA, vilket finjusterar vilka proteiner en cell producerar. I prover från patienter med kolorektal cancer och i stora publika databaser fann författarna att YTHDF2‑nivåerna var märkbart högre i tumörer än i normalt kolonvävnad, och att patienter med högre YTHDF2 tenderade att ha sämre överlevnad, vilket pekar på en cancerfrämjande roll för denna RNA‑”läsare”.
Kopplar RNA‑läsaren till immunbromsen
Gruppen undersökte sedan hur YTHDF2 kan hjälpa tumörer att stå emot attacker från immunceller. De inplanterade humana kolorektalcancerceller med eller utan YTHDF2 i särskilda möss som också fick mänskliga immunceller. Tumörer med normal YTHDF2 växte snabbare och visade färre cancerdödande T‑celler inuti. När YTHDF2 minskades krympte tumörerna och fler CD4‑ och CD8‑T‑celler infiltrerade cancern. Anmärkningsvärt var att sänkning av YTHDF2 inte förändrade hur snabbt cancercellerna delade sig, rörde sig eller invaderade i laboratorieodlingar, vilket tyder på att dess huvudpåverkan var hur tumören interagerade med immunsystemet snarare än på ren tumöraggressivitet.
Hur cancerceller håller PD-L1 högt
PD-L1 är ett protein på tumörcellernas yta som binder PD‑1 på T‑celler och säger åt dem att stå tillbaka. Forskarnas observationer visade att när YTHDF2 slog ned, föll mängden PD‑L1‑protein på cancerceller och i deras utsöndrande vesiklar (exosomer) kraftigt, trots att PD‑L1‑RNA‑nivåerna förblev ungefär desamma. Detta antydde att YTHDF2 påverkar PD‑L1 indirekt, efter RNA‑steget. Detaljerade tester visade att förlust av YTHDF2 gjorde PD‑L1‑proteinet mindre stabilt och lättare att brytas ner av cellens proteinnedbrytande maskineri, och försvagade bindningen mellan PD‑1 och PD‑L1. Som följd dödade T‑celler i samkulturförsök fler cancerceller när YTHDF2 var låg, vilket visade en funktionell förstärkning av immunangreppet.
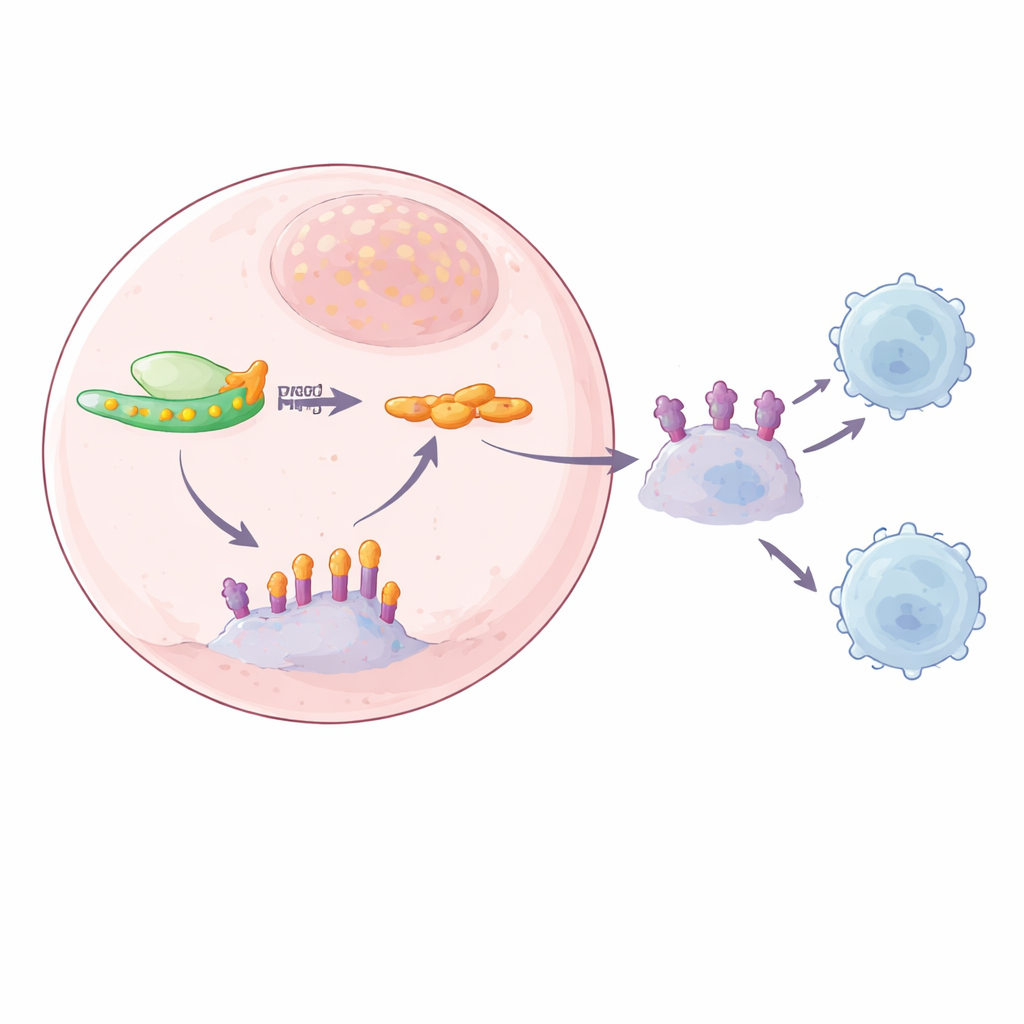
SPOP‑kopplingen: ett trasigt saneringsgäng
För att spåra den saknade länken mellan YTHDF2 och PD‑L1 kombinerade teamet flera sekvenseringsmetoder för att leta efter RNA‑budskap som både bar m6A och band till YTHDF2. En stark kandidat var SPOP, en del av ett proteinkomplex som normalt märker PD‑L1 för nedbrytning och fungerar som ett saneringsgäng som hindrar PD‑L1 från att ansamlas. Forskarna fann m6A‑markeringar i svanstermen av SPOP‑RNA och visade att YTHDF2 binder just där. När YTHDF2 fanns i höga nivåer bröts SPOP‑RNA ner snabbare, vilket ledde till lägre SPOP‑protein och mindre borttagning av PD‑L1. När YTHDF2 minskades blev SPOP‑RNA mer stabilt, SPOP‑protein ökade och PD‑L1‑proteinnivåerna föll, både på cellytan och i exosomer. Att mutera m6A‑platserna på SPOP‑RNA eller ta bort SPOP själv bröt denna kedja, vilket bekräftar att en m6A‑beroende YTHDF2–SPOP‑väg kontrollerar PD‑L1‑mängden.
Vad detta betyder för framtida behandling
Enkelt uttryckt visar detta arbete en trestegsrelay inuti kolorektala cancerceller: RNA‑taggen m6A tillåter YTHDF2 att skära ner SPOP‑nivåerna; försvagat SPOP kan inte ordentligt rensa bort PD‑L1; och den därmed uppkomna överskottet av PD‑L1 skärmar tumören från T‑celler. Genom att avbryta denna relay—antingen genom att blockera YTHDF2 eller stärka SPOP—kan det bli möjligt att sänka PD‑L1 på tumörer och göra befintliga PD‑1/PD‑L1‑läkemedel mer effektiva, särskilt för patienter som i dag får liten nytta. YTHDF2–SPOP–PD‑L1‑axeln framstår därmed som ett lovande nytt mål för att hjälpa immunsystemet att bättre känna igen och förgöra kolorektal cancer.
Citering: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Nyckelord: kolorektal cancer, immunterapi, PD-L1, RNA‑modifiering, tumörens immunflykt