Clear Sky Science · nl
Verminderde YTHDF2 remt PD-L1-expressie door stabilisatie van m6A-bevattend SPOP-mRNA bij colorectale kanker
Waarom dit onderzoek ertoe doet
Colorectale kanker is een van de meest voorkomende en dodelijke vormen van kanker wereldwijd. Veel moderne behandelingen proberen het eigen immuunsysteem van het lichaam te activeren om tumoren aan te vallen door een rem genaamd PD-1/PD-L1 weg te nemen. Toch profiteren de meeste patiënten met colorectale kanker nog steeds niet van deze medicijnen. Deze studie onthult een verborgen moleculaire kettingreactie in kankercellen die hen helpt die immuun“rem” ingedrukt te houden. Inzicht in deze keten biedt een nieuwe manier om immunotherapie voor veel meer mensen effectief te maken.
Een verborgen label op tumor-RNA
Onze cellen lezen en vernietigen voortdurend RNA-strengen, de kortlevende berichtjes die vertellen welke eiwitten gemaakt moeten worden. De afgelopen jaren ontdekten wetenschappers dat veel RNA-berichtjes kleine chemische labels dragen, waaronder één genaamd m6A, die werken als correctiemarkeringen in een manuscript: ze bepalen hoe lang een bericht blijft bestaan en hoe sterk het wordt afgelezen. Een eiwit genaamd YTHDF2 is gespecialiseerd in het herkennen van deze m6A-labels en helpt normaal gesproken bij het afbreken van gelabeld RNA, waarmee het regelt welke eiwitten een cel produceert. In monsters van colorectale tumoren van patiënten en in grote openbare databanken vonden de auteurs dat YTHDF2-niveaus duidelijk hoger waren in tumoren dan in normaal colonweefsel, en dat patiënten met meer YTHDF2 doorgaans een slechtere overleving hadden, wat wijst op een kankerversterende rol voor deze RNA-“lezer”.
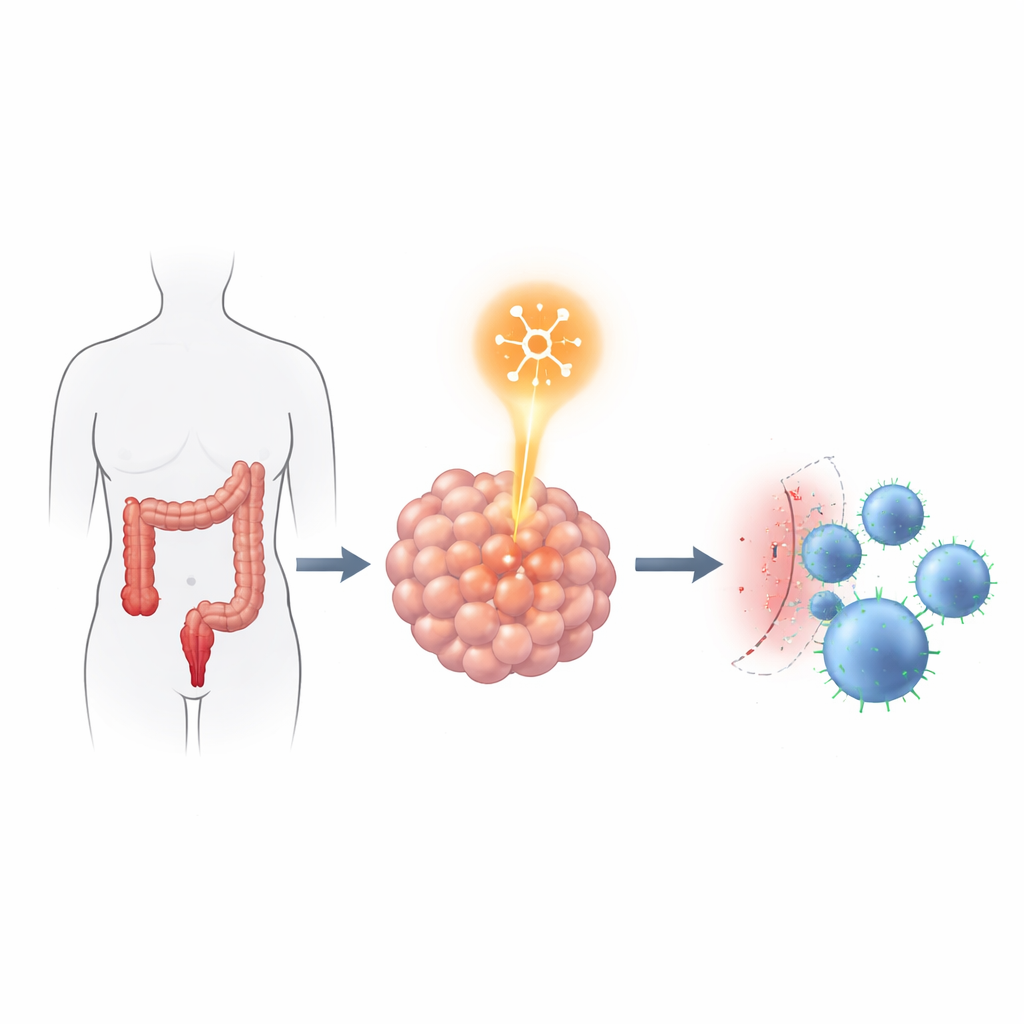
De RNA-lezer koppelen aan de immuunrem
Het team onderzocht vervolgens hoe YTHDF2 tumoren zou kunnen helpen aanvallen door immuuncellen te weerstaan. Ze implanteerden menselijke colorectale kankercellen met of zonder YTHDF2 in speciale muizen die ook menselijke immuuncellen ontvingen. Tumoren met normale YTHDF2 groeiden sneller en toonden minder kankerdodende T-cellen van binnenuit. Wanneer YTHDF2 werd verminderd, krimpten tumoren en drongen meer CD4- en CD8-T-cellen de tumor binnen. Opmerkelijk was dat het verlagen van YTHDF2 de snelheid waarmee kankercellen groeiden, bewogen of invasief werden in kweekschalen niet veranderde, wat suggereert dat de belangrijkste impact ligt op de interactie van de tumor met het immuunsysteem in plaats van op de ruwe agressiviteit van de tumor.
Hoe kankercellen PD-L1 hoog houden
PD-L1 is een eiwit op het oppervlak van tumorcellen dat bindt aan PD-1 op T-cellen en hen tot kalmte aanzet. De onderzoekers zagen dat wanneer YTHDF2 werd uitgeschakeld, de hoeveelheid PD-L1-eiwit op kankercellen en in hun uitgescheiden blaasjes (exosomen) scherp daalde, hoewel de PD-L1-RNA-niveaus ongeveer gelijk bleven. Dit suggereerde dat YTHDF2 PD-L1 indirect beïnvloedt, na het RNA-stadium. Gedetailleerde tests toonden aan dat verlies van YTHDF2 PD-L1-eiwit minder stabiel maakte en gemakkelijker door de eiwitsloopmachinerie van de cel liet afbreken, en dat het de binding tussen PD-1 en PD-L1 verzwakte. Als gevolg daarvan doodden T-cellen in co-kweekexperimenten meer kankercellen wanneer YTHDF2 laag was, wat een functionele versterking van de immuunaanval liet zien.
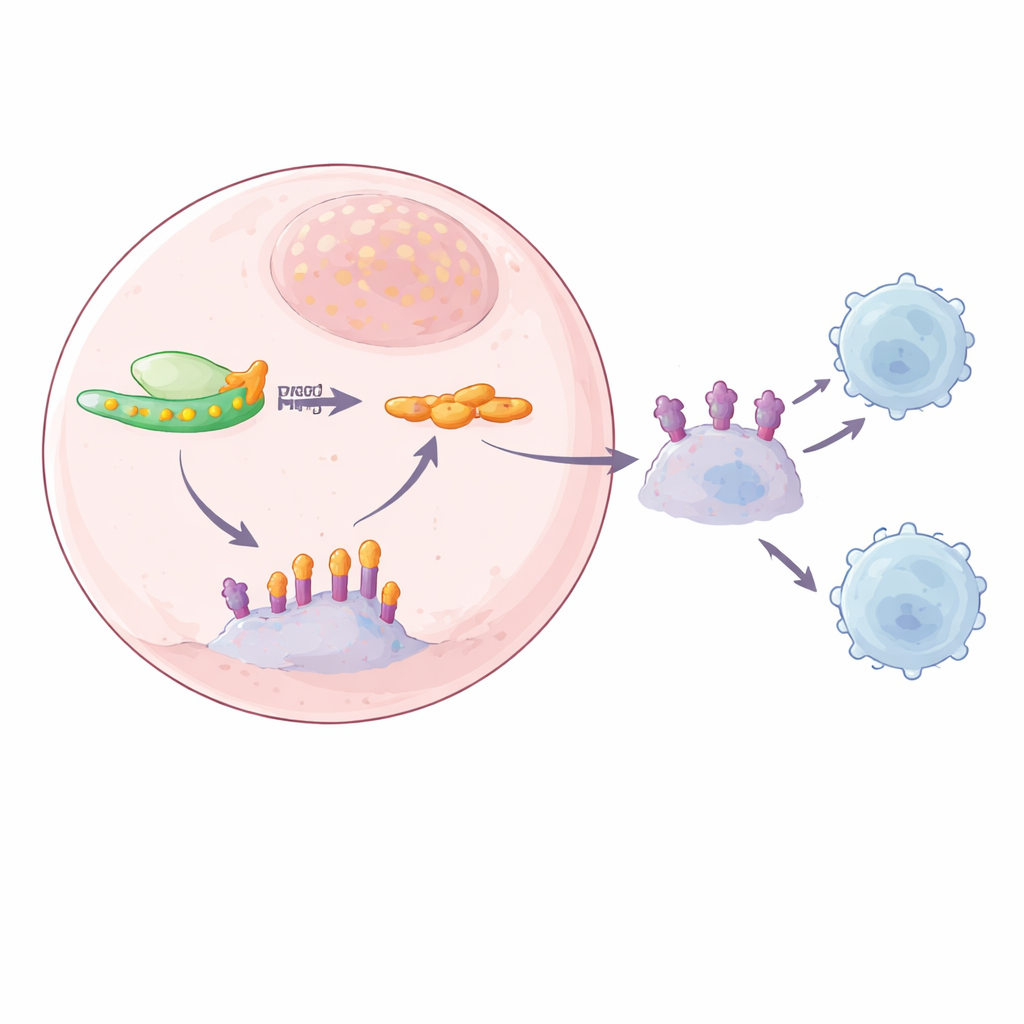
De SPOP-koppeling: een kapot opruimteam
Om de ontbrekende schakel tussen YTHDF2 en PD-L1 op te sporen, combineerde het team meerdere sequencing-benaderingen om RNA-berichtjes te zoeken die zowel m6A-gelabeld waren als door YTHDF2 werden gebonden. Een sterke kandidaat was SPOP, onderdeel van een eiwitcomplex dat normaal gesproken PD-L1 markeert voor vernietiging, fungerend als een opruimcrew die voorkomt dat PD-L1 zich ophoopt. De auteurs vonden m6A-markeringen in het staartgebied van SPOP-RNA en toonden aan dat YTHDF2 daar precies bindt. Wanneer YTHDF2 in hoge mate aanwezig was, werd SPOP-RNA sneller afgebroken, wat leidde tot lagere SPOP-eiwitniveaus en minder verwijdering van PD-L1. Toen YTHDF2 werd verminderd, werd SPOP-RNA stabieler, nam SPOP-eiwit toe en daalde PD-L1-eiwit zowel op het celoppervlak als in exosomen. Het muteren van de m6A-sites op SPOP-RNA of het verwijderen van SPOP zelf onderbrak deze keten, wat bevestigt dat een m6A-afhankelijke YTHDF2–SPOP-route de PD-L1-hoeveelheid regelt.
Wat dit betekent voor toekomstige behandeling
In eenvoudige bewoordingen onthult dit werk een driedelige estafette binnen colorectale kankercellen: het RNA-label m6A maakt het mogelijk dat YTHDF2 SPOP-niveaus verlaagt; verzwakt SPOP kan PD-L1 niet adequaat opruimen; en het resulterende overschot aan PD-L1 beschermt de tumor tegen T-cellen. Door deze estafette te onderbreken—ofwel door YTHDF2 te remmen of SPOP te versterken—zou het mogelijk kunnen zijn PD-L1 op tumoren te verlagen en bestaande PD-1/PD-L1-middelen effectiever te maken, vooral voor patiënten die momenteel weinig baat hebben. De YTHDF2–SPOP–PD-L1-as komt daarmee naar voren als een veelbelovend nieuw doel om het immuunsysteem beter kleur te laten herkennen en colorectale kanker te vernietigen.
Bronvermelding: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Trefwoorden: colorectale kanker, immunotherapie, PD-L1, RNA-modificatie, tumorimmuunontsnapping