Clear Sky Science · ru
Снижение YTHDF2 подавляет экспрессию PD-L1 за счёт стабилизации m6A-содержащей мРНК SPOP при колоректальном раке
Почему это исследование важно
Колоректальный рак — один из самых распространённых и смертоносных видов рака в мире. Многие современные методы лечения пытаются задействовать собственную иммунную систему организма для атаки опухолей, блокируя «тормоз» PD-1/PD-L1. Тем не менее большинство пациентов с колоректальным раком по-прежнему не получают пользы от этих препаратов. В этом исследовании раскрыта скрытая молекулярная цепочка реакций внутри раковых клеток, которая помогает им удерживать этот иммунный «тормоз» включённым. Понимание этой цепочки открывает новый путь для повышения эффективности иммунотерапии для многих пациентов.
Скрытая метка в сообщениях РНК опухоли
Наши клетки постоянно считывают и уничтожают молекулы РНК — краткоживущие сообщения, которые указывают, какие белки синтезировать. В последние годы учёные обнаружили, что многие РНК несут крошечные химические метки, включая метку m6A, которые действуют как правки в тексте: они определяют, как долго сообщение хранится и насколько активно его переводят в белок. Белок YTHDF2 специализированно распознаёт эти m6A-метки и обычно помогает разрушать отмеченную РНК, тонко регулируя набор белков, которые производит клетка. В образцах колоректального рака пациентов и в крупных публичных базах данных авторы обнаружили, что уровень YTHDF2 в опухолях заметно выше, чем в нормальной ткани толстой кишки, а у пациентов с повышенным YTHDF2 выживаемость в целом была хуже, что указывает на пронее роль этого «ридера» РНК.
Связь ридера РНК с иммунным тормозом
Далее команда изучила, как YTHDF2 может помогать опухолям противостоять атаке иммунных клеток. Они имплантировали человеческие клетки колоректального рака с нормальным уровнем YTHDF2 или с его снижением в специальные мыши, которым также вводили человеческие иммунные клетки. Опухоли с нормальным YTHDF2 росли быстрее и содержали меньше Т‑клеток, убивающих раковые клетки. При снижении YTHDF2 опухоли уменьшались, и в тканях появлялось больше CD4‑ и CD8‑Т-клеток. Примечательно, что понижение YTHDF2 не меняло скорость роста, миграции или инвазии раковых клеток в клеточных культурах, что свидетельствует о том, что его основной эффект связан с взаимодействием опухоли с иммунной системой, а не с чистой агрессивностью опухоли.
Как опухолевые клетки поддерживают высокий PD-L1
PD-L1 — белок на поверхности опухолевых клеток, который связывается с PD-1 на Т‑клетках и заставляет их «сойти с ума» — прекратить атаки. Исследователи заметили, что при снижении YTHDF2 количество белка PD-L1 на клетках и в секретируемых ими везикулах (экзосомах) резко уменьшалось, хотя уровни мРНК PD-L1 оставались примерно на том же уровне. Это навело на мысль, что YTHDF2 влияет на PD-L1 косвенно, на посттранскрипционном уровне. Детальные эксперименты показали, что потеря YTHDF2 делала белок PD-L1 менее стабильным и более уязвимым для уничтожения клеточным протеасомным аппаратом, а также ослабляла взаимодействие между PD-1 и PD-L1. В результате в экспериментах с совместной культурой Т‑клетки убивали больше раковых клеток при низком уровне YTHDF2, демонстрируя функциональное усиление иммунного ответа.
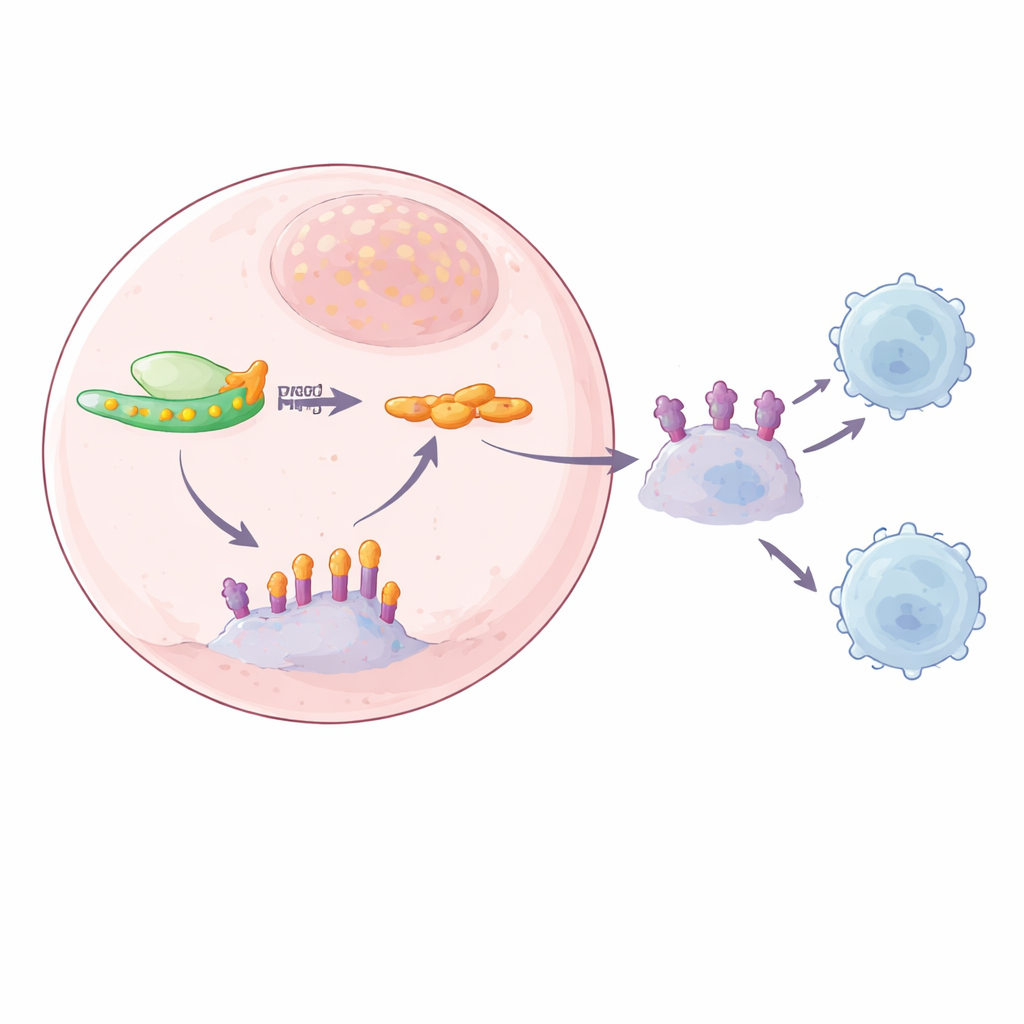
Связь с SPOP: сломанная служба уборки
Чтобы проследить недостающую ссылку между YTHDF2 и PD-L1, команда объединила несколько секвенирующих подходов в поисках мРНК, содержащих m6A и одновременно связанных с YTHDF2. Одним из сильных кандидатов оказался SPOP — часть белкового комплекса, который обычно помечает PD-L1 для разрушения, выступая в роли службы уборки, не позволяющей PD-L1 накапливаться. Авторы выявили m6A‑метки в хвостовой (3'-UTR) области мРНК SPOP и показали, что YTHDF2 связывается именно там. При высоком уровне YTHDF2 мРНК SPOP разрушалась быстрее, что приводило к снижению белка SPOP и уменьшению удаления PD-L1. Когда YTHDF2 снижали, мРНК SPOP становилась более стабильной, уровень белка SPOP повышался, и уровни PD-L1 падали как на поверхности клетки, так и в экзосомах. Мутации в сайтах m6A на мРНК SPOP или удаление самого SPOP разрушали эту цепочку, подтверждая, что m6A‑зависимый путь YTHDF2–SPOP контролирует количество PD-L1.
Что это значит для будущего лечения
Проще говоря, в этой работе описан трёхэтапный ретранслятор внутри клеток колоректального рака: метка m6A на мРНК позволяет YTHDF2 снижать уровень SPOP; ослабленный SPOP не в состоянии эффективно убирать PD-L1; в результате избыток PD-L1 защищает опухоль от Т‑клеток. Прерывая эту цепочку — либо блокируя YTHDF2, либо усиливая SPOP — возможно снизить уровень PD-L1 в опухолях и повысить эффективность существующих препаратов против PD-1/PD-L1, особенно у тех пациентов, которые сейчас получают мало пользы. Ось YTHDF2–SPOP–PD-L1 таким образом выступает многообещающей новой мишенью для того, чтобы помочь иммунной системе лучше распознавать и уничтожать колоректальный рак.
Цитирование: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Ключевые слова: колоректальный рак, иммунотерапия, PD-L1, модификация РНК, иммунное уклонение опухоли