Clear Sky Science · it
La riduzione di YTHDF2 inibisce l’espressione di PD-L1 stabilizzando l’mRNA SPOP contenente m6A nel cancro colorettale
Perché questa ricerca è importante
Il cancro colorettale è uno dei tumori più comuni e letali a livello globale. Molti trattamenti moderni cercano di liberare il sistema immunitario per attaccare i tumori bloccando un freno noto come PD-1/PD-L1. Tuttavia, la maggior parte dei pazienti con cancro colorettale non ottiene ancora benefici da questi farmaci. Questo studio svela una catena molecolare nascosta all’interno delle cellule tumorali che le aiuta a mantenere premuto quel “freno” immunitario. Comprendere questa catena offre una nuova strategia per rendere l’immunoterapia efficace per molti più pazienti.
Un tag di messaggio nascosto sull’RNA tumorale
Le nostre cellule leggono e degradano costantemente filamenti di RNA, i messaggi di breve durata che indicano quali proteine produrre. Negli ultimi anni gli scienziati hanno scoperto che molti messaggi RNA portano piccoli tag chimici, incluso uno chiamato m6A, che funzionano come segni editoriali in un manoscritto: determinano quanto a lungo un messaggio rimane e quanto viene tradotto. Una proteina chiamata YTHDF2 è specializzata nel riconoscere questi tag m6A e di solito contribuisce a degradare l’RNA marcato, regolando finemente quali proteine una cellula produce. Nei campioni di cancro colorettale di pazienti e in grandi banche dati pubbliche, gli autori hanno trovato che i livelli di YTHDF2 erano nettamente più alti nei tumori rispetto al tessuto colico normale, e che i pazienti con più YTHDF2 tendevano ad avere una sopravvivenza peggiore, indicando un ruolo pro‑tumorale per questo “lettore” di RNA.
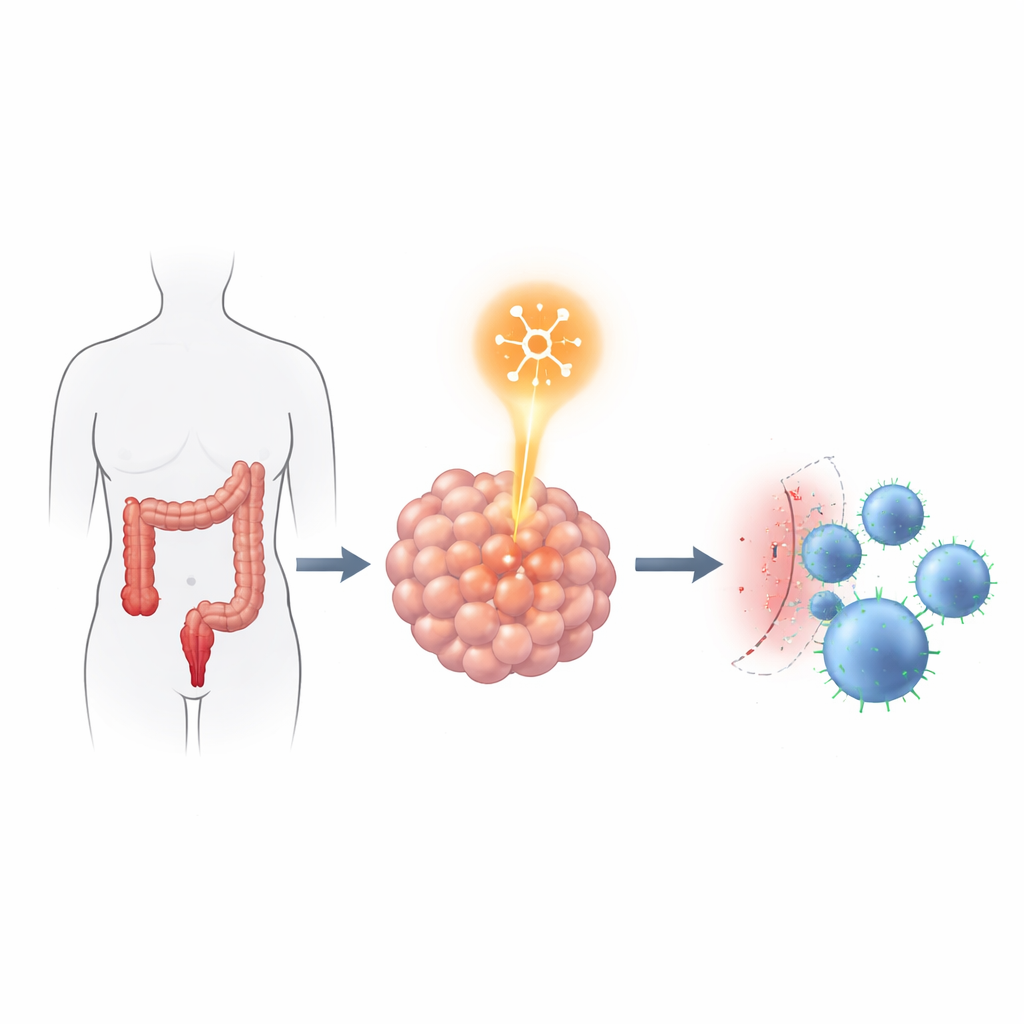
Collegare il lettore di RNA al freno immunitario
Il gruppo ha poi indagato come YTHDF2 possa aiutare i tumori a resistere agli attacchi delle cellule immunitarie. Hanno impiantato cellule di cancro colorettale umano con o senza YTHDF2 in topi speciali che ricevevano anche cellule immunitarie umane. I tumori con livelli normali di YTHDF2 crescevano più rapidamente e mostravano meno cellule T che uccidono il cancro al loro interno. Quando YTHDF2 veniva ridotto, i tumori si contraevano e un maggior numero di cellule T CD4 e CD8 infiltrava il tumore. In modo significativo, la riduzione di YTHDF2 non cambiava la velocità di crescita, la migrazione o l’invasione delle cellule tumorali in coltura, suggerendo che il suo impatto principale riguarda l’interazione del tumore con il sistema immunitario piuttosto che l’aggressività intrinseca del tumore.
Come le cellule tumorali mantengono alto PD-L1
PD-L1 è una proteina sulla superficie delle cellule tumorali che si lega a PD-1 sulle cellule T e le invita a fermarsi. I ricercatori hanno osservato che quando YTHDF2 veniva silenziato, la quantità di proteina PD-L1 sulle cellule tumorali e nelle loro vescicole secrete (esosomi) diminuiva drasticamente, anche se i livelli di RNA di PD-L1 restavano pressoché invariati. Questo suggeriva che YTHDF2 influenza PD-L1 in modo indiretto, dopo la fase dell’RNA. Test dettagliati hanno mostrato che la perdita di YTHDF2 rendeva la proteina PD-L1 meno stabile e più facilmente degradata dalla macchina cellulare di smaltimento delle proteine, e indeboliva il legame tra PD-1 e PD-L1. Di conseguenza, nelle esperienze in co-coltura le cellule T uccidevano più cellule tumorali quando YTHDF2 era basso, mostrando un aumento funzionale dell’attacco immunitario.
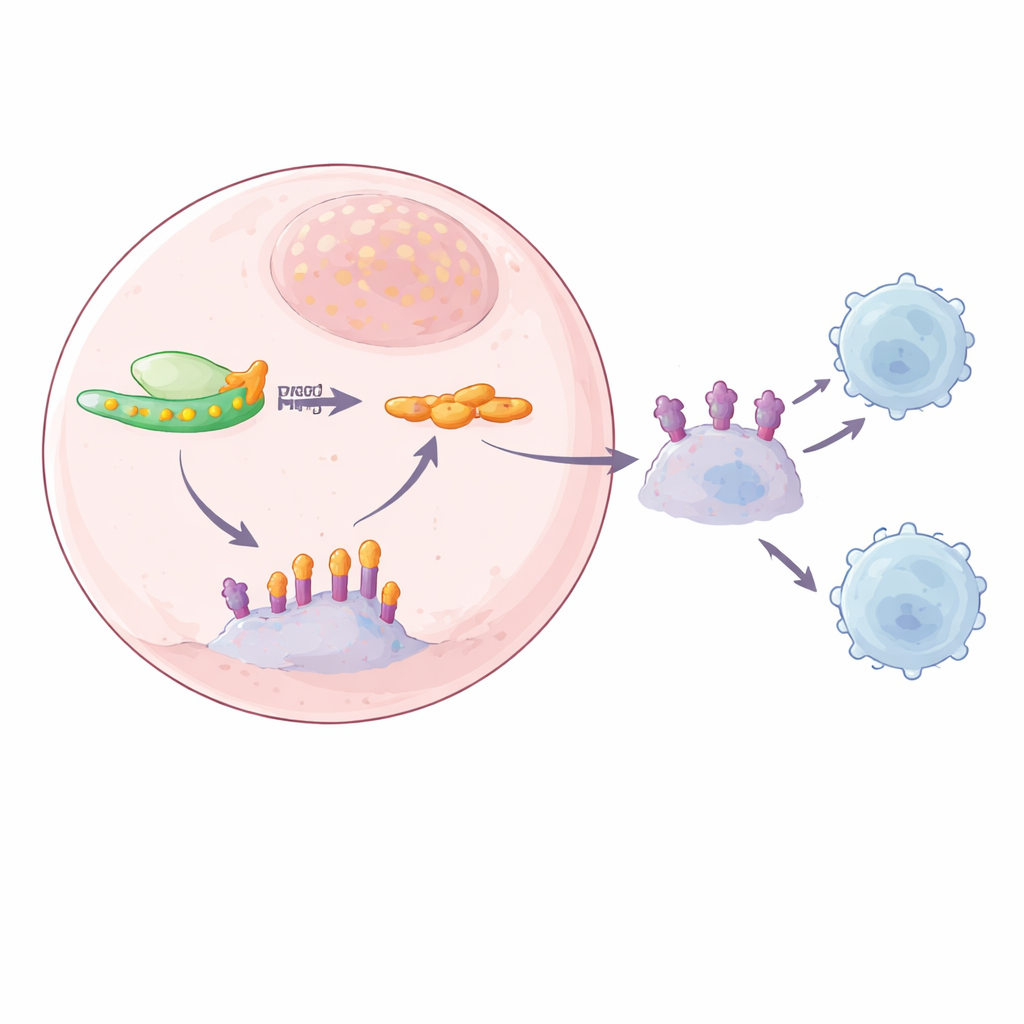
La connessione con SPOP: una squadra di pulizia compromessa
Per rintracciare il collegamento mancante tra YTHDF2 e PD-L1, il team ha combinato diversi approcci di sequenziamento per cercare messaggi RNA che fossero sia marcati con m6A sia legati da YTHDF2. Un candidato forte è risultato essere SPOP, parte di un complesso proteico che normalmente marca PD-L1 per la distruzione, agendo come una squadra di pulizia che evita l’accumulo di PD-L1. Gli autori hanno trovato marche m6A nella regione terminale dell’RNA di SPOP e hanno dimostrato che YTHDF2 si lega precisamente lì. Quando YTHDF2 era presente a livelli elevati, l’RNA di SPOP veniva degradato più rapidamente, portando a una diminuzione della proteina SPOP e a una ridotta eliminazione di PD-L1. Quando YTHDF2 veniva ridotto, l’RNA di SPOP diventava più stabile, la proteina SPOP aumentava e i livelli di PD-L1 diminuivano, sia sulla superficie cellulare che negli esosomi. La mutazione dei siti m6A sull’RNA di SPOP o la rimozione dello stesso SPOP interrompeva questa catena, confermando che una via dipendente da m6A YTHDF2–SPOP controlla l’abbondanza di PD-L1.
Cosa significa per i trattamenti futuri
In termini semplici, questo lavoro rivela una staffetta a tre passaggi all’interno delle cellule del cancro colorettale: il tag m6A sull’RNA permette a YTHDF2 di ridurre i livelli di SPOP; uno SPOP indebolito non riesce a smaltire correttamente PD-L1; e l’eccesso di PD-L1 risultante protegge il tumore dalle cellule T. Interrompendo questa staffetta—o bloccando YTHDF2 o rafforzando SPOP—potrebbe essere possibile abbassare PD-L1 nei tumori e rendere più efficaci i farmaci anti‑PD-1/PD-L1 esistenti, specialmente per i pazienti che attualmente ottengono pochi benefici. L’asse YTHDF2–SPOP–PD-L1 emerge così come un promettente nuovo bersaglio per aiutare il sistema immunitario a riconoscere e distruggere meglio il cancro colorettale.
Citazione: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Parole chiave: cancro colorettale, immunoterapia, PD-L1, modifica dell'RNA, fuga immunitaria tumorale